2021年山東省泰安市肥城市高考化學適應性試卷(三)
發布:2024/4/20 14:35:0
一、選擇題(本題共10小題,每小題2分,共20分。每小題只有一個選項符合題意)
-
1.科技發展離不開化學。下列說法不正確的是( )
A.“直上云霄”:客機所用燃油是石油的分餾產物 B.“乘風破浪”:航母上的鈦合金鉚釘可抗海水腐蝕 C.“一帶一路”:絲綢制品成分的90%都是纖維素,能發生酯化反應 D.“筑夢天宮”:液氫、液氧替代四氧化二氮、偏二甲肼作為推進劑,對環境更友好 組卷:24引用:2難度:0.6 -
2.科學家發現了利用淚液來檢測糖尿病的方法,其原理是用氯金酸鈉(NaAuCl4)溶液與淚液中的葡萄糖發生反應生成納米金單質顆粒(直徑為20~60nm)。下列說法錯誤的是( )
A.氯金酸鈉中金元素為+3價 B.氯金酸鈉是配位化合物 C.葡萄糖發生還原反應 D.反應后的分散系可產生丁達爾效應 組卷:64引用:6難度:0.7 -
3.用NA表示阿伏加德羅常數的值。下列敘述正確的是( )
A.電解精煉銅時,若轉移了NA個電子,則陽極溶解32g銅 B.300mL 2mol?L-1蔗糖溶液中所含分子數為0.6NA C.反應 Ca+4820Cf→24998Og+x294118n中,每生成294g10Og釋放的中子數為3NA294118D.常溫下,5.6g鐵釘與足量濃硝酸反應,轉移的電子數為0.3NA 組卷:51引用:1難度:0.8 -
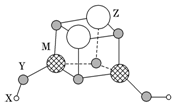 4.短周期元素X、Y、Z、M的原子序數依次增大,它們組成一種團簇分子,結構如圖所示。X、M的族序數均等于周期序數,Y原子核外最外層電子數是其電子總數的,下列說法正確的是( )34
4.短周期元素X、Y、Z、M的原子序數依次增大,它們組成一種團簇分子,結構如圖所示。X、M的族序數均等于周期序數,Y原子核外最外層電子數是其電子總數的,下列說法正確的是( )34A.簡單離子半徑:Z>M>Y B.第一電離能:Y>M>Z C.工業上常用電解熔融物ZY制取Z單質 D.Z、M的簡單離子均可促進水的電離 組卷:34引用:2難度:0.5 -
5.無法達到相應實驗目的的是( )
A. 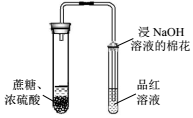
探究濃硫酸的脫水性和氧化性B. 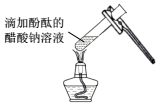
探究溫度對水解程度的影響C. 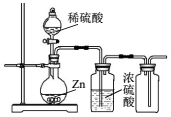
制備干燥的氫氣D. 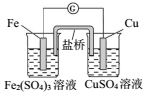
驗證Cu與Fe3+反應產生電流組卷:29引用:4難度:0.5 -
6.藥物異博定(鹽酸維拉帕米)能有效控制血壓升高、促進血液循環,其合成路線中有如圖轉化過程:

已知NaH晶體屬NaCl晶型,則下列說法正確的是( )A.X的沸點低于其同分異構體 
B.Y分子中基態Br原子電子排布式為[Ar]4s24p5 C.1mol Z最多與6mol H2發生加成反應 D.NaH晶體中,與Na+最近的H-有12個 組卷:13引用:1難度:0.6
三、非選擇題(本題共5小題,共60分)
-
19.2-氨基-3-氯苯甲酸(F)是重要的醫藥中間體,其制備流程圖如圖:

已知:
回答下列問題:
(1)B的名稱為。寫出符合下列條件B的所有同分異構體的結構簡式。
a.苯環上只有兩個取代基且互為鄰位;
b.既能發生銀鏡反應又能發生水解反應
(2)該流程未采用甲苯直接硝化的方法制備B,而是經由①②③三步反應制取B,其目的是。
(3)寫出⑥的化學反應方程式:,該步反應的主要目的。
(4)寫出⑧的反應試劑和條件:;F中含氧官能團的名稱為。
(5)設計以 為主要原料,經最少步驟合成含酰胺鍵聚合物的合成路線 。組卷:34引用:2難度:0.6
為主要原料,經最少步驟合成含酰胺鍵聚合物的合成路線 。組卷:34引用:2難度:0.6 -
20.已知磺酰氯(SO2Cl2)是一種無色液體,熔點-54.1℃,沸點69.1℃,遇水發生劇烈水解,且產生白霧。某學習小組依據SO2(g)+Cl2(g)?SO2Cl2(g)ΔH<0,利用下列裝置制備磺酰氯(部分夾持裝置略)。

(1)利用E裝置制取SO2宜選用的試劑是。
a.10%的硫酸溶液和亞硫酸鈣固體
b.銅和98%的濃硫酸
c.80%的硫酸溶液和亞硫酸鈉固體
d.80%的硫酸溶液和亞硫酸鈣固體
(2)為了使Cl2和SO2在D中混合反應,用儀器接口的小寫字母和箭頭表示上述裝置的合理連接順序:→f,g←。(箭頭方向要與氣流方向一致,部分裝置可重復使用)
(3)儀器甲的名稱為,儀器乙的作用是。
(4)制備時,D中的三頸燒瓶宜浸入冰水浴中的原因是。
(5)測定產品中SO2Cl2的含量:取1.5g產品加入足量Ba(OH)2溶液,振蕩、過濾、洗滌,將過濾液和洗滌液均放入錐形瓶中。向錐形瓶中加入硝酸,再加入0.2000mol?L-1的AgNO3溶液100.00mL,搖勻;向其中加入2mL硝基苯,用力搖動;然后滴入幾滴NH4Fe(SO4)2溶液,用0.1000mol?L-1NH4SCN溶液滴定過量Ag+,終點所用體積為20.00mL。[已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12]
①硝基苯的作用是。
②產品中SO2Cl2的質量分數為,若其他操作均正確,滴定終點仰視讀數所測SO2Cl2含量將。(填“偏高”、“偏低”或“無影響”)組卷:52引用:2難度:0.4


