2023-2024學年廣東省東莞市東華高級中學、東華松山湖高級中學高一(上)聯考化學試卷(10月份)
發布:2024/9/11 7:0:8
一、單項選擇題(共16小題,1-10每題3分;11-16每題4分;共54分)
-
1.“古詩文經典已融入中華民族的血脈”。下列詩文中隱含化學變化的是( )
A.月落烏啼霜滿天,江楓漁火對愁眠 B.掬月水在手,弄花香滿衣 C.飛流直下三千尺,疑是銀河落九天 D.忽聞海上有仙山,山在虛無縹緲間 組卷:6引用:1難度:0.8 -
2.下列說法正確的是( )
A.因為Na失電子能力強,所以其還原性強 B.因為Al失電子數目多,所以其還原性強 C.Ca2+既有氧化性又有還原性 D.Fe2+只有氧化性 組卷:12引用:4難度:0.7 -
3.能用H++OH-═H2O來表示的化學反應是( )
A.Ba(OH)2溶液與稀硫酸反應 B.澄清石灰水和HNO3溶液反應 C.KOH溶液和醋酸溶液反應 D.稀氨水和H2SO4溶液反應 組卷:49引用:1難度:0.8 -
4.下列敘述正確的是( )
A.向氫氧化鈉溶液中邊滴加飽和FeCl3溶液邊振蕩制備Fe(OH)3膠體 B.分散系中分散質粒子直徑由小到大的正確順序是:溶液<膠體<濁液 C.膠體中加入電解質會發生的聚沉現象,證明膠體帶電 D.膠體區別于其他分散系的本質原因是膠體有丁達爾效應 組卷:4引用:2難度:0.8 -
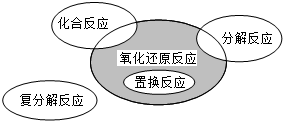 5.氧化還原反應與四種基本類型反應的關系如圖所示,則下列化學反應屬于陰影部分的是( )
5.氧化還原反應與四種基本類型反應的關系如圖所示,則下列化學反應屬于陰影部分的是( )A.Cl2+2KBr═Br2+2KCl B.2NaHCO3 Na2CO3+H2O+CO2↑△C.4Fe(OH)2+O2+2H2O═4Fe(OH)3 D.2Na2O2+2CO2═2Na2CO3+O2↑ 組卷:224引用:63難度:0.7 -
6.下列敘述正確的是( )
A.石墨能導電,所以石墨是電解質 B.SO3的水溶液能導電,所以SO3是電解質 C.NH4Cl的水溶液能導電,所以NH4Cl是電解質 D.固體氯化鋇不能導電,所以氯化鋇不是電解質 組卷:26引用:1難度:0.5 -
7.在能使石蕊變紅的無色透明溶液中,能大量共存的離子組是( )
A.Ba2+、K+、OH-、Cl- B.Fe2+、Na+、 、NO-3SO2-4C.Ca2+、K+、 、Cl-HCO-3D.Mg2+、 、NH+4、Cl-SO2-4組卷:18引用:1難度:0.6
二、非選擇題(共46分)
-
20.某溶液的溶質只可能由下列離子中的幾種組成:Cl-、
、CO2-3、H+、Ba2-、Na+,某同學進行了如下實驗:SO2-4
①向溶液中加入過量的BaCl2溶液,有白色沉淀生成,過濾;
②向①中濾液加入AgNO3溶液,有白色沉淀產生:
③將①的沉淀加入稀鹽酸中,沉淀部分消失,有氣體生成。
依據以上實驗可以推斷:
(1)原溶液中一定含有;一定沒有。
(2)②中生成的沉淀是;③中反應的離子方程式是。
(3)寫出NaHSO4在水溶液中的電離方程式:。
(4)書寫離子方程式
①氫氧化鐵和鹽酸反應;
②向澄清石灰水中通入過量二氧化碳;
③寫出BaCO3固體與足量的NaHSO4溶液反應的離子方程式:。組卷:59引用:1難度:0.5 -
21.亞硝酸鈉(NaNO2)是一種工業鹽,外觀與食鹽非常相似,但毒性較強,食品中添加亞硝酸鈉必須嚴格控制用量。某化學興趣小組設計實驗探究NaNO2的性質。
(1)已知NaNO2能發生如下反應:2NaNO2+4HI═2NO+I2+2NaI+2H2O。用雙線橋標出該反應的電子轉移方向和數目:。
(2)NaNO2(填“是”或“不是”)電解質,根據NaNO2中N的化合價推測NaNO2具有(填“氧化性”、“還原性”或“氧化性和還原性”)。
(3)實驗操作如表所示,請完善表格中的實驗現象和結論(已知I2遇淀粉變藍)。
?③通過上述實驗可知,NaNO2、KMnO4、I2的氧化性由強到弱的順序為實驗 實驗操作及現象或結果 結論 1 取5mL NaNO2溶液于試管中,加入少量KI溶液,充分反應后,再滴加淀粉溶液,溶液變藍 NaNO2具有① 2 取2mL KMnO4溶液(先酸化好)于試管中,滴加足量NaNO2溶液,可觀察到的實驗現象為② NaNO2具有還原性 3 NaNO2固體于70%硫酸反應生成NO和NO2兩種氣體 NaNO2具有氧化性和還原性 。
(4)亞硝酸鈉外觀與食鹽相似,且均有咸味。
①若誤食亞硝酸鈉會導致血紅蛋白中亞鐵離子轉化為鐵離子而中毒,服用維生素C可解除亞硝酸鈉的中毒,下列關于上述中毒。解毒過程的說法中,正確的是。
A.亞硝酸鈉是還原劑
B.維生素C是氧化劑
C.維生素C能把鐵離子還原成為亞鐵離子
D.亞硝酸鈉被還原
②X與亞硝酸鈉發生的反應可表示為2NaNO2+2X+2H2SO4═2NO↑+I2+K2SO4+Na2SO4+2H2O(已配平),其中X是(填化學式),每生成1個I2,轉移個電子。組卷:22引用:1難度:0.4


