2020年北京市昌平區高考化學二模試卷
發布:2024/11/1 17:30:3
一、選擇題本部分共14題,每題3分,共42分.在每題列出的四個選項中,選出最符合題目要求的一項.
-
1.從石油原料到口罩的生產過程中涉及的下列變化不屬于化學變化的是( )
A B C D 



石油催化裂化得到丙烯 丙烯催化聚合生成聚丙烯 聚丙烯熔融后噴絲壓成熔噴布 利用環氧乙烷與微生物蛋白質發生烷基化反應消毒 A.A B.B C.C D.D 組卷:101引用:9難度:0.7 -
2.下列化學用語表述不正確的是( )
A.電解CuCl2溶液:Cu2++2Cl- Cu+Cl2↑電解B.NaCl的形成過程: 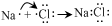
C.HCl在水中電離:HCl═H++Cl- D.NH4Cl在水中發生水解:NH4++H2O?NH3?H2O+H+ 組卷:25引用:1難度:0.5 -
3.下列敘述不正確的是( )
A.蛋白質在酶的作用下能水解成氨基酸,被人體吸收 B.纖維素是天然高分子化合物,在一定條件下能發生水解 C.淀粉可以在酒化酶的作用下轉化成乙醇,用于釀酒 D.牛油主要由不飽和脂肪酸甘油酯組成,熔點較低 組卷:62引用:1難度:0.8 -
4.下列說法不正確的是( )
A.苯和甲苯都能使酸性KMnO4溶液褪色 B.飽和溴水滴入苯酚的稀溶液中,生成白色沉淀 C.乙醛與新制Cu(OH)2懸濁液共熱能生成磚紅色沉淀 D.乙酸能與NaHCO3溶液反應生成無色氣體 組卷:26引用:2難度:0.6 -
5.潛艇中氧氣來源之一的反應是:2Na2O2+2H2O═4NaOH+O2↑.用NA表示阿伏加德羅常數,下列說法正確的是( )
A.22.4L O2含2NA個O原子 B.1.8g H2O含有的質子數為NA C.1mol Na2O2含共價鍵的總數為2NA D.上述反應,每生成1mol O2轉移4mol電子 組卷:52引用:1難度:0.6 -
6.下列變化與氧化還原反應無關的是( )
A.向FeCl3溶液中滴加KSCN溶液,溶液變紅 B.金屬鈉投入水中,有氣體產生 C.將盛有氯氣的試管倒扣在水中,水位上移 D.向H2S溶液中通入SO2氣體,產生淡黃色沉淀 組卷:49引用:1難度:0.8
第二部分本部分共5題,共58分.
-
18.他米巴羅汀(Ⅰ)可用于治療急性白血病,其合成研究具有重要意義,合成路線如圖所示。
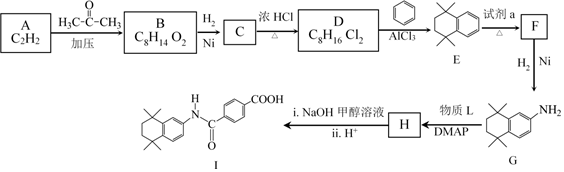
已知:
ⅰ.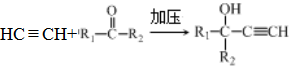
ⅱ.R-NO2R-NH2H2Ni
ⅲ.
(1)A中官能團名稱是。
(2)B的結構簡式是。
(3)D→E的化學方程式是。
(4)試劑a是。
(5)已知H在合成Ⅰ的同時,還生成甲醇,G→H所加物質L的結構簡式是。
(6)B的一種同分異構體符合下列條件,其結構簡式是。
①能發生銀鏡反應
②核磁共振氫譜只有兩組吸收峰
(7)D→E的過程中有多種副產物,其中屬于高分子化合物的結構簡式是。
(8)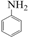 也是合成他米巴羅汀(Ⅰ)的一種原料,合成路線如圖所示。利用題中所給信息,中間產物的結構簡式是。
也是合成他米巴羅汀(Ⅰ)的一種原料,合成路線如圖所示。利用題中所給信息,中間產物的結構簡式是。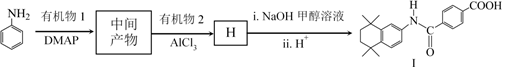 組卷:74引用:3難度:0.3
組卷:74引用:3難度:0.3 -
19.實驗小組制備NaNO2,并探究其性質。
Ⅰ.制備NaNO2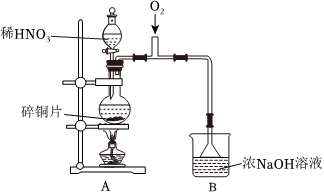
(1)A中發生反應的化學方程式是。
(2)B中選用漏斗替代長直導管的優點是。
(3)為檢驗B中制得NaNO2,甲進行以下實驗:
實驗③的目的是序號 試管 操作 現象 ① 2mL B中溶液 加2mL 0.1mol/L KI溶液,滴加幾滴淀粉溶液 不變藍 ② 2mL B中溶液 滴加幾滴H2SO4至pH=5,加2mL 0.1mol/L KI溶液,滴加幾滴淀粉溶液 變藍 ③ 2mL H2O 滴加幾滴H2SO4至pH=5,加2mL 0.1mol/L KI溶液,滴加幾滴淀粉溶液 不變藍 。
(4)乙認為上述3組實驗無法證明B中一定含NaNO2,還需補充實驗,理由是。
Ⅱ.探究NaNO2的性質
資料:裝置 操作 現象 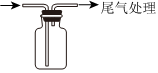
取10mL 1mol/L NaNO2溶液于試劑瓶中,加入幾滴H2SO4酸化,再加入10mL 1mol/L FeSO4溶液,迅速塞上橡膠塞,緩緩通入足量O2. ⅰ.溶液迅速變為棕色。
ⅱ.溶液逐漸變淺,有無色氣泡產生,溶液上方為淺紅棕色。
ⅲ.最終形成棕褐色溶液。
ⅰ.[Fe(NO)]2+在溶液中呈棕色。
ⅱ.HNO2在溶液中不穩定,易分解產生NO和NO2氣體。
(5)溶液迅速變為棕色的原因是。
(6)已知棕色溶液變淺是由于生成了Fe3+,反應的離子方程式是。
(7)最終棕褐色溶液的成分是Fe(OH)x(SO4)y,測得裝置中混合溶液體積為20mL,設計如下實驗測定其組成。
資料:充分反應后,Fe2+全部轉化為Fe(OH)x(SO4)y.Fe(OH)x(SO4)y中x=(用含V1、V2的代數式表示)。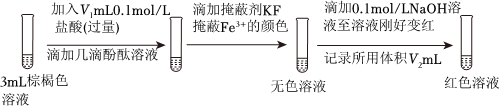 組卷:66引用:3難度:0.4
組卷:66引用:3難度:0.4


