2021-2022學(xué)年北京四中順義分校高二(上)期中化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、第一部分(選擇題共42分)每小題只有一個選項(xiàng)符合題意(每小題2分)
-
1.下列設(shè)備工作時,將化學(xué)能轉(zhuǎn)化為熱能的是( )
A B C D 



硅太陽能電池 鋰離子電池 太陽能集熱器 燃?xì)庠?/td> A.A B.B C.C D.D 組卷:900引用:106難度:0.9 -
2.下列物質(zhì)屬于弱電解質(zhì)的是( )
A.NaOH B.NH3?H2O C.NaCl D.H2SO4 組卷:10引用:1難度:0.6 -
3.下列物質(zhì)的水溶液呈酸性的是( )
A.NH4Cl B.NaCl C.CH3COONa D.Na2CO3 組卷:21引用:2難度:0.8 -
4.在1L的密閉容器中進(jìn)行反應(yīng)A(g)+3B(g)?2C(g),0~2min內(nèi)A的物質(zhì)的量由2mol減小到0.8mol,則用A的濃度變化表示的反應(yīng)速率[mol/(L?min)]為( )
A.1.2 B.1 C.0.6 D.0.4 組卷:311引用:5難度:0.8 -
 5.已知:2SO2(g)+O2(g)?2SO3(g)△H,不同條件下反應(yīng)過程能量變化如圖所示。下列說法中不正確的是( )
5.已知:2SO2(g)+O2(g)?2SO3(g)△H,不同條件下反應(yīng)過程能量變化如圖所示。下列說法中不正確的是( )A.反應(yīng)的△H<0 B.過程b使用了催化劑 C.使用催化劑可以提高SO2的平衡轉(zhuǎn)化率 D.過程b發(fā)生兩步反應(yīng),第一步為吸熱反應(yīng) 組卷:262引用:21難度:0.6 -
6.硫代硫酸鈉溶液與稀硫酸反應(yīng)的化學(xué)方程式為:Na2S2O3+H2SO4═Na2SO4+SO2+S↓+H2O,下列各組實(shí)驗(yàn)中最先出現(xiàn)渾濁的是( )
實(shí)驗(yàn) 反應(yīng)溫度/℃ Na2S2O3溶液 稀H2SO4 V/mL c/mol?L-1 V/mL c/mol?L-1 A 25 5 0.1 10 0.1 B 25 5 0.2 10 0.2 C 35 5 0.1 10 0.1 D 35 5 0.2 10 0.2 A.A B.B C.C D.D 組卷:22引用:8難度:0.5 -
7.下列溶液肯定顯酸性的是( )
A.c(H+)>c(OH-)的溶液 B.含H+的溶液 C.pH<7的溶液 D.加酚酞顯無色的溶液 組卷:102引用:11難度:0.6 -
8.氫氣可通過下列反應(yīng)制得:CO(g)+H2O(g)
CO2(g)+H2(g)△H<0,為了提高氫氣在平衡體系中所占的比例,可采取的措施是( )催化劑A.減小壓強(qiáng) B.降低溫度 C.更換催化劑 D.減小CO的濃度 組卷:23引用:7難度:0.7
二、第二部分(非選擇題共58分)
-
25.氨在國民經(jīng)濟(jì)中占有重要地位。合成氨工業(yè)中,合成塔中每產(chǎn)生2mol NH3,放出92.2 kJ熱量。
(1)工業(yè)合成氨的熱化學(xué)方程式是。
(2)已知:
1molN-H鍵斷裂吸收的能量約等于kJ。
(3)T℃時,在有催化劑的恒容密閉容器中充入N2和H2。圖1為不同投料比[]時某反應(yīng)物X的平衡轉(zhuǎn)化率變化曲線。n(H2)n(N2)
①反應(yīng)物X是(填“N2”或“H2”)。
②判斷依據(jù)是。
(4)在其他條件相同時,圖2為分別測定不同壓強(qiáng)、不同溫度下,N2的平衡轉(zhuǎn)化率。L表示,其中X1X2(填“>”或“<”)。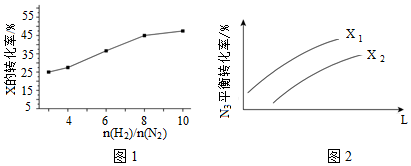 組卷:9引用:2難度:0.7
組卷:9引用:2難度:0.7 -
26.某興趣小組以重鉻酸鉀(K2Cr2O7)溶液為研究對象,結(jié)合所學(xué)反應(yīng)原理的知識改變條件使其發(fā)生“色彩變幻”。
已知:①K2Cr2O7溶液存在平衡:Cr2+H2O?2O2-7+2H+。CrO2-4
②含鉻元素的離子在溶液中的顏色:Cr2(橙色);O2-7(黃色);Cr3+(綠色)。CrO2-4
(1)i可證明反應(yīng)Cr2+H2O?2O2-7+2H+的正反應(yīng)是CrO2-4(填“吸熱”或“放熱”)。
(2)ii是驗(yàn)證“只降低生成物的濃度,該平衡正向移動”,試劑a是。
(3)iii的目的是要驗(yàn)證“增大生成物的濃度,該平衡逆向移動”,此實(shí)驗(yàn)是否能達(dá)到預(yù)期目的(填“能”或“不能”),理由是。
(4)根據(jù)實(shí)驗(yàn)Ⅱ中不同現(xiàn)象,可以得出的結(jié)論是。
(5)繼續(xù)實(shí)驗(yàn)
①解釋溶液變黃的主要原因是。
②溶液變綠色,該反應(yīng)的離子方程式是。組卷:236引用:6難度:0.1


