2021-2022學(xué)年安徽省六安市金安區(qū)皖西中學(xué)高二(上)期末化學(xué)試卷
發(fā)布:2024/12/3 0:0:2
一、選擇題:本題共16小題,每小題3分,共48分。在每小題給出的四個選項(xiàng)中,只有一項(xiàng)是符合題目要求的。
-
1.下列說法正確的是( )
A.燃燒熱和中和熱都屬于反應(yīng)熱的一種 B.酸和堿發(fā)生中和反應(yīng)生成1 mol水,這時(shí)的反應(yīng)熱叫中和熱 C.在101 kPa時(shí),1 mol物質(zhì)完全燃燒時(shí)所放出的熱量,叫做該物質(zhì)的燃燒熱 D.在稀溶液中,1 mol CH3COOH和1 mol NaOH完全中和時(shí)放出的熱量為57.3 kJ 組卷:117引用:3難度:0.8 -
2.氧化亞銅常用于制船底防污漆,用CuO與Cu高溫?zé)Y(jié)可制取Cu2O.已知反應(yīng):
2Cu(s)+O2(g)═2CuO(s)ΔH=-314kJ?mol-1
2Cu2O(s)+O2(g)═4CuO(s)ΔH=-292kJ?mol-1
則CuO(s)+Cu(s)═Cu2O(s)的ΔH等于( )A.-11kJ?mol-1 B.+11kJ?mol-1 C.+22kJ?mol-1 D.-22kJ?mol-1 組卷:1186引用:15難度:0.9 -
3.在四個不同的密閉容器中,采用不同條件進(jìn)行反應(yīng)N2(g)+3H2(g)?2NH3(g),根據(jù)下列在相同時(shí)間內(nèi)測定的結(jié)果判斷,生成氨的速率最快的是( )
A.v(N2)=0.2mol/(L?min) B.v(NH3)=0.3mol/(L?min) C.v(H2)=0.1mol/(L?min) D.v(H2)=0.3mol/(L?min) 組卷:83引用:4難度:0.5 -
4.下列體系加壓后,對化學(xué)反應(yīng)速率沒有影響的是( )
A.2SO2+O2?2SO3 B.CO+H20(氣)?CO2+H2 C.CO2+H2O?H2CO3 D.NaOH+HCl=NaCl+H20 組卷:11引用:1難度:0.9 -
5.反應(yīng)N2(g)+3H2(g)?2NH3(g)△H<0,若在恒壓絕熱容器中發(fā)生,下列選項(xiàng)表明反應(yīng)一定已達(dá)平衡狀態(tài)的是( )
A.容器內(nèi)的溫度不再變化 B.容器內(nèi)的壓強(qiáng)不再變化 C.相同時(shí)間內(nèi),斷開H-H鍵的數(shù)目和生成N-H鍵的數(shù)目相等 D.容器內(nèi)氣體的濃度c(N2):c(H2):c(NH3)=1:3:2 組卷:257引用:34難度:0.5 -
6.已知反應(yīng)CO(g)+H2O(g)
CO2(g)+H2(g)ΔH<0。在一定溫度和壓強(qiáng)下于密閉容器中,反應(yīng)達(dá)到平衡。下列敘述正確的是( )催化劑A.升高溫度,K增大 B.減小壓強(qiáng),n(CO2)增加 C.更換高效催化劑,n(CO)增大 D.充入一定量的氮?dú)猓琻(H2)不變 組卷:8引用:2難度:0.6 -
7.相同溫度下,關(guān)于鹽酸和醋酸兩種溶液的比較,下列說法正確的是( )
A.pH相等的兩溶液中:c(CH3COO-)=c(Cl-) B.分別中和pH相等、體積相等的兩溶液,所需NaOH的物質(zhì)的量相同 C.相同濃度的兩溶液,分別與金屬鎂反應(yīng),反應(yīng)速率相同 D.相同濃度的兩溶液,分別與NaOH固體反應(yīng)后呈中性的溶液中(忽略溶液體積變化):c(CH3COO-)=c(Cl-) 組卷:586引用:11難度:0.7
二、非選擇題:共52分。
-
 20.回答下列有關(guān)水溶液的問題:
20.回答下列有關(guān)水溶液的問題:
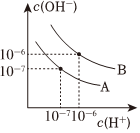
(1)已知在25℃和95℃時(shí),水的電離平衡曲線如圖所示:
①在25℃時(shí),水的電離平衡曲線應(yīng)為(填“A”或“B”);95℃時(shí)水的離子積Kw=。
②25℃時(shí),0.1mol?L-1HNO3中c(OH-)=mol?L-1;將0.1mol?L-1NaOH溶液從25℃升高到95℃,不考慮水的蒸發(fā),溶液的pH如何變化?(填“增大”、“不變”或“減小”)。
(2)Mg(OH)2固體能溶于較濃的NH4Cl溶液,對其原因的分析主要有兩種觀點(diǎn):
①水解使溶液顯酸性,可以溶解Mg(OH)2;NH+4
②與Mg(OH)2電離生成的OH-結(jié)合,使Mg(OH)2?Mg2++2OH-的平衡右移,Mg(OH)2不斷溶解。NH+4
已知Ka(CH3COOH)=Kb(NH3?H2O),設(shè)計(jì)實(shí)驗(yàn)探究哪種觀點(diǎn)正確:。組卷:11引用:1難度:0.7 -
21.圖甲燒杯中盛有稀硫酸,乙燒杯中盛有CuCl2溶液,a、b均為石墨電極,G是靈敏電流計(jì)。回答下列問題:
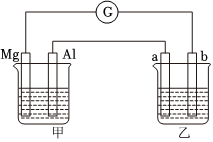
(1)甲裝置是池,Al電極的電極反應(yīng)式為。
(2)乙裝置是池,其總反應(yīng)式為。
(3)工作一段時(shí)間后,甲裝置中某極質(zhì)量減少2.4g。同一時(shí)間內(nèi),乙裝置中某極產(chǎn)生的氣體在標(biāo)準(zhǔn)狀況下的體積為L(假定CuCl2溶液足量)。
(4)若將甲中溶液換成NaOH溶液,則負(fù)極反應(yīng)式為。組卷:2引用:1難度:0.7


