2021-2022學年新疆昌吉州高一(上)期末化學試卷
發布:2024/12/16 15:0:2
一、單選題(25*2=50分,每道題只有一個正確選項)
-
1.下列物質的分類正確的是( )
堿 酸 堿性氧化物 混合物 A Na2CO3 H2SO4 MgO 氯水 B Ba(OH)2 HClO Na2O Fe(OH)3膠體 C NaOH CH3COOH Fe3O4 膽礬 D KOH NaHSO4 CaO 不銹鋼 A.A B.B C.C D.D 組卷:8引用:1難度:0.8 -
2.下列各組物質的轉化中,必須加入還原劑才能完成的是( )
A.Cu→CuSO4 B.Fe2O3→Fe C.KClO3→KCl D.Na2CO3→CO2 組卷:4引用:2難度:0.7 -
3.下列關于膠體的敘述正確的是( )
A.膠體和溶液的本質區別是膠體可以產生丁達爾效應 B.將飽和FeCl3溶液滴入NaOH溶液中可制備氫氧化鐵膠體 C.可以用濾紙分離提純膠體和溶液 D.明礬凈水與膠體的性質有關 組卷:9引用:2難度:0.7 -
4.下列說法正確的是( )
A.CO2溶于水能導電,所以CO2是電解質 B.銅絲能導電,所以銅是電解質 C.熔融的CaCl2能導電,所以CaCl2是電解質 D.氯化氫水溶液能導電,所以鹽酸是電解質 組卷:11引用:1難度:0.8 -
5.某無色透明的溶液中,能大量共存的離子組是( )
A.Na+、Cu2+、SO42-、OH- B.K+、Ba2+、Cl-、NO3- C.K+、Fe2+、Cl-、MnO4- D.Na+、CO32-、SO42-、H+ 組卷:58引用:3難度:0.6 -
6.判斷下列離子方程式書寫錯誤的是( )
A.碳酸氫鈉溶液與硝酸反應:HCO3-+H+=H2O+CO2↑ B.石灰石溶于鹽酸中:CaCO3+2H+=Ca2++CO2↑+H2O C.硫酸溶液與氫氧化鋇溶液混合:Ba2++SO42-=BaSO4↓ D.氧化鐵與稀硫酸反應:Fe2O3+6H+=2Fe3++3H2O 組卷:19引用:3難度:0.7 -
7.下列反應中,氯氣既作氧化劑又作還原劑的是( )
A.3Cl2+2Fe 2FeCl3點燃B.MnO2+4HCl(濃) Cl2↑+MnCl2+2H2O△C.Cl2+2KOH=KCl+KClO+H2O D.3Cl2+8NH3=N2+6NH4Cl 組卷:15引用:3難度:0.8 -
8.下列有關鈉及其化合物的說法正確的是( )
A.Na2O2能與酸反應生成鹽和水,所以Na2O2是堿性氧化物 B.Na、Na2O和Na2O2長時間放在空氣中,最終都會變成Na2CO3 C.將足量的Na2O2、Na2O分別加到酚酞試液中,最終溶液均為紅色 D.“84”消毒液和潔廁靈(主要成分為鹽酸)一起使用,消毒效果會更好 組卷:30引用:2難度:0.6 -
9.下列關于氯元素的單質及其化合物的說法不正確的是( )
A.漂白粉的有效成分是Ca(ClO)2,應密封保存 B.氯水溶液呈淺黃綠色,且有刺激性氣味,說明有Cl2分子存在 C.向新制的氯水中滴入紫色石蕊試液,溶液將先變紅后褪色 D.氯氣有漂白性,所以氯氣能使濕潤的有色布條褪色 組卷:39引用:1難度:0.7 -
10.下列說法正確的是( )
A.16gO2和O3混合氣體中所含的氧原子的物質的量為1mol B.常溫常壓下,1molCl2的質量是71g/mol C.36gH2O的物質的量為1mol D.16g氧氣中含有的氧原子數為2NA個 組卷:20引用:1難度:0.5
二、填空題(共5道大題,50分)
-
30.利用如圖所示裝置以二氧化錳和濃鹽酸為主要原料制取氯氣。
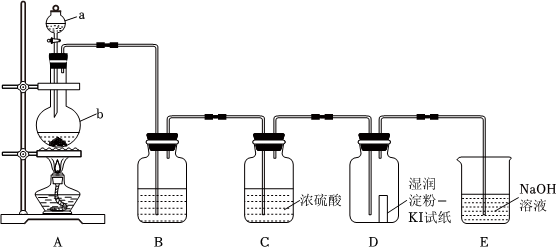
(1)請指出儀器a的名稱,寫出裝置b中發生反應的離子方程式:。
(2)裝置B中的試劑是,裝置C是否必需(填“是”或者“否”)。
(3)裝置D中的現象是。
(4)用上述氯氣制取如圖1的84消毒液,離子反應方程式。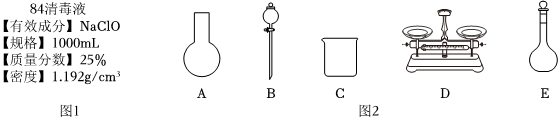
(5)該“84消毒液”中NaClO的物質的量濃度為mol?L-1。
(6)該同學欲用NaClO固體配制480mL含NaClO質量分數為25%的消毒液。如圖2所示的儀器中,還缺少的是(填儀器名稱)。
(7)下列操作會導致所配溶液的物質的量濃度偏高的是。
A.使用容量瓶配制溶液時,俯視液面定容后所得溶液的濃度
B.使用容量瓶配制溶液時,仰視液面定容后所得溶液的濃度
C.定容時,滴加蒸餾水,液面略高于刻度線,再吸出少量水使液面凹面與刻度線相切
D.用蒸餾水洗滌燒杯2~3次,未將洗液移入容量瓶中
E.用蒸餾水溶解NaClO固體后,立即轉入容量瓶中定容組卷:30引用:1難度:0.7 -
31.為探究鐵和鐵的化合物的一些化學性質,某學生實驗小組設計以下實驗。
(1)如圖:
①Fe2O3和HCl的離子方程式是。
②B→C變化中可看到的現象是,發生氧化還原反應的化學方程式是。
(2)某班同學用如下實驗探究Fe2+、Fe3+的性質。回答下列問題:
①分別取一定量氯化鐵、氯化亞鐵固體,均配制成100mL0.1mol/L的溶液。在配制FeCl2溶液時需加入少量鐵屑,其目的是。
②某同學取2mLFeCl2溶液,加入幾滴氯水,再加入1滴KSCN溶液,溶液變紅,說明Cl2可將Fe2+氧化。FeCl2溶液與氯水反應的離子方程式為。
(3)某實驗小組探究氯水與鐵的反應。(實驗過程)操作過程及實驗現象如圖所示。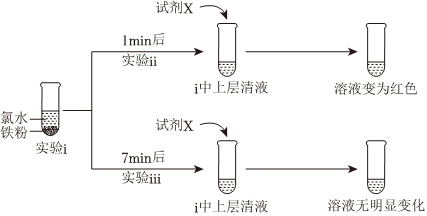
①實驗i中產生少量無色氣體,該氣體可能是。
②實驗ii中觀察到溶液變為紅色,可推知上層清液中含有Fe3+,則試劑X是(填字母)。
a.KSCN溶液
b.NaCl溶液
③實驗iii中觀察到溶液無明顯變化,可推知上層清液中不含Fe3+,其原因是(用離子方程式表示)。
④甲同學認為上層清液中的Fe3+是由Cl2與Fe2+反應生成。乙同學認為還有其他可能性,請寫出其中一種:。組卷:12引用:1難度:0.6


