2022-2023學年上海市復興高中高二(上)質檢化學試卷(10月份)
發布:2024/4/20 14:35:0
一、選擇題(共10分,每小題2分,每小題只有一個正確答案)
-
1.下列有關濃硫酸的說法正確的是( )
A.與碳的反應體現了濃硫酸的強酸性 B.常溫時不與鋁發生化學反應,可用鋁制容器盛裝濃硫酸 C.可以用來干燥二氧化硫 D.使蔗糖變黑體現了濃硫酸的強氧化性 組卷:47引用:1難度:0.7 -
2.有4種短周期主族元素X、Y、Z和Q的原子序數依次增大,相關信息如表:
下列說法正確的是( )元素 相關信息 X 最外層電子數等于次外層電子數 Y 與X在同一主族 Z 單質為淡黃色固體,常存在于火山噴口附近 Q 同周期主族元素中原子半徑最小 A.X的金屬性比Y強 B.Y的離子半徑是同周期中最小的 C.Q的氣態氫化物比Z的氣態氫化物定 D.Q的含氧酸是最強酸 組卷:18引用:1難度:0.6 -
3.向物質的量濃度均為1mol?L-1的AlCl3和鹽酸的混合溶液中逐滴滴入NaOH溶液,如圖中[n表示Al(OH)3的物質的量、V表示NaOH溶液的體積]能正確表示這個反應過程的是( )
A. 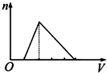
B. 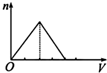
C. 
D. 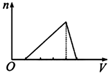 組卷:403引用:12難度:0.9
組卷:403引用:12難度:0.9
二、綜合題(共90分)
-
10.碳酸亞鐵(FeCO3)是生產補血劑的重要原料,制取碳酸亞鐵的過程中涉及以下探究實驗。
實驗一:
為探究某固體化合物X(僅含有三種元素)的組成和性質,設計并完成如圖實驗。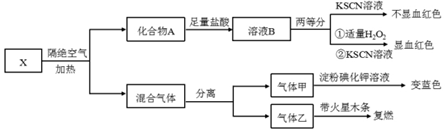
已知:氣體甲、氣體乙均為單質。
請回答:
(1)氣體甲與碘化鉀溶液反應的離子方程式為。
(2)化合物X含有的元素為(寫元素符號)。
(3)化合物A的化學式為。
實驗二:
如圖裝置,利用實驗一所得溶液B制取FeCO3(白色固體,難溶于水):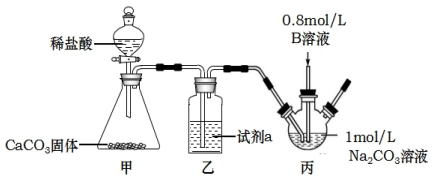
裝置丙中,先向Na2CO3溶液(pH=11.9)通入一段時間CO2至其pH為7,再滴加一定量B溶液產生白色沉淀和無色氣體(離子方程式為Fe2++2HCO3-═FeCO3↓+CO2↑+H2O),過濾、洗滌、干燥,得到FeCO3固體。
請回答:
(4)乙裝置中的試劑a是,作用是。
(5)向Na2CO3溶液通入的CO2目的是。
(6)不可用酸性高錳酸鉀溶液檢驗溶液B中的金屬陽離子的原因是:。
(7)100mL0.8mol/LB溶液完全反應,最終得到5.568gFeCO3固體,則產率為。組卷:16引用:1難度:0.3 -
11.實驗小組用兩種不同的方法測定已部分變質的亞硫酸鈉樣品的純度。
方案一:實驗流程如圖1。
(1)簡述檢驗亞硫酸鈉樣品已經變質的方法。
(2)操作Ⅱ的名稱是;整個實驗過程中需要用到的儀器主要有燒杯、玻璃棒、干燥器、酒精燈、石棉網、、(固定、夾持儀器除外)。
(3)能證明冷卻后稱量的質量已達恒重的依據是。
方案二:如圖2,Y管左側裝亞硫酸鈉樣品,右側裝較濃硫酸,相互接觸即可反應產生SO2,通過測定SO2體積來測定樣品中Na2SO3含量。
(4)如圖2,加入試劑之前須進行的操作是;反應不用稀硫酸原因。為減小實驗誤差,量氣管中液體M可用。
(5)若樣品的質量為ag,加入10mL較濃硫酸充分反應后,測得排出液體的體積為VL(標準狀況下),則樣品中Na2SO3的質量分數的計算式為。
(6)若實驗結果測得該樣品中Na2SO3含量偏低,原因可能是(選填編號)。
a.硫酸不足量
b.測定氣體體積時未冷卻至室溫
c.Y型管中留有反應生成的氣體
d.測定氣體體積時水準管的液面高于量氣管的液面組卷:5引用:1難度:0.5


