新人教版九年級下冊《第11章 鹽 化肥》2021年單元測試卷(江蘇省無錫市江陰市南閘中學)
發布:2024/4/20 14:35:0
一、選擇題(本題包括14小題,每小題只有1個選項符合題意。每小題1分,共14分)
-
1.下列物質的名稱、俗名與化學式完全對應的是( )
A.氯化鈉、食鹽、NaCl2 B.碳酸氫鈉、小蘇打、NaHCO3 C.氧化鈣、熟石灰、CaO D.氫氧化鈉、純堿、NaOH 組卷:38引用:3難度:0.9 -
2.下列物質溶解于水時,溶液的溫度無明顯變化的是( )
A.濃硫酸 B.氫氧化鈉固體 C.氧化鈣固體 D.硝酸鉀晶體 組卷:97引用:15難度:0.9 -
3.鹽酸、稀硫酸在水溶液中都能產生H+,故有許多共同的性質。下列有關敘述正確的是( )
A.打開盛有濃鹽酸和濃硫酸的試劑瓶瓶塞,在瓶口都有白霧 B.稀鹽酸和稀硫酸都可用于除鐵銹 C.濃鹽酸、濃硫酸都可用來干燥氧氣 D.在稀鹽酸、稀硫酸中滴加氯化鋇溶液,都有白色沉淀 組卷:110引用:4難度:0.6 -
4.為提高染發劑染色效果,一般先用堿劑等對頭發預處理.某堿劑在染發時可聞到刺激性氣味,該氣體能使濕潤的紅色石蕊試紙變藍.則該氣體為( )
A.CO2 B.O2 C.NH3 D.H2 組卷:145引用:21難度:0.9 -
5.物質存放在燒杯中一段時間后,質量變大且變質的是( )
①濃鹽酸 ②濃硫酸 ③燒堿 ④食鹽 ⑤生石灰 ⑥稀硫酸。A.①⑥ B.②③⑤ C.③⑤ D.②③④ 組卷:681引用:212難度:0.7 -
6.下列家庭小實驗不能成功的是( )
A.用食品級的檸檬酸和小蘇打自制汽水 B.用10%的氫氧化鈉溶液浸泡樹葉制“葉脈書簽” C.用食鹽水浸泡菜刀除去表面的鐵銹 D.用紫包菜的酒精浸出液試驗食醋的酸性 組卷:72引用:4難度:0.5
二、非選擇題(共5小題,滿分36分)
-
19.FeCl3可用作催化劑和外傷止血劑。某實驗興趣小組利用FeCl3腐蝕電路銅板后的溶液(主要成分為FeCl2、CuCl2)進行了氯化鐵回收實驗。
該實驗小組同學通過查閱資料,進行了嘗試。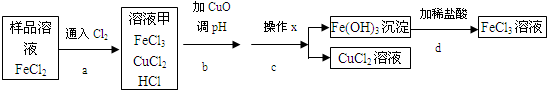
【閱讀資料】
不同金屬氫氧化物可以在不同的pH范圍內從溶液中沉淀析出,工業上利用調節溶液pH的方法,使金屬氫氧化物依次沉淀,結合過濾等操作,進行物質分離。下表是氫氧化鐵與氫氧化銅開始沉淀與沉淀完全的pH。
(1)進行操作x時,應用到的儀器有:鐵架臺、玻璃棒、燒杯和Fe(OH)3 Cu(OH)2 開始沉淀的pH 1.9 4.7 沉淀完全的pH 3.2 6.7 。
(2)實驗中,步驟b加入CuO消耗溶液甲中的HCl,使溶液pH增大到所需范圍,請寫出鹽酸與氧化銅反應的化學方程式;你認為步驟b調節溶液的pH到(填數值范圍)比較合適。
(3)實驗中,步驟d加稀鹽酸前,因缺少(填操作名稱)而使獲得的氯化鐵溶液不純。
(4)FeCl3溶液容易生成Fe(OH)3發生變質,在保存FeCl3溶液時,常向FeCl3溶液中加入某種酸,以防止FeCl3溶液變質,你認為選用(用字母表示)最合理。
A.稀硝酸 B.稀硫酸 C.稀鹽酸 D.稀醋酸。組卷:74引用:5難度:0.5 -
20.目前全世界的鎳(Ni)消費量僅次于銅、鋁、鉛、鋅,居有色金屬第五位。鎳常用于各種高光澤裝飾漆和塑料生產,也常用作催化劑。
Ⅰ.【鎳粉制備】:
工業用電解鎳新液(主要含NiSO4、NiCl2等)制備堿式碳酸鎳晶體[xNiCO3?yNi(OH)2?zH2O],并利用其制備鎳粉的流程如圖1: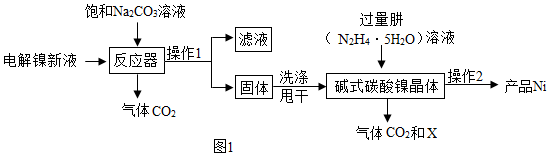
(1)制備鎳粉的流程圖中,氣體X是空氣中含量最多的氣體,該氣體是。反應器中的一個重要反應為3NiSO4+3Na2CO3+2Y═NiCO3?2Ni(OH)2↓+3Na2SO4+2CO2↑,Y的化學式為。
(2)物料在反應器中反應時需要控制反應條件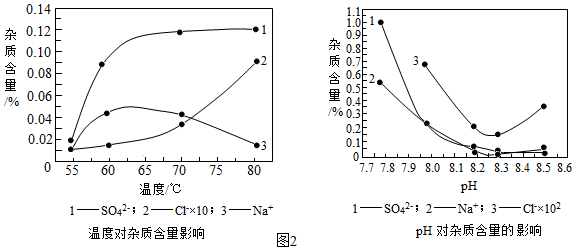
分析圖2,反應器中最適合的溫度及pH分別為℃、8.3。
(3)生產中,pH逐漸增加,生成Ni(OH)2含量也相對增加,則生成的堿式碳酸鎳晶體中,鎳的含量將(填“升高”、“降低”或“不變”)。
(4)操作2包括過濾、水洗、95%酒精浸泡、晾干等操作。其中在晾干之前使用95%酒精浸泡的目的是。
Ⅱ.【測定堿式碳酸鎳晶體的組成】:
為測定堿式碳酸鎳晶體[xNiCO3?yNi(OH)2?zH2O]組成,某小組設計了如圖3實驗方案及裝置: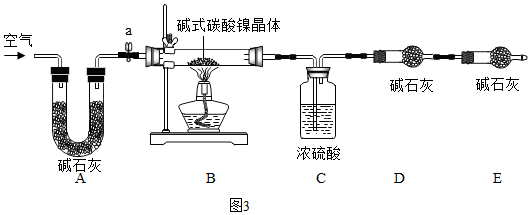
【資料卡片】
①堿式碳酸鎳晶體受熱會完全分解生成NiO固體、CO2和H2O(水蒸氣)。
②堿石灰是NaOH和CaO的混合物,可以吸收CO2和H2O。
【實驗步驟】
①檢查裝置氣密性;
②準確稱取7.54g堿式碳酸鎳晶體[xNiCO3?yNi(OH)2?zH2O]放在B裝置中,連接儀器;
③打開彈簧夾a,鼓入一段時間空氣,分別稱量裝置C、D、E的質量;
④關閉彈簧夾a,加熱裝置B至裝置C中導管末端無氣泡冒出;
⑤打開彈簧夾a,緩緩鼓入一段時間空氣;
⑥分別準確稱量裝置C、D、E的質量;
⑦根據數據進行計算(相關數據如下表)。
【實驗分析及數據處理】裝置C/g 裝置D/g 裝置E/g 加熱前 250.00 190.00 190.00 加熱后 252.16 190.88 190.00
(5)裝置A的作用是。實驗過程中步驟⑤鼓入空氣的目的是。
(6)根據7.54g堿式碳酸鎳晶體[xNiCO3?yNi(OH)2?zH2O]完全分解所得的數據,通過計算堿式碳酸鎳晶體中含有鎳元素的質量為g。(寫出計算過程)
【實驗反思】
(7)另一小組同學加熱時在酒精燈上加了鐵絲網罩,實驗結束后,稱得裝置B中殘留固體質量明顯偏大。經查閱資料發現:在溫度控制不當導致溫度過高時,NiO會部分被氧化成Ni2O3。該組同學稱得的殘留固體混合物的質量可能是。
A.4.5g
B.4.6g
C.4.98g
D.5.2g組卷:68引用:1難度:0.5


