2018-2019學年山東省威海市環翠區八年級(下)期末化學試卷(五四學制)
發布:2024/4/20 14:35:0
一、選擇題(本題共15小題,每小題只有一個選項符合題意)
-
1.下列各選項的能量轉化過程中,主要發生化學變化的是( )
①太陽能供熱
②電水壺燒水
③火力發電
④電熱器取暖
⑤火藥爆炸A.③⑤ B.③④ C.②③⑤ D.①② 組卷:3引用:1難度:0.5 -
2.規范操作是實驗成功的保證,如圖所示實驗操作正確的是( )
A. 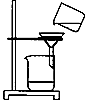
過濾B. 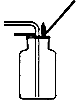
驗滿二氧化碳C. 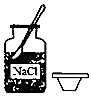
取固體D. 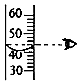
讀取液體體積組卷:3引用:1難度:0.7 -
3.分類是一種重要的學習方法,下列不同物質的微觀粒子示意圖中,分類正確的是( )

A.屬于混合物的是:②③④ B.屬于純凈物的是①②④⑤ C.由單質組成的純凈物的是①②⑤ D.屬于化合物的是:④ 組卷:12引用:1難度:0.8 -
4.下列對分子、原子、離子的認識正確的是( )
A.同種分子排列方式不同,化學性質不同 B.水結冰后,分子因相互作用而靜止不動 C.原子得失電子形成離子后,原子核發生了變化 D.同種原子按不同方式結合,可以構成不同的物質 組卷:5引用:1難度:0.7 -
5.下列關于元素的說法正確的是( )
A.同種元素的原子化學性質相同,但質量可能不同 B.世界萬物都是由元素組成的,地殼中含量最多的金屬元素是鐵 C.人造元素是通過化學方法合成的 D.元素的種類是由質子數和中子數共同決定的 組卷:16引用:1難度:0.7 -
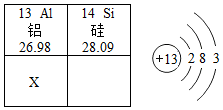 6.元素周期表為預測新元素的結構和性質提供了線索,如圖是元素周期表的部分內容和鋁原子結構示意圖,下列說法不正確的是( )
6.元素周期表為預測新元素的結構和性質提供了線索,如圖是元素周期表的部分內容和鋁原子結構示意圖,下列說法不正確的是( )A.X元素原子在化學反應中易失去電子變成X3+ B.表中數據28.09是一個硅原子的質量與一個碳12原子質量的比值 C.X元素原子與鋁原子有相似的化學性質 D.X元素應該位于元素周期表第四周期 組卷:4引用:1難度:0.5
二、填空與簡答題(包括4個小題)
-
19.認識氨氣。
材料:①氨氣是無色有強烈的刺激性氣味的氣體;②密度比空氣小;③降溫至-33.5℃可變為液態;④1體積水大約溶解700體積氨氣;⑤在高溫條件下分解生成氮氣和氫氣;⑥與氯化氫氣體混合產生白煙(成分為氯化銨);⑦用于制液氮、氨水、硝酸、銨鹽和胺類等。⑧工業上用氮氣和氫氣在高溫高壓催化劑作用下合成氨氣;⑨實驗室可用加熱氯化銨(NH4Cl)和熟石灰【Ca(OH)2】兩種固體的方法制取氨氣,并且生成氯化鈣和水。
(1)氨氣的組成與結構
根據上述材料⑤,可以確定氨氣是由(填符號)元素組成的,理由是:。已知氨氣的相對分子質量為17,它所生成的氮氣與氫氣的質量比為14:3,寫出氨氣的化學式并標注氮元素的化合價(負價元素在左)。
(2)氨氣的性質
閱讀上文,歸納氨氣的化學性質(兩條)。
(3)氨氣的變化
Ⅰ.請分別寫出工業和實驗室制取氨氣的化學方程式:、。
Ⅱ.變化③中不發生變化的是(填字母編號)。
a.氨分子的能量
b.氨分子的運動速率
c.氨分子的質量
d.氨分子之間的間隔
e.氨分子的化學性質
f.氨分子之間的相互作用
g.氨分子的構成
Ⅲ.描述變化⑤的微觀過程。
(4)氨氣的制備
Ⅰ.工業制氨氣所用催化劑可重復使用,其原因是。
Ⅱ.實驗室制取氨氣應選取的發生裝置是(填裝置編號),選擇此裝置的理由是,可以用法收集,理由是,若選擇如圖裝置D進行收集,應從(填“a”或“b”)處進入。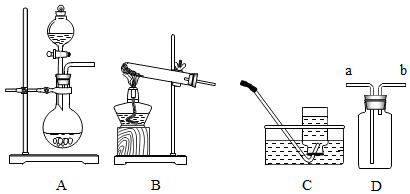
(5)氨氣的化學性質再探究
將氨氣通入紫色石蕊試液,石蕊試液變藍。
提出問題:哪種物質使紫色石蕊試液變藍?
猜想1:氨氣;
猜想2:水;
猜想3:。
設計實驗方案:
實驗用品:純凈的氨氣、蒸餾水、干燥的紫色石蕊試紙(若干)
請選擇上述用品進行方案設計,將實驗方案以及現象填寫在下表中,儀器自選。實驗方案 實驗現象 實驗結論 猜想3正確 組卷:9引用:1難度:0.5
三、計算題
-
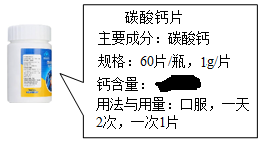 20.測定碳酸鈣片中的鈣含量。
20.測定碳酸鈣片中的鈣含量。
為測定一標簽破損(如圖)的碳酸鈣片中鈣的含量,某同學進行了如下實驗:
①稱量燒杯的質量為20g,在燒杯中放入5片鈣片;
②稱取50g稀鹽酸,用膠頭滴管取稀鹽酸逐滴滴到燒杯中,至不再有氣泡放出,稱量剩余稀鹽酸的質量為17g;
③反應后,燒杯及燒杯內剩余物質的總質量為56.35g。(碳酸鈣片中其他成分不和稀鹽酸反應,反應中產生的氣體全部放出)
試通過上述實驗數據計算,若按說明書服用,則每天通過服用碳酸鈣片攝入鈣的質量為多少克?組卷:6引用:1難度:0.4


