2022年福建省廈門市高考化學第二次質檢試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共10小題,每小題4分,共40分。每小題只有一個選項符合題目要求。
-
1.我國明代《余東錄》記載“鉛塊懸酒缸內,封閉四十九日,開之則化為粉矣。化不白者,炒為黃丹。”涉及物質轉化如下:Pb
(CH3COO)2Pbi2Pb(OH)2?PbCO3iiPbO。下列有關說法錯誤的是( )iiiA.Pb屬于電解質 B.2Pb(OH)2?PbCO3屬于堿式鹽 C.反應ⅰ中(CH3COO)2Pb為氧化產物 D.反應ⅲ為分解反應 組卷:39引用:1難度:0.5 -
 2.北京冬奧會“冰墩墩”“雪容融”成為頂流,由PVC、PC、ABS和亞克力等環保材料制作而成。下列說法錯誤的是( )
2.北京冬奧會“冰墩墩”“雪容融”成為頂流,由PVC、PC、ABS和亞克力等環保材料制作而成。下列說法錯誤的是( )A.PVC( 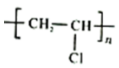 )的單體為氯乙烯
)的單體為氯乙烯B.PC( 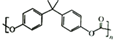 )中所有碳原子均可共面
)中所有碳原子均可共面C.ABS的單體之一苯乙烯能使溴水褪色 D.亞克力( 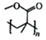 )可通過加聚反應制備組卷:83引用:12難度:0.7
)可通過加聚反應制備組卷:83引用:12難度:0.7 -
3.為探究增氧劑過氧碳酸鈉(2Na2CO3?3H2O2)的性質,向以下溶液中分別滴加少量過氧碳酸鈉溶液,既有沉淀又有氣體生成的是( )
A.H2SO4 B.NaClO C.KI D.FeCl3 組卷:41引用:1難度:0.8 -
4.下列有關海水綜合利用的離子方程式不正確的是( )
A.海水提鎂中用石灰乳沉鎂:Mg2++2OH-=Mg(OH)2↓ B.海水提溴中用SO2水溶液富集溴:SO2+Br2+2H2O=4H++SO42-+2Br- C.氯堿工業中電解飽和食鹽水:2Cl-+2H2O Cl2↑+2OH-+H2↑通電D.侯氏制堿法中獲取碳酸氫鈉:Na++CO2+NH3+H2O=NaHCO3↓+NH4+ 組卷:66引用:4難度:0.6 -
5.設NA為阿伏加德羅常數的值。由電化學固氮得到的AlN轉化為NH3的反應為:AlN+NaOH+3H2O=Na[Al(OH)4]+NH3↑,下列說法不正確的是( )
A.固氮過程中,每生成1molAlN轉移的電子數目為3NA B.室溫下,pH為13的NaOH溶液中OH-數目為0.1NA C.標準狀況下,1.12LNH3中含有的電子數目為0.5NA D.11.8gNa[Al(OH)4]中含有的共價鍵數目為0.8NA 組卷:27引用:2難度:0.6
二、非選擇題:本題共5小題,共60分。
-
14.為探究新制Cu(OH)2和甲醛的反應,進行如下實驗。
(1)由上述實驗可知,新制Cu(OH)2會發生如下轉化:新制Cu(OH)2實驗序號 6mol?L-1NaOH溶液體積/mL 0.5mol?L-1CuSO4溶液體積/mL 14mol?L-1甲醛溶液體積/mL 反應條件 實驗現象 1 12 8 6 65℃水浴加熱13min 溶液中出現磚紅色固體,逐漸變為紅色蓬松固體并產生氣泡,共收集83mL氣體。 2 12 1 6 溶液中出現磚紅色固體,逐漸變為暗紅色顆粒并產生氣泡,共收集13mL氣體。 3 12 2 0.1 溶液中出現磚紅色固體,且無氣泡產生。 甲醛△Cu,說明反應物的相對用量會影響固體產物。甲醛△
(2)為確認氣體產物進行實驗,裝置如圖1。
①NaOH溶液作用是。
②氣體產物含H2,不含CO的證據是。
(3)為進一步確認H2產生的原因,查閱資料并進行實驗:2HCHO+NaOHCH3OH+HCOONa;CH3OH△HCHO+H2↑。Cu
①實驗說明催化劑的催化性能與實驗序號 6mol?L-1NaOH溶液體積/mL 14mol?L-1甲醛溶液體積/mL 甲醇/mL 其他試劑 反應條件 生成氣體體積/mL 4 12 0 6 銅粉 65℃水浴加熱13min 0 5 12 0 6 Cu2O粉 0 6 12 6 0 Cu2O粉 70 有關(填“物質形態”或“溶液pH”)。
②實驗2中產生氣體體積小于實驗1的原因可能為。
(4)已知C-O鍵鍵長為0.142nm,C=O鍵鍵長為0.120nm,請結合HCOO-中碳氧鍵鍵長數據如圖2,分析HCOONa無法進一步被新制Cu(OH)2氧化成Na2CO3的原因。
(5)新制Cu(OH)2和過量甲醛反應的化學方程式為。組卷:21引用:1難度:0.5 -
15.有機物K是合成酪氨酸血癥藥物尼替西農的中間體,其合成路線如圖:
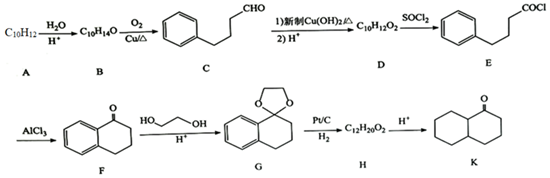
(1)A中官能團的名稱為。
(2)B→C的反應方程式為。
(3)D→E的反應類型。
(4)H的結構簡式為。
(5)M(C9H10O2)是D的同系物,其核磁共振氫譜峰面積之比為6:2:1:1。M的結構簡式為(寫出一種即可)。
(6)以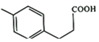 為原料合成
為原料合成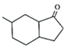 試寫出合成路線(無機試劑任選) 。組卷:24引用:1難度:0.5
試寫出合成路線(無機試劑任選) 。組卷:24引用:1難度:0.5


