2021-2022學(xué)年天津市塘沽一中高三(上)第一次月考化學(xué)試卷
發(fā)布:2024/12/11 23:0:1
一.本卷共12題,每題3分,共36分。
-
1.電視紀(jì)錄片《輝煌中國》讓“厲害了,我的國”成了人們的口頭禪,其展示的我國在科技領(lǐng)域取得的許多偉大成就都與化學(xué)密切相關(guān)。下列有關(guān)說法錯誤的是( )
A.“蛟龍”號載人潛水器的外殼使用的耐超高壓的鈦合金,屬于金屬材料 B.“中國天眼”FAST傳輸信息用的光導(dǎo)纖維的主要成分是硅酸鹽 C.高鐵“復(fù)興號”車廂連接關(guān)鍵部位使用的增強(qiáng)聚四氟乙烯板屬于高分子材料 D.港珠澳大橋水下鋼柱鑲鋁塊防腐的方法為“犧牲陽極的陰極保護(hù)法” 組卷:18引用:1難度:0.6 -
2.下列化學(xué)用語表述正確的是( )
A.核內(nèi)質(zhì)子數(shù)為117,核內(nèi)中子數(shù)為174的核素Ts可表示為: TS174117B.乙醇的結(jié)構(gòu)簡式:C2H6O C.COCl2 的結(jié)構(gòu)式為: 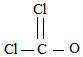
D.CaO2的電子式為: 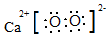 組卷:752引用:9難度:0.9
組卷:752引用:9難度:0.9 -
3.下列物質(zhì)的性質(zhì)與用途具有對應(yīng)關(guān)系的是( )
A.NH4Cl溶液呈酸性,可用于除鐵銹 B.NaHCO3受熱易分解,可用于治療胃酸過多 C.Fe(OH)3膠體有吸附性,可用于殺菌消毒 D.Na2SO3溶液呈堿性,可用于污水脫氯(Cl2) 組卷:15引用:1難度:0.7 -
4.下圖所示的實(shí)驗(yàn)或操作中,能達(dá)到實(shí)驗(yàn)?zāi)康牡氖牵ā 。?br />
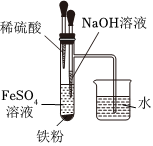
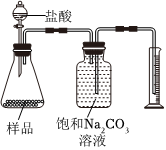
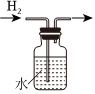
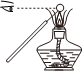
制備氫氧化亞鐵 測定純堿樣品中碳酸鈉的質(zhì)量分?jǐn)?shù)(雜質(zhì)不與酸作用) 排水法收集H2 鉀的焰色試驗(yàn) A B C D A.A B.B C.C D.D 組卷:22引用:6難度:0.5 -
5.實(shí)驗(yàn)室從碘的四氯化碳溶液中分離單質(zhì)碘的主要步驟為:用濃NaOH溶液進(jìn)行反萃取、分液、酸化、過濾及干燥等。下列說法正確的是( )
A.反萃取時I2與NaOH溶液反應(yīng)的離子方程式:I2+2OH-═I-+IO3-+H2O B.反萃取時倒轉(zhuǎn)振蕩過程中要適時旋開活塞放氣 C.分液時,先放出有機(jī)相,然后從下口放出水相 D.酸化后過濾時,用玻璃棒攪拌可加快單質(zhì)碘從酸化后的體系分離 組卷:82引用:2難度:0.3
二、解答題(共4小題,滿分0分)
-
15.具有抗菌、消炎作用的黃酮醋酸類化合物L(fēng)的合成路線如圖所示:
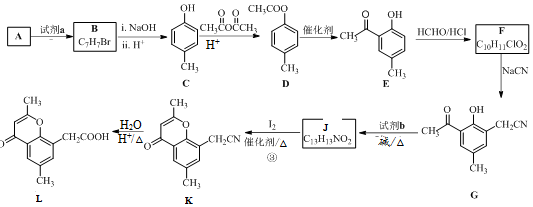
已知部分有機(jī)化合物轉(zhuǎn)化的反應(yīng)式如下:
i.R-X+NaCN→R-CNR-COOH (R為烴基)H+
ii.RCHO+CH3COR′RCH=CHCOR′(R、R′代表烴基或氫)堿△
iii.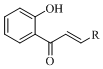 I2催化劑/加熱
I2催化劑/加熱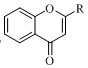 (R、R′代表烴基或氫)
(R、R′代表烴基或氫)
(1)A的分子式是C7H8,其結(jié)構(gòu)簡式是;A→B所屬的反應(yīng)類型為。
(2)C→D的化學(xué)方程式是。
(3)寫出滿足下列條件的D的任意一種同分異構(gòu)體的結(jié)構(gòu)簡式:。
a.能發(fā)生銀鏡反應(yīng)
b.分子中含有酯基
c.苯環(huán)上有兩個取代基,且苯環(huán)上的一氯代物有兩種
(4)F的結(jié)構(gòu)簡式是;試劑b是。
(5)J與I2反應(yīng)生成K和HI的化學(xué)方程式是。
(6)以A和乙烯為起始原料,結(jié)合題中信息,選用必要的無機(jī)試劑合成苯乙酸乙酯(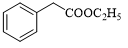 ),參照下列模板寫出相應(yīng)的合成路線。
),參照下列模板寫出相應(yīng)的合成路線。 組卷:35引用:2難度:0.4
組卷:35引用:2難度:0.4 -
16.高鐵酸鉀(K2FeO4)是一種新型、高效、多功能綠色水處理劑,已知:
①NaClO在較高溫度下發(fā)生歧化反應(yīng)生成NaClO3。
②K2FeO4具有下列性質(zhì):可溶于水、微溶于濃KOH溶液;在強(qiáng)堿性溶液中比較穩(wěn)定;在Fe3+催化作用下發(fā)生分解,在酸性至弱堿性條件下,能與水反應(yīng)生成Fe(OH)3和O2實(shí)驗(yàn)室以次氯酸鹽和鐵鹽為原料制備少量K2FeO4的操作步驟如下:
Ⅰ.制備NaClO強(qiáng)堿性飽和溶液:
①將20mL NaOH溶液加入儀器b中,冷水浴冷卻,通入Cl2,攪拌,直至溶液變?yōu)辄S綠色且有少量白色晶體析出為止(裝置如圖所示)。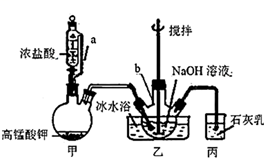
②將所得飽和NaClO倒入燒杯并置于冷水浴中,分幾次加入20g NaOH固體并不斷攪拌,過濾,得NaClO強(qiáng)堿性飽和溶液。
(1)甲裝置中a管的作用是。
(2)寫出甲裝置中反應(yīng)的化學(xué)方程式。
(3)石灰乳的作用是。
(4)反應(yīng)過程中用冷水浴冷卻的原因是。
Ⅱ.合成K2FeO4:
①稱取5.05g Fe(NO3)3?9H2O(相對分子質(zhì)量為404)固體,在冷水浴中分批加入Ⅰ中所得濾液,并不斷攪拌,反應(yīng)1小時后溶液呈深紫紅色(即Na2FeO4)。
②離心分離除去Na2FeO4水解得到的Fe(OH)3膠體,留上層清液(深紫紅色)。
③向②的上層清液中緩慢加入KOH飽和溶液50.00mL,冰水浴保持5min,過濾,得K2FeO4[M(K2FeO4)=198g/mol]粗產(chǎn)品。
④將粗產(chǎn)品重結(jié)晶,并洗滌,低溫烘干,得純產(chǎn)品2.13g。
(5)工業(yè)上常用廢鐵屑為原料制備Fe(NO3)3溶液,檢驗(yàn)Fe3+所需試劑名稱,其反應(yīng)原理為(用離子方程式表示);合成Na2FeO4的離子方程式為。
(6)過程③加入飽和KOH溶液即可得到K2FeO4粗產(chǎn)品,析出K2FeO4固體,過濾、洗滌、干燥。洗滌操作所用最佳試劑為。
A.水
B.無水乙醇
C.稀KOH溶液
(7)K2FeO4的產(chǎn)率為(保留至0.1%)。組卷:35引用:1難度:0.6


