2018-2019學年北京166中高三(上)期中化學試卷
發布:2024/4/20 14:35:0
一.選擇題
-
1.下列敘述正確的是( )
A.NaOH可用于治療胃酸過多 B.CaO可防止月餅等食品氧化變質 C.氫彈中用到的2H、3H互為同位素 D.向海水中加入凈水劑明礬可以使海水淡化 組卷:100引用:2難度:0.9 -
2.下列比較中正確的是( )
A.金屬性:Mg>Al>Na B.原子半徑:S>O>F C.堿性:KOH>Mg(OH)2>NaOH D.氫化物穩定性:HBr>HCl>PH3 組卷:104引用:13難度:0.9 -
3.下列各組離子因發生氧化還原反應而不能大量共存的是( )
A.H+、Fe2+、Cr2 、O2-7SO2-4B.Ca2+、H+、 、SO2-4HCO-3C.Na+、Cu2+、Cl-、S2- D.Fe3+、K+、SCN-、Cl- 組卷:440引用:10難度:0.7 -
4.下列說法正確的是( )
A.1molC7H16中含有23 mol共價鍵 B.標準狀況下,1.12LNH3中含有0.5mol e- C.常溫常壓下,22gCO2中所含分子物質的量是0.5mol D.40gNaOH溶于1L水,所得溶液中c(Na+)=1mol/L 組卷:19引用:2難度:0.7 -
5.下列反應所得溶液中一定只含一種溶質的是( )
A.向NaOH溶液中通入CO2 B.向Ca(OH)2溶液中通入Cl2 C.向蒸餾水中加入少量金屬Na D.向Al2(SO4)3溶液中滴入Ba(OH)2溶液 組卷:28引用:7難度:0.7 -
6.下列說法正確的是( )
A.c(H+)>c(OH-)的溶液一定顯酸性 B.常溫下,pH=6的溶液一定是酸溶液 C.電解稀硫酸或氫氧化鈉溶液的產物不同 D.水電解生成氫氣和氧氣,證明水是弱電解質 組卷:8引用:3難度:0.7 -
7.《常用危險化學用品貯存通則》規定:“遇火、遇熱、遇潮能引起燃燒、爆炸或發生化學反應,產生有毒氣體的化學危險品不得在露天或在潮濕、積水的建筑物中貯存”。下列解釋事實的方程式中,不合理的是( )
A.貯存液氮的鋼瓶防止陽光直射:N2+O2 2NO陽光B.硝酸銨遇熱爆炸:2NH4NO3 2N2↑+O2↑+4H2O↑△C.干燥的 AlCl3遇水產生氣體:AlCl3+3H2O═Al(OH)3+3HCl↑ D.火災現場存有電石,禁用水滅火:CaC2+2H2O→Ca(OH)2+C2H2↑ 組卷:166引用:5難度:0.5 -
8.Na2CO3俗稱純堿,是基本化工原料.下列涉及Na2CO3的方程式中,正確的是( )
A.Na2O2與CO2反應生成Na2CO3:Na2O2+CO2═Na2CO3+O2 B.Na2CO3溶液呈堿性:CO32-+H2O?H2CO3+OH- C.Na2CO3溶液除去CH3COOC2H5中的CH3COOH:CO32-+2H+═CO2↑+H2O D.飽和Na2CO3溶液處理水垢中的CaSO4:CO32-+CaSO4═CaCO3+SO42- 組卷:71引用:5難度:0.9
二、第Ⅱ部分(非選擇題共60分)
-
24.已知:①工業上用硫酸與β-鋰輝礦(LiAlSi2O6和少量鈣鎂雜質)反應,生成Li2SO4、MgSO4等,最終制備金屬鋰.
②氫氧化鋰在一定溫度下可轉化為氧化鋰.
用硫酸與β-鋰輝礦生產金屬鋰的工業流程如下: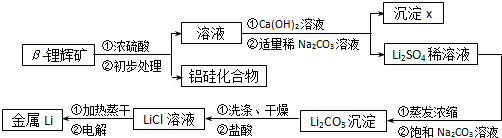
請回答:
(1)β-鋰輝礦經初步處理后從溶液中分離出鋁硅化合物沉淀的操作是.
(2)沉淀x的主要成分的化學式是.
(3)流程中使用了不同濃度的Na2CO3溶液,從物質溶解度大小的角度解釋其濃度不同的原因是.
(4)由Li2CO3與鹽酸反應得到LiCl溶液的離子方程式是.
(5)LiCl溶液加熱蒸干后,所得固體在熔融狀態下進行電解生產鋰.電解時產生的氯氣中混有少量氧氣,產生氧氣的原因是.組卷:26引用:2難度:0.3 -
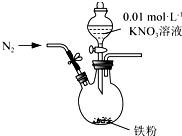 25.某同學看到“利用零價鐵還原NO3-脫除地下水中硝酸鹽”的相關資料后,利用如下裝置探究鐵粉與KNO3溶液的反應.實驗過程如下:
25.某同學看到“利用零價鐵還原NO3-脫除地下水中硝酸鹽”的相關資料后,利用如下裝置探究鐵粉與KNO3溶液的反應.實驗過程如下:
i.打開彈簧夾,緩慢通入N2,并保持后續反應均在N2氛圍中進行;
ii.加入pH 已調至2.5 的 0.01mol?L-1KNO3酸性溶液100mL,一段時間后鐵粉部分溶解,
溶液逐漸變為淺綠色;待鐵粉不再溶解,靜置后發現,剩余固體表面有少量白色物
質附著;
iii.過濾剩余固體時,表面的白色物質變為紅褐色;
iv.檢測到濾液中存在NO3-、NH4+和Fe2+.
(1)通入N2并保持后續反應均在N2 氛圍中進行的實驗目的是.
(2)白色物質是,用化學方程式解釋其變為紅褐色的原因:.
(3)用K3[Fe(CN)6]檢驗濾液中Fe2+的實驗方案是.
(4)取少量濾液,向其中加入幾滴KSCN 溶液,無明顯現象;再加入幾滴稀硫酸,溶液呈紅色.溶液變成紅色的原因是.
(5)該同學進一步查閱資料發現,用鐵粉、碳粉的混合物脫除硝酸鹽,效果更佳.他用上述KNO3溶液繼續設計如下實驗,探究碳粉的作用
③關于碳粉的作用,還可以提出的假設是假設 實驗操作 現象及結論 假設1:碳粉可用作還原劑,脫除硝酸鹽 向燒杯中加入 一段時間后,測定燒杯中NO3-的濃度NO3-濃度無明顯變化,說明假設不成立 假設2:碳粉、鐵粉形成無數個微小的原電池,促進了硝酸鹽的脫除 按下圖所示組裝實驗裝置,一段時間后,測定NO3-濃度 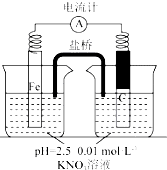
,說明假設2成立.組卷:67引用:3難度:0.5


