2014-2015學(xué)年河北省石家莊市正定一中高三(上)周測化學(xué)試卷(2)
發(fā)布:2024/12/6 22:0:2
一.選擇題(每小題6分)
-
1.設(shè)NA為阿伏加德羅常數(shù),則下列說法中正確的是( )
A.2 mol的NO2與水完全反應(yīng)轉(zhuǎn)移電子數(shù)為2NA B.39 g Na2O2晶體中所含陰陽離子個數(shù)均為2NA C.3.4 g氨中含有0.6NA個N-H鍵 D.在pH=13的NaOH溶液中,OH-數(shù)目為0.1NA 組卷:5引用:2難度:0.5 -
2.下列各組離子在指定條件下,一定能大量共存的是( )
A.pH為1的無色溶液:K+、Fe2+、 、Cl-SO2-3B.能使碘化鉀淀粉試紙變藍的溶液:Na+、 、S2-、Br-NH+4C.水電離出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、 、Cl-NO-3D.加入鋁條有氫氣放出的溶液:Na+、 、NH+4、HCO-3SO2-4組卷:211引用:11難度:0.9 -
3.下列說法正確的是( )
A.強電解質(zhì)溶液的導(dǎo)電能力一定比弱電解質(zhì)溶液的導(dǎo)電能力強 B.因為CH3COOH是弱電解質(zhì),HCl是強電解質(zhì),所以中和等體積、等物質(zhì)的量濃度的醋酸和鹽酸時,中和醋酸消耗的NaOH比中和鹽酸消耗的NaOH的量少 C.足量Zn分別與等體積、等物質(zhì)的量濃度的鹽酸和醋酸反應(yīng)時,產(chǎn)生H2的量相同,放出H2的速率不同 D.在物質(zhì)的量濃度相同的磷酸鈉溶液和磷酸溶液中 的物質(zhì)的量濃度相同PO3-4組卷:174引用:4難度:0.9
二.非選擇題
-
10.在一個2L的密閉容器中,投入反應(yīng)物,發(fā)生反應(yīng)2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的變化如圖所示:

(1)寫出該反應(yīng)的平衡常數(shù)表達式并根據(jù)8min時到達平衡計算出結(jié)果.
(2)用O2表示0到8min內(nèi)該反應(yīng)的平均速率v=.
(3)能說明該反應(yīng)已達到平衡狀態(tài)的是.
A.v(SO3)=2v(O2) B.容器內(nèi)壓強保持不變
C.v(SO2)逆=2v(O2)正 D.容器內(nèi)密度保持不變
(4)在第12min時,容器壓縮到1L,則SO3的變化曲線為.
A.a(chǎn) B.b C.c D.d
(5)若保持容積不變在第12min時,加入SO3(g),則平衡向反應(yīng)方向移動(填“正”或“逆”).SO3的體積分?jǐn)?shù)(填“增大”或“減小”).組卷:25引用:4難度:0.5 -
11.過氧化鈣(CaO2)難溶于水,在常溫下穩(wěn)定,在潮濕空氣及水中緩慢分解放出氧氣,因而廣泛應(yīng)用于漁業(yè)、農(nóng)業(yè)、環(huán)保等許多方面。如圖是以大理石(主要雜質(zhì)是氧化鋁)等為原料制取過氧化鈣(CaO2)的流程。
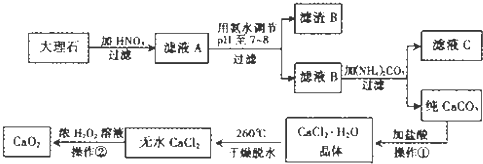
請回答下列問題:
(1)①中實驗操作順序為(填序號)。
a.過濾 b.蒸餾 C.分液 d.蒸發(fā)結(jié)晶
(2)用氨水調(diào)節(jié)pH至7~8的目的是。
(3)寫出生成濾渣B的離子方程式。
(4)若在濾液C中,加入HN,使溶液呈酸性以得到副產(chǎn)物NH4NO3,則酸化后溶液中,c()NH+4c()(填“≥”、“≤”、“<”、“>”或“=”)NO-3
(5)操作②是在低溫下,往過氧化氫濃溶液中投入無水氯化鈣進行反應(yīng),寫出該反應(yīng)的化學(xué)方程式。一段時間后,再加入氫氧化鈉溶液,調(diào)節(jié)溶液的pH至9~11,現(xiàn)大量沉淀。用簡要的文字解釋需用氫氧化鈉調(diào)節(jié)pH至9~11的原因。組卷:3引用:1難度:0.5


