2016-2017學年江蘇省常州市鐘樓實驗中學九年級(下)周末化學作業(5.28)
發布:2024/4/20 14:35:0
一、選擇題(共5小題,每小題3分,滿分15分)
-
1.已知:膽礬晶體呈藍色,其所帶結晶水很容易失去而呈白色.在下圖的實驗裝置中,實驗開始一段時間后,觀察到的現象不正確的是( )

A.蘋果塊會干癟 B.膽礬晶體表面有“白斑” C.小試管內有晶體析出 D.pH試紙只會變紅不會變黑 組卷:70引用:4難度:0.9 -
2.加熱條件下,將24g CuO、Fe2O3的混合物與充足的CO完全反應,并將反應后的氣體全部通入到澄清石灰水中,得到白色沉淀40g.下列有關敘述中不正確的是( )
A.原混合物中CuO與Fe2O3物質的量的比為1:1 B.反應后所得CO2的質量為40g C.參加反應的CO的質量為11.2g D.原混合物中CuO與Fe2O3的質量比為1:2 組卷:101引用:3難度:0.5 -
3.為比較Fe3+和Cu2+對H2O2分解反應的催化效果,甲、乙兩組同學分別設計了如圖1、圖2所示的實驗.下列敘述中不正確的是( )

A.圖1實驗可通過觀察產生氣泡快慢來比較反應速率的大小 B.若圖1所示實驗中反應速率為①>②,則一定說明Fe3+比Cu2+對H2O2分解催化效果好 C.用圖2裝置測定反應速率,可測定反應產生的氣體體積及反應時間 D.為檢查圖2裝置的氣密性,可關閉A處活塞,將注射器的活塞拉出一定距離,過一段時間后再松開活塞,觀察活塞是否回到原位 組卷:772引用:6難度:0.7
二、非選擇題:
-
8.過碳酸鈉(化學式xNa2CO3?yH2O2)遇水易分解為碳酸鈉和過氧化氫,有效增加水體中的溶解氧.某化學研究性學習小組的同學設計如圖裝置(夾持裝置略)測定過碳酸鈉的化學式(假設氣體完全反應或吸收).
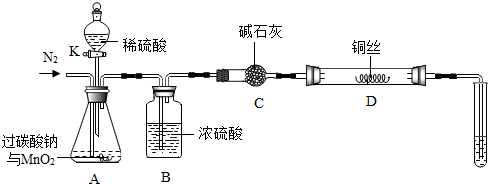
(1)實驗步驟:
①組裝儀器,;
②裝入藥品,通入一段時間N2,分別稱量裝置C和裝置D的質量為200g和250g;
③繼續通入N2,加熱裝置D,打開分液漏斗的活塞;
④過碳酸鈉完全反應后,停止加熱裝置D,繼續通入N2;
⑤停止通入N2,再次分別稱量裝置C和裝置D的質量為208.8g和254.8g;
(2)向錐形瓶中滴加稀硫酸,產生的氣體有,反應物中加入少量MnO2的作用是.
(3)根據實驗步驟,全套裝置缺少的玻璃儀器是,裝置B作用是,
(4)步驟②通入一段時間N2的目的是,步驟③繼續通入N2的目的是,步驟④繼續通入N2的目的是.
(5)導管始終插入水中的目的是,判斷氮氣通入速率的現象是.
(6)裝置D中反應的化學方程式為,實驗前后現象為.
(7)判斷過碳酸鈉完全反應的方法是.
(8)通過計算確定過碳酸鈉的化學式(寫出具體的計算過程).
(9)若測得的值偏大,原因可能是xy(只寫一種).組卷:40引用:2難度:0.5 -
9.小王同學對化學充滿了興趣,喜歡做各種實驗。有一次他和其它同學對鎂進行了一些研究:
【Ⅰ】他們用砂紙打磨掉表面灰黑色的物質,將其放入水中,未看到有明顯的現象,改用酒精燈加熱后,觀察到表面有大量氣泡,經驗是氫氣。他們又向溶液中滴加無色酚酞試液,發現酚酞變成紅色,說明有產生。該實驗表明化學反應的發生和速率與有關。
【Ⅱ】該小組成員開始研究鎂帶表面的灰黑色物質,小王大膽提出了三個假設:
假設1該物質是MgO;假設2該物質是Mg(OH)2;假設3鎂可能會像銅一樣生成堿式碳酸鎂。
但其它同這立即否定了他的假設1和2,因為根據所學的知識MgO,Mg(OH)2都是色固體。對于假設3,他們設計了如下方案
【Ⅲ】他們在取鎂帶表面灰黑色樣品時感到比較困難,索性將表面發黑的鎂帶全部磨成粉末,放入干燥的硬質試管中加熱,一段時間后,鎂粉突然出現紅熱燃燒起來,反應停止后有少量黑色物質A粘在試管壁上,這黑色物質A中混有什么?他們查資料篩選出幾條有價值的信息:實驗方案 實驗現象 實驗結論 證明有 CO2-3取樣于試管,加熱 證明有氫元素
(1)2Mg+CO2=2MgO+C; (2)C+2H2SO4(濃)=CO2↑+SO2↑+H2O;
試分析A物質為,根據上述信息,他們又設計了下列實驗,幫助他們完成實驗報告:
【Ⅳ】為驗證碳和濃硫酸反應的三種產物,應將氣體通過下列三種試劑(假設每步均完全)即:實驗方案 實驗現象 實驗結論 取反應后試管內樣品,先滴加過量的 再 (填一具體的實驗操作)黑色固體全部溶解
氣體→→→;(現象依次為)、、。
【V】該興趣小組的同學進一步又查出胃藥堿式碳酸鎂有多種不同的組成,如Mg2(OH)2CO3、Mg4(OH)2(CO3)3、Mg5(OH)2(CO3)4等。小紅同學為確定堿式碳酸鎂的組成,設計如圖所示的實驗:
實驗步驟(1)按圖組裝置后,首先進行的操作是,E處干燥管內盛放的藥品是,其作用是。
實驗步驟(2)稱取樣品31g,并將其放入硬質玻璃管中,稱量裝濃硫酸的洗氣瓶C的質量為87.6g,裝堿石灰的U型管D的質量為74.7g。
實驗步驟(3)打開活塞,關閉,緩慢鼓入空氣數分鐘。
實驗步驟(4)關閉活塞,打開,點燃酒精燈加熱至不再產生氣體為止。
實驗步驟(5)打開活塞K1,緩緩鼓入空氣數分鐘,然后拆下裝置,稱得洗氣瓶C的質量為89.4g,U型管D的質量為87.9g,則該堿式碳酸鎂的化學式為。
【Ⅵ】小明認為其化學式可用Mgx(OH)2(CO3)y表示,根據化合價規律,x和y的關系是,寫出該物質分解的方程式:。
小明設計了兩套方案(忽略裝置中原來的氣體)
方案I:只測定分解后生成的水,連接方案是A→C→B,則C中盛放的藥品是,B中盛放的藥品是。
方案Ⅱ:只測定分解生成的CO2的質量,連接方案是A→C→B→C,則B中的藥品是,最后連接的C中的藥品是。請你設計出更簡單的實驗方法。若取樣品7.88克,方案I測得生成水0.36g,方案Ⅱ測得生成CO2 3.52g,請你選擇實驗數據,通過計算得出堿式碳酸鎂的化學式。組卷:56引用:1難度:0.3


