2022-2023學(xué)年江蘇省南通市海安市實(shí)驗(yàn)中學(xué)高二(上)月考化學(xué)試卷(9月份)
發(fā)布:2024/4/20 14:35:0
一、單項(xiàng)選擇題:共13題,每題3分,共39分。每題只有一個(gè)選項(xiàng)最符合題意。
-
1.已知:過氧化氫的分解屬于放熱反應(yīng)。下圖為科研人員采用新型復(fù)合光催化劑,利用太陽光高效分解水,下列說法正確的是( )
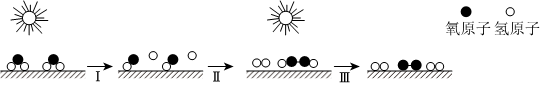
A.過程Ⅰ中水的極性鍵發(fā)生斷裂,吸收能量,過程Ⅲ中非極性鍵斷裂,放出熱量 B.過程Ⅱ產(chǎn)生的化合物只有氧化性,產(chǎn)生的過氧化氫是極性分子 C.過程Ⅲ中斷裂舊鍵吸收的能量小于形成新鍵放出的能量 D.該過程主要是吸收太陽能,將光能轉(zhuǎn)化為化學(xué)能,說明分解反應(yīng)均為吸熱反應(yīng) 組卷:25引用:1難度:0.7 -
2.1-丁烯(CH2=CHCH2CH3)和2-丁烯(CH3CH=CHCH3)分別與HCl發(fā)生反應(yīng),得到相同的產(chǎn)物2-氯丁烷(CH3CHClCH2CH3)的能量曲線如圖。下列說法錯(cuò)誤的是( )

A.2-氯丁烷的同分異構(gòu)體有3種 B.1molCH3CH=CHCH3中含有32mol電子 C.相同條件下,1-丁烯比2-丁烯穩(wěn)定 D.相同條件下,與2-丁烯相比,1-丁烯生成2-氯丁烷的ΔH更小 組卷:53引用:3難度:0.7 -
3.2022年2月,第24屆冬奧會在北京和張家口聯(lián)合舉行。本屆冬奧會的辦奧理念是“綠色、共享、開放、廉潔”。下列說法錯(cuò)誤的是( )
A.場館使用的光伏發(fā)電系統(tǒng)含有太陽能電池板,其主要材料是硅 B.冬奧會頒獎(jiǎng)花束所用的編織材料是以羊毛為原料的絨線,其主要成分為蛋白質(zhì) C.速滑館采用二氧化碳跨臨界直接制冰,實(shí)現(xiàn)二氧化碳的循環(huán)利用和零排放,干冰屬于分子晶體 D.冬奧會火炬改良了氣源比例,使火焰在日光下也清晰可見,火炬燃燒過程化學(xué)能完全轉(zhuǎn)化為熱能 組卷:16引用:3難度:0.7 -
 4.我國科學(xué)家利用計(jì)算機(jī)模擬技術(shù)研究CH3OH和SO3反應(yīng)的催化反應(yīng)歷程,如圖所示。下列說法錯(cuò)誤的是( )
4.我國科學(xué)家利用計(jì)算機(jī)模擬技術(shù)研究CH3OH和SO3反應(yīng)的催化反應(yīng)歷程,如圖所示。下列說法錯(cuò)誤的是( )A.該反應(yīng)是放熱反應(yīng) B.使用催化效果更好的催化劑,可降低該反應(yīng)的焓變 C.生成物的結(jié)構(gòu)簡式是CH3OSO3H D.該反應(yīng)過程中有O-H鍵的斷裂與形成 組卷:57引用:1難度:0.8 -
5.下列關(guān)于焓與熵的說法正確的是( )
A.焓與內(nèi)能無關(guān) B.化學(xué)反應(yīng)的反應(yīng)熱等于反應(yīng)的焓變 C.孤立體系(與環(huán)境沒有物質(zhì)交換和能量交換)的自發(fā)過程向著熵增方向進(jìn)行 D.焓與物質(zhì)的聚集狀態(tài)有關(guān),熵與物質(zhì)的聚集狀態(tài)無關(guān) 組卷:40引用:1難度:0.8
二、非選擇題:共4題,共61分。
-
16.如圖是煤的綜合利用過程中化工產(chǎn)業(yè)鏈的一部分

(1)煤的氣化發(fā)生的主要反應(yīng)是:C(s)+H2O(g)?CO(g)+H2(g)。
已知:
C(s)+O2(g)═CO2(g)ΔH=-393kJ?mol-1
H2(g)+O2(g)═H2O(g)ΔH=-242.0kJ?mol-112
CO(g)+O2(g)═CO2(g)ΔH=-283.0kJ?mol-112
煤氣化時(shí)發(fā)生主要反應(yīng)的熱化學(xué)方程式是。
(2)用煤氣化后得到的H2合成氨:N2(g)+3H2(g)?2NH3(g)ΔH=-92.4kJ?mol-1。在容積為2L的密閉容器中投入N2和H2充分反應(yīng),在不同時(shí)間改變反應(yīng)條件,正反應(yīng)速率的變化如圖所示。下列說法正確的是(填字母)。
a.t1時(shí)可能增大了N2的濃度
b.t2時(shí)可能充入了氦氣
c.t3時(shí)可能降低了溫度
d.t4時(shí)可能分離出氨氣
(3)如圖是合成氨反應(yīng)平衡混合氣中NH3的體積分?jǐn)?shù)隨溫度或壓強(qiáng)變化的曲線,圖中L(L1、L2)、X分別代表溫度或壓強(qiáng)。其中X代表的是(填“溫度”或“壓強(qiáng)”);判斷L1L2(填“>”或“<”),理由是。
(4)某溫度時(shí)合成甲醇的反應(yīng)CO(g)+2H2(g)?CH3OH(g)ΔH=-90.8kJ?mol-1,在容積固定的密閉容器中,各物質(zhì)的濃度如表所示:
①前2min的反應(yīng)速率v(H2)=濃度
時(shí)間c(CO)/mol?L-1 c(H2)/mol?L-1 c(CH3OH)/mol?L-1 0 1.0 1.8 0 2min 0.5 0.5 4min 0.4 0.6 0.6 6min 0.4 0.6 0.6 。
②該溫度下的平衡常數(shù)(可用分?jǐn)?shù)表示)。組卷:14引用:2難度:0.5 -
 17.“中和熱”是在稀溶液中,生成1mol液態(tài)水時(shí)所釋放的熱量。實(shí)驗(yàn)室用如圖所示簡易量熱裝置測定中和熱。量取50mL0.50mol?L-1鹽酸,用溫度計(jì)測量鹽酸溫度并記錄(數(shù)據(jù)見下表)。用水將溫度計(jì)上的酸沖洗干凈,擦干。再量取50mL0.55mol?L-1氫氧化鈉溶液,用同一支溫度計(jì)測量溫度。將兩份溶液在量熱計(jì)內(nèi)筒(小燒杯)中迅速混合,立即蓋上蓋板,勻速攪拌,密切關(guān)注溫度變化,記錄最高溫度。
17.“中和熱”是在稀溶液中,生成1mol液態(tài)水時(shí)所釋放的熱量。實(shí)驗(yàn)室用如圖所示簡易量熱裝置測定中和熱。量取50mL0.50mol?L-1鹽酸,用溫度計(jì)測量鹽酸溫度并記錄(數(shù)據(jù)見下表)。用水將溫度計(jì)上的酸沖洗干凈,擦干。再量取50mL0.55mol?L-1氫氧化鈉溶液,用同一支溫度計(jì)測量溫度。將兩份溶液在量熱計(jì)內(nèi)筒(小燒杯)中迅速混合,立即蓋上蓋板,勻速攪拌,密切關(guān)注溫度變化,記錄最高溫度。
已知:水的比熱容為4.18J?g-1?℃-1。H+(aq)+OH-(aq)═H2O(l)ΔH=-57.3kJ?mol-1。本實(shí)驗(yàn)所用酸、堿稀溶液的密度和ΔH2比熱容與水近似相等,并忽略量熱計(jì)的比熱容。
請回答下列問題:實(shí)驗(yàn)編號 反應(yīng)物溶液的溫度 反應(yīng)前體系溫度 反應(yīng)后體系溫度 溫度差 HCl(aq) NaOH(aq) 1 24.8℃ 25.0℃ 24.9℃ 27.8℃ 2.9℃ 2 25.0℃ 25.2℃ 25.1℃ 28.1℃ 3.0℃ 3 25.0℃ 25.0℃ 25.0℃ 28.1℃ 3.1℃
(1)儀器A的名稱是;碎泡沫塑料的作用是。
(2)該裝置存在一處明顯錯(cuò)誤,請指出:。
(3)為什么實(shí)驗(yàn)中只允許使用同一支溫度計(jì),不能使用兩支溫度計(jì)?請說明理由:。
(4)根據(jù)實(shí)驗(yàn)記錄的數(shù)據(jù)計(jì)算,該實(shí)驗(yàn)測得的中和熱ΔH1=kJ?mol-1。用相同濃度和體積的醋酸代替鹽酸進(jìn)行上述實(shí)驗(yàn),測得的中和熱ΔH2ΔH1(填“>”、“=”或“<”)。組卷:16引用:2難度:0.7


