2021-2022學年河北省衡水市武強中學高二(下)期中化學試卷
發布:2024/4/20 14:35:0
一、(每小題只有一個正確答案,每小題3分,共27分)
-
1.化學與生活、社會密切相關。下列說法不正確的是( )
A.燃煤中加入適量石灰石,可減少廢氣中SO2的量 B.“遼寧艦”上用于艦載機降落攔阻索的特種鋼纜,屬于新型無機非金屬材料 C.為防止電池中的重金屬污染土壤和水體,應積極開發廢舊電池的綜合利用技術 D.利用太陽能、風能和氫能等能源替代化石能源有利于實現“低碳經濟” 組卷:5引用:1難度:0.8 -
2.下列過程或現象與鹽類水解無關的是( )
A.純堿溶液去油污 B.鐵在潮濕的環境下生銹 C.加熱氯化鐵溶液顏色變深 D.濃硫化鈉溶液有臭味 組卷:335引用:92難度:0.9 -
3.2NO(g)+O2(g)?2NO2(g)體系中能使該反應的反應速率增大,且平衡向正反應方向移動的是( )
A.及時分離出NO2氣體 B.擴大容器體積 C.增大O2的濃度 D.選擇高效催化劑 組卷:15引用:1難度:0.5 -
4.分析下表中的四個熱化學方程式,判斷氫氣和丙烷的標準燃燒熱分別是( )
“嫦娥一號”發射火箭燃料 液氫(H2) ①2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ?mol-1
②2H2(l)+O2(l)═2H2O(g)△H=-482.6kJ?mol-1北京奧運會“祥云”火炬燃料 丙烷(C3H8) ③C3H8(l)+5O2(g)═3CO2(g)+4H2O(g)△H=-2013.8kJ?mol-1
④C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-2221.5kJ?mol-1A.-571.6 kJ?mol-1,-2221.5kJ?mol-1 B.-285.8 kJ?mol-1,-2013.8 kJ?mol-1 C.-285.8 kJ?mol-1,-2221.5 kJ?mol-1 D.-241.3 kJ?mol-1,-2013.8 kJ?mol-1 組卷:19引用:4難度:0.9 -
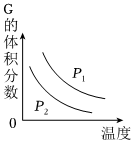 5.在一密閉容器中有如下反應:L (s)+a G (g)?b R (g)溫度和壓強對該反應的影響如圖所示,其中壓強P1<P2,由此可判斷( )
5.在一密閉容器中有如下反應:L (s)+a G (g)?b R (g)溫度和壓強對該反應的影響如圖所示,其中壓強P1<P2,由此可判斷( )A.正反應為放熱反應 B.化學方程式中的計量數a>b C.G的轉化率隨溫度升高而減小 D.增大壓強,容器內氣體質量不變 組卷:123引用:15難度:0.7
三、非選擇題
-
16.電離平衡常數(用Ka表示)的大小可以判斷電解質的相對強弱。25℃時,有關物質的電離平衡常數如下表所示:
(1)HF、H2CO3、HClO酸性由強到弱的順序為化學式 HF H2CO3 HClO 電離平衡常數(Ka) 7.2×10-4 K1=4.4×10-7
K2=4.7×10-113.0×10-8 。物質的量濃度均為0.1mol/L的下列溶液:a.Na2CO3 b.NaClO c.NaHCO3 d.NaF,pH值由大到小的順序是(填編號)
(2)將濃度為0.1mol/LHF溶液加水稀釋一倍(假設溫度不變),下列各量增大的是。
A.c(H+)
B.c(H+)?c(OH-)
C.c(H+)c(HF)
D.c(OH-)c(H+)
(3)25℃時,在20mL0.1mol/L氫氟酸中加入VmL0.1mol/LNaOH溶液,測得混合溶液的pH變化曲線如圖所示,下列說法正確的是。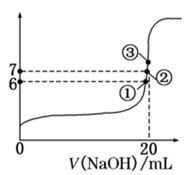
A.pH=3的HF溶液和pH=11的NaF溶液中,由水電離出的c(H+)相等
B.①點時pH=6,此時溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②點時,溶液中的c(F-)=c(Na+)
D.③點時V=20mL,此時溶液中c(F-)<c(Na+)=0.1mol/L組卷:10引用:1難度:0.6 -
17.完成下列問題。
(1)節能減排是當今社會的熱門話題,研發混合動力汽車對于中國汽車業的未來具有重要的戰略意義。混合動力汽車持續工作時間長,動力性好的優點,無污染、低噪聲的好處,汽車的熱效率可提高10%以上,廢氣排放可改善30%以上,某種混合動力汽車的動力系統由“1.6L汽油機+自動變速器+20kW+200V鎳氫電池”組成。
①混合動力汽車所用的燃料之一是乙醇,lg乙醇完全燃燒生成CO2氣體和液態H2O放出30.0kJ熱量,寫出乙醇燃燒的燃燒熱的熱化學方程式。
②鎳氫電池的使用可以減少對環境的污染,它采用儲氫金屬為負極,堿液NaOH為電解液,鎳氫電池充電時發生反應Ni(OH)2=NiO(OH)+H2。其放電時的正極的電極反應方程式為12。
(2)二氧化錳、鋅是制備干電池的重要原料,工業上用軟錳礦(含MnO2)和閃鋅礦(含ZnS)聯合生產二氧化錳、鋅的工藝如圖: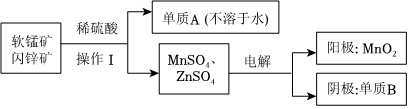
①操作I需要的玻璃儀器是。
②軟錳礦(含MnO2)和閃鋅礦與硫酸反應的化學方程式為,上述電解過程中,當陰極生成6.5gB時,陽極生成的MnO2的質量為。
③利用鋁熱反應原理,可以從軟錳礦中提取錳,發生的化學方程式為。組卷:2引用:1難度:0.7


