2020-2021學年安徽省淮北市樹人高級中學高一(下)期末化學試卷
發布:2024/11/23 2:30:1
一、選擇題(共18題,每小題只有一個正確答案,每小題3分,共計54分)
-
1.化學與生活密切相關,下列說法不正確的是( )
A.做衣服用的棉和麻均與淀粉互為同分異構體 B.煤經過氣化和液化等化學變化可轉化為清潔燃料 C.雙氧水和75%的酒精均可用于殺菌消毒,但原理不同 D.蛋白質灼燒時會產生燒焦羽毛的特殊氣味,利用這一性質可鑒別棉和蠶絲 組卷:2引用:1難度:0.9 -
2.下列表示正確的是( )
A.CO2的電子式: 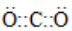
B.乙酸的結構式: 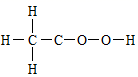
C.CH4的空間填充模型: 
D.乙烯的球棍模型: 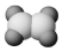 組卷:2引用:1難度:0.7
組卷:2引用:1難度:0.7 -
3.下列說法不正確的是( )
A.用電子式表示K2S的形成過程為: 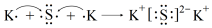
B.MgCl2和NaOH中的化學鍵類型完全相同,都屬于離子化合物 C.CO2和Cl2兩種分子中,每個原子的最外層都具有8電子穩定結構 D.反應2H2O+F2=O2+2HF,同時有極性鍵和非極性鍵的斷裂和形成 組卷:5引用:1難度:0.7 -
4.設阿伏加德羅常數的值為NA。下列說法不正確的是( )
A.2g的2H2O中含有的中子數為NA B.2.8g乙烯和丙烯(C3H6)的混合物完全燃燒,消耗O2的分子數為0.3 NA C.3.2gCu完全溶于一定量的濃硝酸,轉移電子數為0.1 NA D.1molCH4與1molCl2在光照條件下充分反應,得到CH3Cl的分子數為NA 組卷:28引用:2難度:0.8 -
5.下列指定反應的離子方程式正確的是( )
A.用氨水吸收足量的SO2氣體:2OH-+SO2=SO32-+H2O B.Ca(HCO3)2溶液與足量NaOH溶液反應:HCO3-+Ca2++OH-=CaCO3↓+H2O C.將稀鹽酸滴在石灰石上:CO32-+2H+=H2O+CO2↑ D.NaClO將污水中的NH3氧化成N2:3ClO-+2NH3=N2↑+3Cl-+3H2O 組卷:2引用:1難度:0.7 -
6.下列由實驗得出的結論正確的是( )
實驗 結論 A. 將乙烯通入溴的四氯化碳溶液,溶液最終變為無色透明 生成的1,2-二溴乙烷無色、可溶于四氯化碳 B. 乙醇和水都可與金屬鈉反應產生可燃性氣體 乙醇分子中的氫與水分子中的氫具有相同的活性 C. 用乙酸浸泡水壺中的水垢,可將其清除 乙酸的酸性小于碳酸的酸性 D. 甲烷與氯氣在光照下反應后的混合氣體能使濕潤的石蕊試紙變紅 生成的氯甲烷具有酸性 A.A B.B C.C D.D 組卷:2106引用:40難度:0.7 -
7.根據下表信息,判斷以下敘述正確的是( )
部分短周期元素的原子半徑及主要化合價元素代號 L M Q R T 原子半徑/nm 0.160 0.143 0.112 0.104 0.066 主要化合價] +2 +3 +2 +6、-2 -2 A.氫化物的沸點為H2T<H2R B.單質與稀鹽酸反應的速率為L<Q C.L2+與R2-的核外電子數相等 D.M與T形成的化合物具有兩性 組卷:15引用:3難度:0.9
二、填空題(本大題共四大題,共計46分)
-
21.NO2和N2O4之間發生反應:N2O4?2NO2,一定溫度下,體積為2L的密閉容器中,各物質的物質的量隨時間變化的關系如圖1所示。請回答下列問題:
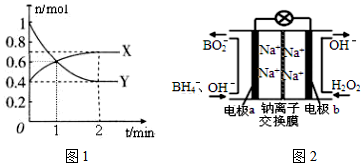
(1)曲線(填“X”或“Y”)表示NO2的物質的量隨時間的變化曲線。在0到1min中內用X表示該反應的速率是,該反應達最大限度時Y的轉化率。
(2)若上述反應在甲、乙兩個相同容器內同時進行,分別測得甲中 v(NO2)=0.3 mol?L-1?min-1,乙中y(N2O4)=0.2 mol?L-1?min-1,則中反應更快。
(3)下列描述能表示反應達平衡狀態的是。
A.容器中X與Y的物質的量相等
B.容器內氣體的顏色不再改變
C.2v(X)=v(Y)
D.容器內氣體的平均相對分子質量不再改變
E.容器內氣體的密度不再發生變化
(4)據報道以硼氫化合物NaBH4(H的化合價為-1價)和 H2O2作原料的燃料電池,可用作通信衛星電源。負極材料采用Pt/C,正極材料采用MnO2,其工作原理如圖2所示。寫出該電池放電時負極的電極反應式:。
(5)火箭發射常以液態肼(N2H4)為燃料,液態過氧化氫為助燃劑。
已知:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-534 kJ?mol-1
H2O2(l)=H2O(l)+O2(g)△H=-98.6 kJ?mol-112
寫出常溫下,N2H4(l) 與H2O2(l)反應生成N2和H2O的熱化學方程式:。組卷:0引用:1難度:0.7 -
22.某化學興趣小組的幾位同學探究原電池原理的應用時,做了如圖1的實驗:
(1)甲同學利用打磨過的銅片和鋁片設計了如圖1的實驗裝置,并測量和繪制了原電池的電流(I)隨時間(t)的變化曲線(極短時間電流反轉),則圖2中t1時刻之后階段,負極材料是。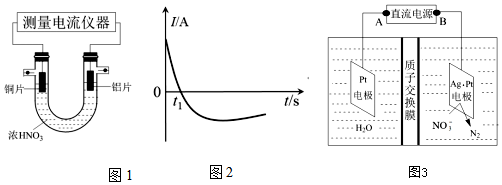
Ⅱ.銅與濃硝酸反應探究
(2)乙同學將銅片直接放入濃硝酸中:
①實驗現象為,溶液顯綠色。
②待反應停止后,若銅有剩余,再加入少量25%的稀硫酸,這時銅片上又有氣泡產生,原因是(用離子方程式表示)。
(3)電化學降解NO3-的原理如圖3所示。
電源正極為(填“A”或“B”),陽極的電極反應式為。若電解過程中轉移了2mol電子,則膜兩側電極液的質量變化差(△m左-△m右)為。組卷:10引用:1難度:0.5


