2021-2022學年江蘇省南通市如皋市高三(上)調研化學試卷(三)
發布:2024/4/20 14:35:0
一、選擇題(共7小題,每小題3分,滿分24分)
-
1.2021年,中國科學家突破了人工合成淀粉技術,以二氧化碳、氫氣為原料,人工合成淀粉。檢測發現,人工合成淀粉分子與天然淀粉分子的結構組成一致。下列說法正確的是( )
A.人工合成的淀粉屬于無機物 B.合成淀粉和葡萄糖的分子式相同 C.淀粉屬于單糖 D.該技術有助于解決糧食危機 組卷:5引用:1難度:0.8 -
2.利用蛋白質的變性可以進行消毒殺菌。下列物質均能使蛋白質變性,其中變性的原理與物質的性質具有對應關系的是( )
A.乙醇的揮發性 B.鹽酸的還原性 C.NaClO的氧化性 D.甲醛的可溶性 組卷:15引用:1難度:0.7 -
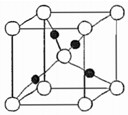 3.閱讀下列資料,完成第3~4題:葡萄糖和蔗糖都是常見的糖類,均為有甜味的無色晶體,易溶于水。葡萄糖與新制Cu(OH)2可發生如下反應:RCHO+2Cu(OH)2+NaOHRCOONa+Cu2O↓+3H2O(RCHO表示葡萄糖)。Cu2O的晶胞如右圖所示。蔗糖水解的實驗過程是:在試管中加入2mL蔗糖溶液,接著加入2mL2mol?L-1 H2SO4溶液,加熱。△
3.閱讀下列資料,完成第3~4題:葡萄糖和蔗糖都是常見的糖類,均為有甜味的無色晶體,易溶于水。葡萄糖與新制Cu(OH)2可發生如下反應:RCHO+2Cu(OH)2+NaOHRCOONa+Cu2O↓+3H2O(RCHO表示葡萄糖)。Cu2O的晶胞如右圖所示。蔗糖水解的實驗過程是:在試管中加入2mL蔗糖溶液,接著加入2mL2mol?L-1 H2SO4溶液,加熱。△
下列說法正確的是( )A.葡萄糖分子間不能形成氫鍵 B.葡萄糖分子中含4個手性碳原子 C.基態Cu2+的電子排布式為[Ar]3d84s1 D.NaOH的電子式為 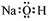 組卷:5引用:0難度:0.60
組卷:5引用:0難度:0.60 -
 4.閱讀下列資料,完成第3~4題:葡萄糖和蔗糖都是常見的糖類,均為有甜味的無色晶體,易溶于水。葡萄糖與新制Cu(OH)2可發生如下反應:RCHO+2Cu(OH)2+NaOHRCOONa+Cu2O↓+3H2O(RCHO表示葡萄糖)。Cu2O的晶胞如右圖所示。蔗糖水解的實驗過程是:在試管中加入2mL蔗糖溶液,接著加入2mL2mol?L-1 H2SO4溶液,加熱。△
4.閱讀下列資料,完成第3~4題:葡萄糖和蔗糖都是常見的糖類,均為有甜味的無色晶體,易溶于水。葡萄糖與新制Cu(OH)2可發生如下反應:RCHO+2Cu(OH)2+NaOHRCOONa+Cu2O↓+3H2O(RCHO表示葡萄糖)。Cu2O的晶胞如右圖所示。蔗糖水解的實驗過程是:在試管中加入2mL蔗糖溶液,接著加入2mL2mol?L-1 H2SO4溶液,加熱。△
下列關于蔗糖水解實驗的說法正確的是( )A.蔗糖水解產物均為葡萄糖 B.檢驗蔗糖是否水解的方法是:取上述反應后的溶液,冷卻后加入少量新制Cu(OH)2,加熱,若有紅色沉淀生成,則蔗糖已水解 C.可以用如下方法配制新制Cu(OH)2:在試管中加入2mL10%NaOH溶液,滴加5滴2%CuSO4溶液 D.Cu2O晶胞中,距離每個Cu+最近的O2-有4個 組卷:4引用:0難度:0.70 -
5.前3周期主族元素X、Y、Z、W的原子序數依次增大,X是空氣中含量最多的元素,基態時Y最外層電子數是次外層的四分之一,基態Z原子3p軌道上只有1個電子,W與X位于同一主族。下列說法正確的是( )
A.原子半徑:r(W)>r(Z)>r(Y)>r(X) B.第一電離能:I1(X)>I1(Y)>I1(Z) C.X的簡單氣態氫化物分子的空間構型為平面三角形 D.最高價氧化物對應水化物的堿性:Z>Y 組卷:42引用:4難度:0.6
三、解答題(共4小題,滿分64分)
-
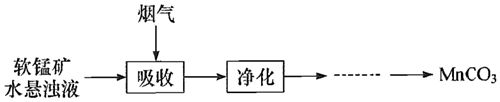
16.高純碳酸錳(MnCO3)是制備Mn2O3、MnO2等錳的氧化物的重要原料。實驗室模擬工業用軟錳礦(主要成分MnO2,雜質金屬元素Fe、Al)的水懸濁液吸收煙氣中SO2,制取高純MnCO3的流程如圖:
(1)吸收過程在如圖1所示裝置中進行,用混有SO2的空氣模擬煙氣。反應過程中,為使SO2盡可能轉化完全,在SO2和空氣比例一定、水浴溫度一定、不改變固液投料并充分攪拌的情況下,還可采取的合理措施有(任寫一種)。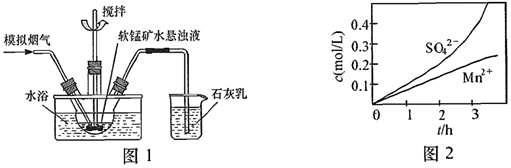
(2)實驗測得吸收液中Mn2+、SO42-的物質的量濃度隨時間變化的關系如圖2所示。
①導致吸收液中SO42-的物質的量濃度大于Mn2+的原因是。
②2h后,吸收液中SO42-的物質的量濃度增大速率加快的原因是。驗證的實驗方法是。
(3)將三頸燒瓶中的混合物過濾,測得濾液中c(Mn2+)=1.0mol?L-1,還含有Fe3+和Al3+。常溫下,由100mL該濾液制取高純MnCO3的實驗方案為:向溶液中邊攪拌邊滴加1.0mol?L-1 NaOH溶液,,干燥,得高純MnCO3固體。[實驗中可供選擇的試劑有1.0mol?L-1 BaCl2溶液、1.0mol?L-1 NaHCO3溶液、無水乙醇]
已知:
Ⅰ.MnCO3難溶于水和乙醇,在潮濕條件下易被氧化;
Ⅱ.常溫Ksp[Al(OH)3]=10-32.9,Ksp[Fe(OH)3]=10-37.4,Ksp[Mn(OH)2]=10-12.8。當溶液中金屬離子的濃度小于1×10-5mol?L-1時認為沉淀完全;
Ⅲ.加NaOH溶液調節pH過程中溶液總體積變化忽略不計。組卷:5引用:1難度:0.5 -
17.CO、SO2及氮氧化物(NOx)都是常見的大氣污染物,消除污染并實現資源化利用是化學工作者研究的重要課題。
(1)水煤氣變換[CO(g)+H2O(g)?CO2(g)+H2(g)]可用于生產氫氣。我國學者結合實驗與計算機模擬結果,研究了在金催化劑表面上水煤氣變換的反應歷程,如圖1所示,該歷程中決定總反應速率快慢所對應反應的活化能是。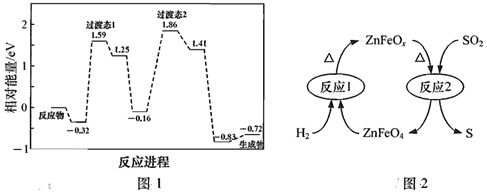
(2)新型納米材料氧缺位高鐵酸鹽( ZnFeOx)能將煙氣中的SO2除去,原理如圖2所示。當x=3.5時,轉化的SO2和H2的體積比為。
(3)工業上用亞硫酸鈉溶液作吸收液脫除煙氣中的SO2。吸收后的溶液用雙陽離子交換膜電解技術可使吸收液再生,工作原理如圖3所示(電極均為惰性電極)。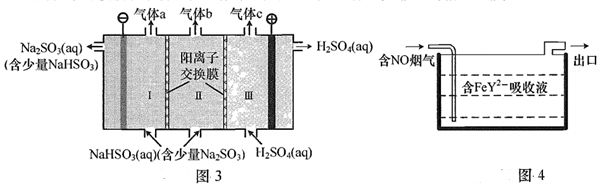
①氣體b的化學式為。
②電解時陰極上的電極反應方程式為。
(4)H2Y2-與Fe2+生成的絡合物FeY2-可用于吸收煙氣中的NO。其吸收原理如下:FeY2-(aq)+NO(g)?FeY2-(NO)(aq)ΔH<0。
①將含NO的煙氣以一定流速通入起始溫度為50℃的FeY2-溶液,裝置如圖4所示。出口處氣體中NO的含量隨通入煙氣時間的延長而增加。原因是。
②向FeY2-(NO)(aq)中加入鐵粉后生成NH3和Fe(OH)2,并使吸收液再生。寫出反應的離子方程式。組卷:12引用:1難度:0.6


