2022-2023學(xué)年陜西省西安市鐵一中學(xué)高二(上)期末化學(xué)試卷
發(fā)布:2024/4/20 14:35:0
一、選擇題:(本題共16小題,每題3分,共48分.在每小題給出的四個(gè)選項(xiàng)中,只有一項(xiàng)是符合題目要求的).
-
1.用NA表示阿伏加德羅常數(shù)的數(shù)值,下列說法正確的是( )
A.標(biāo)準(zhǔn)狀況下,1molH2O的體積為22.4L B.16gO2和O3的混合氣體中所含的氧原子數(shù)目為NA C.1L1.00mol/LNaCl溶液中含有的離子總數(shù)為NA D.2.4gMg轉(zhuǎn)化為鎂離子時(shí)失去的電子數(shù)目為0.1NA 組卷:27引用:1難度:0.6 -
2.一定條件下,下列選項(xiàng)所示的含氯物質(zhì)間轉(zhuǎn)化均能實(shí)現(xiàn)的是( )
A.Cl2(g) HClO(aq)H2OCl2(g)光照B.NaCl(aq) NaOH(aq)通電NaAlO2(aq)Al2O3C.NaCl(aq) NaHCO3(s)過量CO2Na2CO3(s)△D.AlCl3(aq) AlCl3(s)△Al(S)通電組卷:39引用:2難度:0.8 -
3.下列關(guān)于化學(xué)用語(yǔ)表示正確的是( )
A.F-的結(jié)構(gòu)示意圖: 
B.中子數(shù)是19的Cl原子: Cl1917C.二氧化碳分子的比例模型: 
D.NaHCO3在水中的電離方程式:NaHCO3═Na++H++ CO2-3組卷:15引用:2難度:0.7 -
 4.據(jù)文獻(xiàn)報(bào)道,氨催化還原法可用來(lái)消除某些污染氣體,其反應(yīng)歷程如圖所示:.
4.據(jù)文獻(xiàn)報(bào)道,氨催化還原法可用來(lái)消除某些污染氣體,其反應(yīng)歷程如圖所示:.
下列說法正確的是( )A.V的核外電子排布式為3d34s2 B.當(dāng)消耗標(biāo)準(zhǔn)狀況下11.2LO2時(shí),整個(gè)過程轉(zhuǎn)移6 mol e- C.V5+-OH 在該反應(yīng)過程中作催化劑,V4+-OH 是該反應(yīng)過程的中間產(chǎn)物 D.總反應(yīng)化學(xué)方程式:4NH3+3O2 2N2+6H2O催化劑組卷:26引用:4難度:0.7 -
5.下列用來(lái)表示物質(zhì)變化的化學(xué)反應(yīng)中,正確的是( )
A.鋼鐵腐蝕時(shí)可能發(fā)生的正極反應(yīng):4OH--4e-═2H2O+O2↑ B.表示中和熱的離子方程式:H++OH-═H2O;ΔH=-57.3kJ/mol C.明礬水解反應(yīng)的離子方程式:Al3++3H2O═Al(OH)3+3H+ D.硫酸銨溶液與氫氧化鈉溶液混合共熱的離子方程式: +OH-NH+4NH3↑+H2O△組卷:10引用:2難度:0.9 -
6.X、Y、Z為三種短周期元素.X原子最外層電子數(shù)是核外電子層數(shù)的3倍;Y在地殼中的含量?jī)H次于X;Y、Z同周期,Z的常見化合價(jià)為+2.下列說法不正確的是( )
A.X、Y、Z的原子序數(shù)依次增大 B.X與Z形成的化合物為離子化合物 C.X與Y形成的化合物只含共價(jià)鍵 D.存放Z單質(zhì)的倉(cāng)庫(kù)失火不能用CO2滅火 組卷:101引用:6難度:0.9
二、綜合題:52分
-
19.草酸(H2C2O4,二元弱酸)與草酸鹽在實(shí)驗(yàn)和工業(yè)生產(chǎn)中都起著重要的作用,常溫下,H2C2O4:Ka1=5.4×10-2,Ka2=5.4×10-5.H2CO3:K1=4×10-7 K2=6×10-11。
(1)NaHCO3溶液顯性。
(2)常溫下,0.1 mol?L-1的Na2C2O4溶液pH=a,0.1 mol?L-1的Na2CO3溶液pH=b,則ab (填“>”“<”或“=”)。
(3)常溫下,pH=3的H2C2O4溶液的物質(zhì)的量濃度為c1,水電離出的c(H+)為c3;pH=4的H2C2O4溶液的物質(zhì)的量濃度為c2,水電離出的c(H+)為c4.則c110 c2(填“>”“<”或“=”,下同);c310 c4。
(4)常溫下,用0.100 0 mol?L-1 NaOH溶液滴定20.00 mL某未知濃度的H2C2O4溶液,滴定曲線如圖,c點(diǎn)所示溶液中:2c(C2)+2c(HC2O2-4)+2c(H2C2O4)=c(Na+)O-4
①該草酸溶液的物質(zhì)的量濃度為(結(jié)果保留三位小數(shù))。
②a點(diǎn)所示溶液中各離子的濃度由大到小的順序?yàn)?。組卷:74引用:2難度:0.5 -
20.連二亞硫酸鈉(Na2S2O4)又稱為保險(xiǎn)粉,常作還原劑,能溶于冷水,難溶于乙醇,在堿性介質(zhì)中穩(wěn)定。
Ⅰ.用甲酸鈉(HCOONa)生產(chǎn)保險(xiǎn)粉的工藝流程如圖1。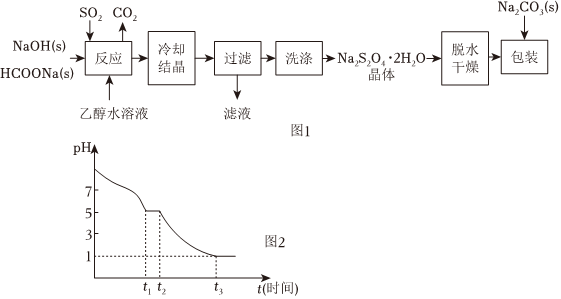
回答下列問題:
(1)Na2S2O4中硫元素的化合價(jià)為。
(2)“濾液”中可以循環(huán)利用的物質(zhì)是。
(3)“洗滌”所用試劑最好為。(填序號(hào))
a.冰水
b.熱水
c.無(wú)水乙醇
d.90%乙醇水溶液
(4)“反應(yīng)”在70℃條件下進(jìn)行,寫出發(fā)生反應(yīng)的化學(xué)方程式。
(5)在包裝保存“保險(xiǎn)粉”時(shí)加入少量的Na2CO3固體,目的是。
Ⅱ.探究保險(xiǎn)粉的性質(zhì)
(6)現(xiàn)將0.05mol?L-1Na2S2O4溶液在空氣中放置,其溶液的pH與時(shí)間(t)的關(guān)系如圖2所示。
①t1時(shí)溶液中含硫元素的粒子濃度由大到小的順序。
②t2→t3段發(fā)生反應(yīng)的離子方程式為。
(7)取少量連二亞硫酸鈉在隔絕空氣的條件下加強(qiáng)熱使其完全分解,得到Na2SO3、Na2S2O3和一種氣體(STP),該反應(yīng)中氧化產(chǎn)物、還原產(chǎn)物的物質(zhì)的量之比為。組卷:28引用:2難度:0.5


