2019-2020學年湖南省長沙市瀏陽一中高三(上)第六次月考化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本題包括24小題,每小題2分,共48分,每小題只有一個選項符合題意)
-
1.中華文化源遠流長、博大精深。從化學的視角看,下列理解不正確的是( )
A.“千淘萬漉雖辛苦,吹盡黃沙始到金”中“淘”“漉”相當于分離提純操作中的“過濾” B.漢代燒制出“明如鏡、聲如磬”的瓷器,其主要原料為黏土 C.“凡石灰,經火焚煉為用”,這段記載中涉及分解反應 D.北斗導航專用ASIC硬件結合國產處理器打造出一顆真正意義的“中國芯”,其主要成分為SiO2 組卷:7引用:2難度:0.8 -
2.下列說法正確的是( )
A.合成纖維和光導纖維都是新型無機非金屬材料 B.食品包裝中常放入有鐵粉的小袋,防止食物受潮變質 C.鎂在空氣中燃燒生成氧化鎂、氮化鎂,鐵在氧氣中燃燒生成氧化鐵 D.將廢動植物油脂經反應改性制成“生物柴油”,代替柴油作為內燃機燃料的做法符合“綠色化學”的理念 組卷:4引用:2難度:0.6 -
3.下列表示正確的是( )
A.雙氧水的電子式: 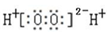
B.二氧化硅的分子式:SiO2 C.聚氯乙烯的結構簡式: 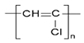
D.乙炔的球棍模型:  組卷:11引用:4難度:0.6
組卷:11引用:4難度:0.6 -
4.NA為阿伏加德羅常數的值,下列說法正確的是( )
A.標準狀況下,11.2LCl2溶于水,溶液中Cl2、Cl-、ClO-和HClO的微粒數之和為NA B.MnO2與足量濃鹽酸反應產生22.4LCl2時轉移電子數為2NA C.100mL 18mol?L-1濃硫酸與足量Cu粉加熱反應,產生SO2分子數為0.9NA D.常溫常壓下,9.5g羥基(-18OH)含有的中子數為5 NA 組卷:12引用:2難度:0.5 -
5.廢舊銀鋅紐扣電池(含Zn、Ag、石墨及少量Hg、Mn等)的正極片中回收銀的工藝流程如圖:下列說法錯誤的是( )
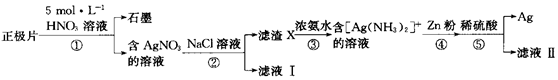
A.①中會產生對大氣有污染的氣體 B.③的離子方程式為Ag++2NH3?H2O ═[Ag(NH3)2]++2H2O C.⑤中加稀硫酸的目的是除去銀粉中的鋅 D.合理處理廢舊電池有利于保護環境和資源再利用 組卷:12引用:2難度:0.4 -
6.下列離子方程式正確的是( )
A.強堿性溶液中NaClO將Fe(OH)3氧化為FeO42-:3ClO-+2Fe(OH)3═2FeO42-+3Cl-+4H++H2O B.硬脂酸與乙醇的酯化反應:C17H35COOH+C2H518OH C17H35COOC2H5+H218O濃硫酸△C.用稀硫酸除去硫酸鈉溶液中少量的硫代硫酸鈉:S2O32-+2H+═SO2↑+S↓+H2O D.向NH4HCO3溶液中加入足量石灰水:Ca2++HCO3-+OH-═CaCO3↓+H2O 組卷:22引用:4難度:0.6 -
7.下列離子組在給定條件下離子共存判斷及反應的離子方程式均正確的是( )
選項 條件 離子組 離子共存判斷及反應的離子方程式 A 滴加氨水 Na+、Al3+、Cl-、NO3- 不能大量共存,Al3++3OH-═Al(OH)3↓ B AG=lg[ ]=10的溶液中c(H+)c(OH-)NH4+、Fe2+、I-、NO3- 一定能大量共存 C pH=1的溶液 Fe2+、Al3+、SO42-、MnO4- 不能大量共存,5Fe2++MnO4-+8H+═Mn2++5Fe3++4H2O D 通入少量SO2氣體 K+、Na+、ClO-、SO42- 不能大量共存,2ClO-+SO2+H2O═2HClO+SO32- A.A B.B C.C D.D 組卷:44引用:3難度:0.6 -
8.實驗室模擬工業漂白液(有效成分為NaClO)脫除廢水中氨氮(NH3)的流程如下:粗鹽
精制鹽提純①Cl電解②漂白吸收③NaCl。下列分析正確的是( )廢水(含)NH3④A.①中采用蒸餾的方法精制粗鹽水 B.②中陽極的主要電極反應:4OH--4e-=2H2O+O2↑ C.③中制備漂白液的反應:Cl2+2OH-=HCl+HClO D.②、③、④中均發生了氧化還原反應 組卷:0引用:2難度:0.7 -
9.僅用下表提供的儀器(夾持儀器和試劑任選)不能實現相應實驗目的是( )
選項 實驗目的 儀器 A 除去氫氧化鋁膠體中的泥沙 漏斗(帶濾紙)、燒杯、玻璃棒 B 從食鹽水中獲得NaCl晶體 坩堝、玻璃棒、酒精燈、泥三角 C 用0.1000mol?L-1的鹽酸測定未
知濃度的NaOH溶液濃度堿式滴定管、酸式滴定管、錐形瓶、膠頭滴管、燒杯 D 用MnO2和濃鹽酸制取干燥、純
凈的Cl2圓底燒瓶、分液漏斗、酒精燈、洗氣瓶、集氣瓶、導管、石棉網 A.A B.B C.C D.D 組卷:1182引用:11難度:0.9
二、非選擇題(本題包括4小題,共52分)
-
27.開發、使用清潔能源發展“低碳經濟”,正成為科學家研究的主要課題。氫氣、甲醇是優質的清潔燃料,可制作燃料電池。
(1)已知:①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H1=-1275.6kJ?mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ?mol-1
③H2O(g)═H2O(l)△H3=-44.0kJ?mol-1
寫出甲醇不完全燃燒生成一氧化碳和液態水的熱化學方程式:。
(2)工業上甲醇利用水煤氣合成,反應為CO(g)+2H2(g)═CH3OH(g)△H<0.在一定條件下,將1molCO和2molH2通入密閉容器中進行反應,當改變某一外界條件(溫度或壓強)時,CH3OH的體積分數φ(CH3OH)變化趨勢如圖所示: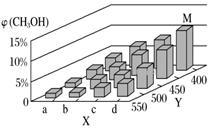
①平衡時,M點CH3OH的體積分數為10%,則CO的轉化率為。
②X軸上a點的數值比b點(填“大”或“小”)。
③生產甲醇的原料CO和H2來源于:CH4(g)+H2O(g)?CO(g)+3H2(g)△H>0,一定條件下CH4的平衡轉化率與溫度、壓強的關系如圖1.則T1T2(填“<”、“>”、“=”,下同);A、B、C三點處對應平衡常數(KA、KB、KC)的大小關系為。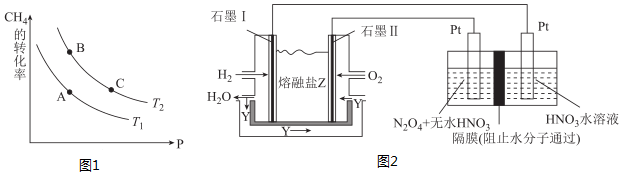
(3)現以H2、O2、熔融鹽Na2CO3組成的燃料電池,采用電解法制備N2O5,裝置如圖2所示,其中Y為CO2。
寫出石墨Ⅰ電極上發生反應的電極反應式。在電解池中生成N2O5的電極反應式為。組卷:4引用:2難度:0.8 -
28.美托洛爾可用于治療各類型高血壓及心絞痛,其一種合成路線如圖:
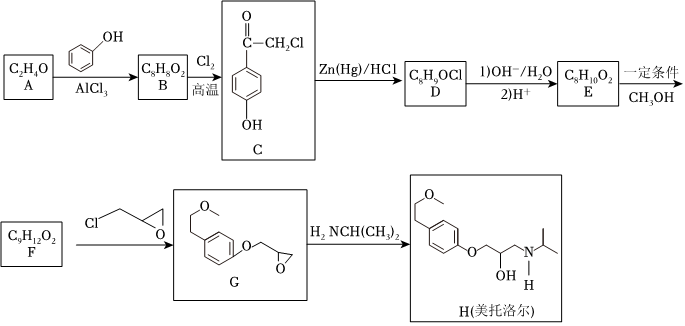
已知:①CH3COCH2RCH3CH2CH2R;Zn(Hg)HCl
②B-F苯環上均只有兩個取代基
回答下列問題:
(1)A的化學名稱是,C中含氧官能團的名稱是。
(2)E→F的反應類型是,G的分子式為。
(3)D的結構簡式為。
(4)反應B→C的化學方程式為。
(5)芳香族化合物W是G的同分異構體,符合下列條件的同分異構體共有種。(不考慮含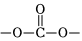 的結構)
的結構)
①W能發生水解反應
②核磁共振氫譜有4組峰,峰面積之比為9:3:2:2
(6)4一芐基苯酚(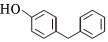 )是一種藥物中間體,請設計以苯甲醇和苯酚為原料制備4-芐基苯酚的合成路線:(無機試劑任用)。組卷:5引用:2難度:0.4
)是一種藥物中間體,請設計以苯甲醇和苯酚為原料制備4-芐基苯酚的合成路線:(無機試劑任用)。組卷:5引用:2難度:0.4


