2021-2022學年上海市曹楊二中高一(上)月考化學試卷(12月份)
發布:2024/4/20 14:35:0
一、選擇題(每題僅有一個選項符合題意,共60分)
-
1.在氯水中存在多種分子和離子,它們在不同的反應中表現出各自的性質,下列實驗現象和結論一致且正確的是( )
A.加入AgNO3溶液產生白色沉淀,說明溶液中有Cl-存在 B.溶液呈淺黃綠色,且有刺激性氣味,說明有HCl分子存在 C.向氯水中放入紅色布條,一會兒紅色布條褪色,說明溶液中有Cl2存在 D.加入NaOH溶液,氯水強黃綠色消失,說明有HClO分子存在 組卷:9引用:1難度:0.7 -
 2.在學習了氯元素相關化合物的知識后,某學生繪制了如圖所示的轉化關系,下列敘述錯誤的是( )
2.在學習了氯元素相關化合物的知識后,某學生繪制了如圖所示的轉化關系,下列敘述錯誤的是( )A.d的水溶液見光易分解 B.常溫下,含a的濃溶液與二氧化錳充分反應可制取b C.從氧化還原角度分析可知:a和f混合可以制得b,a和e混合也可制得b D.b可以用于自來水的殺菌消毒,f可以用于環境殺菌消毒 組卷:29引用:2難度:0.5 -
 3.實驗室制取氯氣裝置如圖所示,主要操作步驟為:
3.實驗室制取氯氣裝置如圖所示,主要操作步驟為:
①加熱制取氯氣
②收集氯氣
③檢查裝置氣密性
④處理尾氣。
下列選項中正確的實驗操作順序是( )A.①②③④ B.③①②④ C.②④③① D.④③①② 組卷:162引用:2難度:0.5 -
4.實驗室常用二氧化錳與濃鹽酸共熱制取氯氣,對于該反應,下列說法正確的是( )
A.二氧化錳是該反應的催化劑 B.該反應涉及的氧化物有兩種 C.可用濃硫酸除去氯氣中的氯化氫氣體雜質 D.反應中,還原劑與氧化產物的物質的量之比為4:1 組卷:108引用:2難度:0.5 -
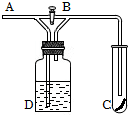 5.如圖所示,在A處通入含水蒸氣的氯氣,關閉B閥時,C處的(干燥的)紅色布條看不到明顯現象;當打開B閥后,C處的紅色布條逐漸褪色.則D瓶中盛放的溶液不可能是( )
5.如圖所示,在A處通入含水蒸氣的氯氣,關閉B閥時,C處的(干燥的)紅色布條看不到明顯現象;當打開B閥后,C處的紅色布條逐漸褪色.則D瓶中盛放的溶液不可能是( )A.濃硫酸 B.氫氧化鈉溶液 C.飽和碘化鉀溶液 D.飽和氯化鈉溶液 組卷:167引用:2難度:0.5 -
6.歷史上曾有化學家用以下方法制取氯氣,反應原理如圖所示。下列推斷不正確的是( )

A.反應Ⅰ屬于復分解反應 B.反應Ⅱ的化學方程式為2CuCl2+O2═2Cl2+2CuO C.CuCl2是整個過程的催化劑 D.該方法制氯氣主要原料是鹽酸和氧氣 組卷:90引用:3難度:0.5 -
7.某學習小組擬用手持技術對新制飽和氯水進行檢測,下列圖象變化最有可能是其檢測結果的是( )
A. 
氯水pH隨時間的變化B. 
溶液中氯離子濃度隨時間的變化C. 
氯水的電導率隨時間的變化D. 
液面上方氧氣體積分數隨時間的變化組卷:342引用:12難度:0.5 -
8.用如圖裝置制備并檢驗Cl2的性質,下列有關說法正確的是( )
A. 
圖中:如果MnO2過量,濃鹽酸就可全部反應B. 
圖中:充分光照后,量筒中液體酸性增強C. 
圖中:生成藍色的煙,若在集氣瓶中加入少量水,所得溶液呈黃色D. 
圖中:干燥的有色布條不褪色,濕潤的有色布條能褪色,說明Cl2有漂白性組卷:79引用:3難度:0.5 -
9.下列物質檢驗的方法正確的是( )
A.向某溶液中加硝酸銀溶液生成白色沉淀,說明原溶液中有Cl- B.向某溶液中加BaCl2溶液生成白色沉淀,說明原溶液中有SO42- C.向某溶液中加稀鹽酸,生成的氣體能使澄清石灰水變渾濁,說明原溶液中有CO32- D.向某深黃色溶液中,加入CCl4溶液后分層且下層為紫色,可確定有I2存在 組卷:15引用:2難度:0.7 -
10.下列說法正確的是( )
A.容量瓶、量筒上都標有溫度和“0”刻度 B.油鍋著火時用水滅火 C.用容量瓶配制溶液時,定容時俯視刻度線,所配溶液濃度偏低 D.用潔凈的鉑絲蘸取某溶液于酒精燈火焰上灼燒,焰色黃色,則該溶液可能為鈉鹽溶液 組卷:7引用:1難度:0.7 -
11.下列實驗操作正確的是( )
A.用酒精萃取碘水中的碘 B.用過濾的方法除去NaCl溶液中含有的少量淀粉溶液 C.蒸餾時,應使溫度計溫感泡上沿與蒸餾燒瓶支管口下沿齊平 D.用分液漏斗分離汽油和水,水和汽油分別用兩個燒杯在下口接 組卷:6引用:1難度:0.5
二、填空題(共40分)
-
 32.氯氣是一種重要的化工原料,在生產和生活中應用十分廣泛。實驗室也可用高錳酸鉀固體和濃鹽酸反應氯氣。
32.氯氣是一種重要的化工原料,在生產和生活中應用十分廣泛。實驗室也可用高錳酸鉀固體和濃鹽酸反應氯氣。
(1)請為該實驗選擇合適的發生裝置(填“a”或“b”)。
(2)寫出儀器的名稱:①;②。
(3)當集氣瓶中收集滿氯氣時,可以觀察到氣體呈色,干燥的氯氣可使濕潤的有色布條褪色,是因為的漂白性(填化學式,下同)。
(4)反應中,氧化產物是,實驗結束時,可選用溶液來吸收多余的氯氣。實驗室配制好2.0mol/LNaOH溶液,至少需要這種溶液mL才能與4.48L氯氣(標準狀況)恰好完全反應。
(5)現需220mL2.0mol/LNaOH溶液,需稱量g氫氧化鈉固體,上述實驗需要的儀器有電子天平、藥匙、燒杯、量筒、玻璃棒、膠頭滴管和。
(6)工業上常用電解飽和食鹽水制取氯氣:2NaCl+2H2O2NaOH+電解+Cl2↑,該反應中,陽極發生的電極反應是。標況下生成2.24LCl2時,轉移電子mol。組卷:19引用:1難度:0.7 -
 33.為了探究Fe2+、Cu2+、Ag+的氧化性強弱。設計實驗如圖所示。請回答:
33.為了探究Fe2+、Cu2+、Ag+的氧化性強弱。設計實驗如圖所示。請回答:
(1)實驗I、II的現象和結論如表:
實驗I的現象:實驗編號 實驗現象 實驗結論 I ① 氧化性:Cu2+>Fe2+ II 溶液變藍色 ② ;實驗II得到的結論:。寫出實驗II中發生反應的化學方程式:。向FeCl2溶液中滴加氯水,發現溶液顏色變為黃色,說明氯氣的氧化性強于(填離子符號)。
(2)實驗II中的AgNO3完全反應后,抽出銅絲,洗凈后干燥,稱重,發現銅絲比反應前增重0.152g,則反應生成的Ag的質量為g。組卷:6引用:1難度:0.7


