2021-2022學年北京161中高一(下)期中化學試卷(選考)
發布:2024/11/8 1:30:2
一、選擇題:本大題共20道小題,每小題2分,共40分。在每小題給出的四個選項中,只有一項符合題目的要求。把正確答案涂寫在答題卡上相應的位置。
-
1.下列物品所使用的主要材料屬于無機非金屬材料的是( )
A B C D 



陶瓷工藝品 紙質練習簿 不銹鋼臉盆 鋁罐 A.A B.B C.C D.D 組卷:7引用:1難度:0.7 -
2.下列說法正確的是( )
A.氨氣有刺激性氣味,因此不可以用作制冷劑 B.晶體硅用來做光導纖維 C.富勒烯屬于新型無機非金屬材料 D.二氧化硫有毒,不能用作食品添加劑 組卷:14引用:1難度:0.6 -
3.下列說法中正確的一組是( )
A.H2和D2互為同位素 B. 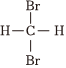 和
和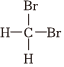 是同一種物質
是同一種物質C.正丁烷和異丁烷是同系物 D. 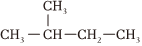 和
和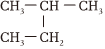 互為同分異構體組卷:22引用:5難度:0.9
互為同分異構體組卷:22引用:5難度:0.9 -
4.對下列事實的解釋錯誤的是( )
A.在蔗糖中加入濃硫酸后出現發黑現象,說明濃硫酸具有脫水性 B.濃硝酸在光照條件下顏色變黃,說明濃硝酸不穩定 C.常溫下濃硫酸、濃硝酸可以用鋁罐貯存,說明濃硫酸、濃硝酸與鋁不反應 D.硝酸露置于空氣中溶液濃度會減小因為揮發性 組卷:19引用:1難度:0.5 -
5.下列變化中,屬于吸熱反應的是( )
A.氫氧化鋇與氯化銨的反應 B.鎂條與鹽酸的反應 C.氫氣在氯氣中燃燒 D.固體氫氧化鈉溶于水 組卷:57引用:3難度:0.7 -
6.除去粗鹽溶液中的Ca2+、Mg2+、SO42-等雜質,需依次加入稍過量的NaOH溶液、X溶液、Y溶液,最終滴加稀鹽酸調至中性.其中X、Y分別是( )
A.Na2CO3 Ba(NO3)2 B.Na2CO3 AgNO3 C.Na2CO3 BaCl2 D.BaCl2 Na2CO3 組卷:225引用:11難度:0.9 -
7.下列反應中H2SO4既表現出酸性又表現出強氧化性的是( )
A.稀硫酸與CuO反應 B.稀硫酸與NaOH溶液反應 C.濃硫酸與灼熱的碳反應 D.濃硫酸與銅反應 組卷:18引用:1難度:0.6 -
8.利用固體表面催化工藝進行NO分解的過程如圖所示:

下列說法不正確的是( )A.NO是有毒氣體 B.催化劑能改變NO的分解速率 C.NO分解生成N2和O2 D.過程②釋放能量,過程③吸收能量 組卷:57引用:7難度:0.7
二、非選擇題:本部分共6題,共60分。請把答案填在答題紙中相應的橫線上。
-
25.用如圖方法回收廢舊CPU中的單質Au(金),Ag和Cu。
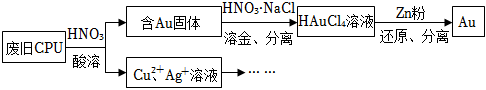
已知:①濃硝酸不能單獨將Au溶解。
②HAuCl4═H++。AuCl-4
(1)酸溶后經操作,將混合物分離。
(2)濃、稀HNO3均可作酸溶試劑。溶解等量的Cu消耗HNO3的物質的量不同,寫出消耗HNO3物質的量少的反應的化學方程式:。
(3)HNO3-NaCl與王水[V(濃硝酸):V(濃鹽酸)=1:3]溶金原理相同。
①將溶金反應的化學方程式補充完整:Au+NaCl+HNO3(稀)═HAuCl4+++NaNO3。
②關于溶金的下列說法正確的是。
A.用到了HNO3的氧化性
B.王水中濃鹽酸的主要作用是增強溶液的酸性
C.用濃鹽酸與NaNO3也可使Au溶解
(4)若用Zn粉將溶液中的1molHAuCl4完全還原,則參加反應的Zn的物質的量是mol。組卷:10引用:1難度:0.6 -
26.某小組同學通過“FeSO4被濃HNO3氧化”的實驗,驗證Fe2+的還原性。
實驗一:驗證Fe2+的還原性
(1)紅棕色氣體是實驗操作 預期現象 實驗現象 向盛有2 mLFeSO4溶液的試管
中,滴入幾滴濃硝酸,振蕩試管中產生紅棕色氣
體,溶液變為黃色試管中產生紅棕色氣
體,溶液變為深棕色。
(2)實驗現象與預期不符,繼續進行實驗。
取深棕色溶液于試管中,滴加KSCN溶液,溶液變為紅色,該現象說明。
實驗二:探究溶液變為深棕色的原因
【資料與猜想】
查閱資料后猜想,可能是生成的NO2或NO與溶液中的Fe2+或Fe3+反應,而使溶液變為深棕色。
【實驗與探究】
用下圖所示裝置進行實驗(氣密性已檢驗,尾氣處理已略去)
ⅰ.關閉c,打開a和b,通入N2,一段時間后關閉a;
ⅱ.向甲中加入適量濃HNO3,一段時間后丙中溶液變為深棕色,丁中溶液無明
顯變化;
ⅲ.關閉b、打開c,更換丙、丁中的溶液(試劑不變);
ⅳ.繼續向甲中加入濃HNO3,一段時間后觀察到了與ⅱ相同的實驗現象。
(1)通入N2的目的是。
(2)銅與濃硝酸反應的化學方程式是。
(3)裝置乙的作用是。
(4)實驗結論是。
【反思與改進】
實驗三:驗證Fe2+的還原性
該小組同學依據實驗二的結論改進了實驗一,觀察到了預期現象,其實驗操作是。組卷:44引用:4難度:0.6


