2020-2021學年四川省綿陽市東辰國際學校高一(下)第一次月考化學試卷
發布:2024/4/20 14:35:0
一、單項選擇題(本題共14題,每題3分,共42分)
-
1.《厲害了,我的國》展示了中國探索太空,開發深海,建設世界第一流的高鐵、橋梁、碼頭,5G技術聯通世界等取得的舉世矚目的成就。它們與化學有著密切聯系。下列說法不正確的是( )
A.耐高溫、耐腐蝕的合金材料,科學家們是從元素周期表中過渡元素去尋找的 B.D和T原子可用于制造氫彈 C.我國提出網絡強國戰略,光纜線路總長超過三千萬公里,光纜的主要成分是晶體硅 D.C919大型客機使用了大量先進復合材料、鋁鋰合金等,鋁鋰合金可減輕機身自重 組卷:12引用:2難度:0.6 -
2.雷雨天閃電時空氣中有O3生成。下列說法中,正確的是( )
A.等質量的O2和O3含有相同的質子數 B.16O和18O的相互轉化是化學變化 C.在相同的溫度和壓強下,等體積的O2和O3含有相同數目的原子 D.O2和O3互為同位素 組卷:22引用:2難度:0.8 -
3.MarieCurie(瑪麗居里)因為發現了放射性元素釙和鐳而獲得了1911年Nobel化學獎,關于鐳的敘述不正確的是( )
A.氫氧化鐳是一種弱堿 B.鐳的單質能與水劇烈反應生成氫氣 C.鐳在化合物中呈+2價 D.碳酸鐳難溶于水 組卷:51引用:2難度:0.3 -
4.下列敘述中,不正確的是( )
A.HCl溶于水時要破壞離子鍵 B.CCl4和NH3都是只含有極性鍵的共價化合物 C.Na2O2是含有非極性鍵的離子化合物 D.CaO和NaCl晶體熔化時要破壞離子鍵 組卷:18引用:2難度:0.7 -
5.三氟甲磺酸用途十分廣泛,是已知超強酸之一,其化學式為:CF3SO3H.下列有關說法正確的是( )
A.原子半徑:H<C<O<F<S B.熔沸點:CH4<H2S<H2O C.熱穩定性:H2S<HF<H2O D.上述元素中F的最高價含氧酸的酸性最強 組卷:39引用:3難度:0.7 -
6.室溫下,下列各組離子在指定溶液中能大量共存的是( )
A.FeCl2溶液中:K+、H+、NO3-、SO42- B.強酸性溶液中:K+、Na+、HCO3-、Cl- C.透明溶液中:K+、Cu2+、Cl-、NO3- D.FeCl3溶液中:Na+、SO42-、SCN-、NO3- 組卷:22引用:1難度:0.7
二、解答題(共6小題,滿分58分)
-
19.以硫鐵礦(主要成分為FeS2,還有少量CuS、SiO2等雜質)為原料制備綠礬晶體(FeSO4?7H2O)的工藝流程如圖:
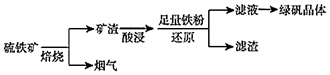
(1)“酸浸”過程,礦渣中的Fe2O3與稀H2SO4反應的離子方程式。
(2)煙氣中的SO2會污染環境,可用足量氨水吸收。寫出該反應的離子方程式。
(3)寫出檢驗濾液中陰離子的方法。
(4)鐵粉還原過濾,濾渣主要成分是(寫化學式)。
(5)燃料細菌脫硫法是用氧化亞鐵硫桿菌(T.f)對硫鐵礦進行催化脫硫,同時得到FeSO4溶液。其過程如圖所示: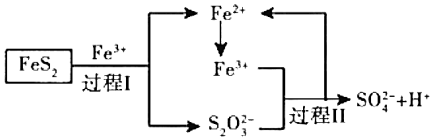
已知總反應為:FeS2+14Fe3++8H2O═2SO42-+15Fe2++16H+
寫出過程Ⅱ反應的離子方程式。組卷:26引用:4難度:0.4 -
20.32g銅投入一定濃度的硝酸溶液中,銅完全溶解,共收集到NO和NO2的混合氣體8.96L氣體(標準狀況)。
(1)計算產生NO和NO2的體積(標準狀況)分別為多少L?(請寫出計算過程)。
(2)將盛有此混合氣體的容器倒扣在水中,通入標準狀況下一定體積的O2,恰好使氣體完全溶于水中,則通入O2的體積為L。
(3)向100mL 0.8mol?L-1硝酸溶液中加入一定量Fe、FeO、Fe2O3的混合物,充分反應后,放出標準狀況下的氣體224mL,且測得溶液中鐵只以Fe2+形式存在,為使Fe2+完全沉淀,可向反應后的溶液中加入0.1mol?L-1的NaOHmL。組卷:23引用:2難度:0.5


