2021-2022學年江蘇省泰州市海陵區九年級(上)期末化學試卷
發布:2024/4/20 14:35:0
一.第一部分選擇題(20分)1—10題為單項選擇題,每題1分,共10分;11—15題為不定項選擇題,每題有1或2個答案,全部選對得2分,漏選一個得1分,錯選、多選不得分,共10分。
-
1.下列實驗室中的變化屬于化學變化的是( )
A.酒精揮發 B.試管破裂 C.鐵架臺生銹 D.蠟燭熔化 組卷:6引用:2難度:0.8 -
2.物質的性質決定物質的用途。下列說法錯誤的是( )
A.氮氣化學性質穩定,可作食品保護氣 B.銅導電能力強,可作導線 C.氧氣具有助燃性,可作火箭燃料 D.活性炭具有吸附性,可作冰箱除味劑 組卷:8引用:1難度:0.7 -
3.下列化學用語正確的是( )
A.鎂元素 mg B.一氧化碳 Co C.銨根離子 NH3+ D.兩個氮分子 2N2 組卷:20引用:1難度:0.5 -
4.實驗室制取二氧化碳的部分操作如圖,其中正確的是( )
A. 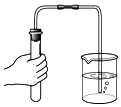
檢查氣密性B. 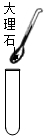
取用大理石C. 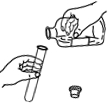
傾倒稀鹽酸D. 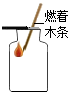
驗滿二氧化碳組卷:13引用:1難度:0.7 -
5.生活中下列物質屬于純凈物的是( )
A.汽水 B.不銹鋼 C.蒸餾水 D.白醋 組卷:10引用:1難度:0.8 -
 6.鉻是自然界中硬度最大的金屬。如圖是鉻在元素周期表中的信息及原子結構示意圖,下列有關敘述錯誤的是( )
6.鉻是自然界中硬度最大的金屬。如圖是鉻在元素周期表中的信息及原子結構示意圖,下列有關敘述錯誤的是( )A.鉻原子的質子數是24 B.鉻的相對原子質量是52.00g C.鉻屬于金屬元素 D.鉻原子核外有4個電子層 組卷:28引用:4難度:0.8
二.第二部分非選擇題(40分)過量酸
-
18.A~F是初中化學常見物質,其中A和C是組成元素相同的兩種液體,D和E是碳元素的兩種氧化物,F為黑色固體單質。它們相互反應和轉化關系如圖所示(圖中的“—”表示物質間能發生化學反應,“→”表示物質間存在轉化關系,部分反應物、生成物或反應條件已略去)。回答下列問題:
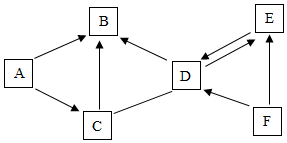
(1)F的化學式為,固態D的俗稱,E的一種用途為,自然界中D→B的轉化稱為作用。
(2)實驗室檢驗D的化學方程式為。
(3)寫出化學方程式:A→C,該反應屬于反應(填基本反應類型);D→E。組卷:442引用:2難度:0.5 -
19.我國力爭在2060年前實現“碳中和”。“碳中和”是指在一定時間內CO2的排放量和吸收量基本相當。
【CO2的排放】
(1)工業上化石燃料的大量燃燒是CO2排放逐年升高的主要原因,CO2的過度排放會導致的加劇。
【CO2的封存】
(2)地質封存:將CO2在高壓、低溫的條件下轉化為液態,注入地層中。從微觀角度分析,CO2從氣態轉化為液態,分子的間隙。
(3)海洋封存:將CO2運輸到封存地點,灌注于海洋深處。該方案可能導致海水逐漸酸化,原因是(用化學方程式表示)。
【CO2的轉化】
(4)已知CO2和H2在合適催化劑和一定溫度下可以發生反應,生成兩種氧化物。某研究小組設計如圖1裝置(固定裝置省略)探究該反應的產物。
查閱資料:①無水硫酸銅是一種白色固體,遇水變成藍色。
②堿石灰能充分吸收二氧化碳且不與氫氣、一氧化碳反應。
③H2是一種還原性氣體,高溫下可還原氧化銅、氧化鐵等金屬氧化物。
實驗現象及結論:B中白色固體變成藍色,說明CO2與H2反應生成了;D中色固體變為黑色,E中澄清石灰水變渾濁,說明CO2與H2反應生成了CO。裝置D中反應的化學方程式。
實驗反思:圖1裝置中有一處明顯不足,請指出。若去掉裝置E,則不能證明CO2與H2反應生成了CO,理由是。
【CO2的捕集】
(5)二氧化碳的“捕集”技術實現了二氧化碳的捕捉、封存和資源化利用。圖2為捕集二氧化碳流程圖。
已知:反應Ⅰ的化學方程式為:K2CO3+CO2+H2O═2KHCO3;KHCO3不穩定,受熱易分解。請回答相關問題:
①反應Ⅰ需控制在一定溫度范圍內進行,原因是。
②要利用反應Ⅰ吸收8.8噸CO2,需要消耗多少噸K2CO3?(寫出計算過程)
③上述捕集CO2的流程中,可循環利用的物質是。組卷:75引用:1難度:0.5


