2021-2022學(xué)年江西省撫州、贛州六校聯(lián)考高三(上)質(zhì)檢化學(xué)試卷
發(fā)布:2025/1/2 21:30:3
一、選擇題(本大題共15小題,每小題3分,共45分。在每小題給出的四個(gè)選項(xiàng)中,只有一項(xiàng)是符合題目要求的)
-
1.利用物質(zhì)的特殊性質(zhì)來(lái)檢驗(yàn)的分析方法很多,下列有關(guān)說(shuō)法錯(cuò)誤的是( )
A.用試紙對(duì)血糖或尿糖的監(jiān)測(cè)——利用葡萄糖特殊的性質(zhì)進(jìn)行分析 B.農(nóng)產(chǎn)品殘余農(nóng)藥的快速檢測(cè)——利用農(nóng)產(chǎn)品特殊的性質(zhì)進(jìn)行分析 C.大氣中污染物氮氧化合物的測(cè)定——進(jìn)行氮氧化合物性質(zhì)分析 D.新冠病毒核酸檢測(cè)方法——進(jìn)行核酸序列分析 組卷:26引用:1難度:0.6 -
2.NA是阿伏加德羅常數(shù)的值。下列說(shuō)法正確的是( )
A.1 molNa2O2固體中含有1mol 和1Na+2molO2-2B.1 molN2H4分子中含有5mol共價(jià)鍵 C.1molClO2 (二氧化氯)分子作氧化劑,最多得到4mol電子 D.1 與酸反應(yīng),最多消耗1molH+molAlO-2組卷:41引用:1難度:0.3 -
3.下列過(guò)程中的化學(xué)反應(yīng),相應(yīng)的離子(或化學(xué))方程式正確的是( )
A.工業(yè)上用飽和食鹽水吸收NH3、CO2制備N(xiāo)aHCO3:NH3+CO2+NaCl+H2O═NaHCO3↓+NH4++Cl- B.工業(yè)上用電化學(xué)氧化的方法,增加鋁金屬表面氧化膜厚度,陽(yáng)極反應(yīng)為:Al-3e-═Al3+ C.工業(yè)上制備硫酸時(shí),用98%的濃硫酸吸收SO3:SO3+H2O═2H++SO42- D.工業(yè)上用水吸收NO2制備50%的硝酸:3NO2+H2O═2H++2NO3-+NO 組卷:19引用:1難度:0.7 -
4.下列所選裝置與試劑合理,能達(dá)到實(shí)驗(yàn)?zāi)康牡氖牵ā 。?br />
選項(xiàng) 實(shí)驗(yàn)?zāi)康?/td> 分液漏斗內(nèi)試劑 錐形瓶?jī)?nèi)試劑 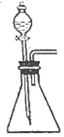
A 制CO2 鹽酸 碳酸鈣 B 制Cl2 濃鹽酸 二氧化錳 C 制NH3 飽和石灰水 氯化銨溶液 D 制SO2 濃硫酸 銅 A.A B.B C.C D.D 組卷:5引用:1難度:0.5 -
5.《考工記》:金(青銅)有六齊,六分其金而錫居一,謂之鐘鼎之齊;五分其金而錫居一,謂之斧斤之齊;四分其金而錫居一,謂之戈戟之齊;三分其金而錫居一,謂之大刃之齊;五分其金而錫居二,謂之削殺矢之齊;金錫半,謂之鑒燧之齊。下列有關(guān)說(shuō)法錯(cuò)誤的是( )
A.六齊是銅錫合金6種配比 B.大刃硬度大于斧斤 C.六齊之金,日久也會(huì)有銅綠生成 D.依據(jù)銅錫不同比例可以配成黃銅 組卷:191引用:1難度:0.3 -
6.綠色酸性廢蝕液中含有4種離子Fe3+、Cu2+、Cl-、H+,向其中加入鐵粉充分反應(yīng),下列說(shuō)法正確的是( )
A.反應(yīng)前的廢蝕液中,離子濃度最大的為Cl- B.加入鐵粉反應(yīng)后,離子濃度最大的為Fe2+ C.反應(yīng)后的溶液若為綠色,則溶液中不存在Fe3+、Cu2+ D.反應(yīng)后若固體有剩余,該固體為過(guò)量的鐵 組卷:81引用:1難度:0.7
二、非選擇題(本大題共4小題,共55分)
-
18.納米TiO2?2H2O作為一種重要的無(wú)機(jī)氧化物材料,因其在電子、化纖、廢水處理等諸多領(lǐng)域的應(yīng)用而備受關(guān)注。如圖是利用NH3、TiCl4、正丁醇—水制備納米TiO2?2H2O的簡(jiǎn)易裝置。
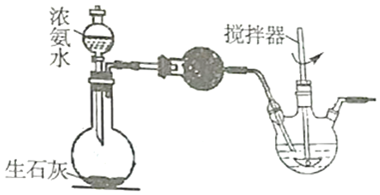
(1)請(qǐng)寫(xiě)出利用上圖裝置制備氨氣的化學(xué)方程式:。
(2)干燥管內(nèi)盛裝的物質(zhì)是,其作用為。
(3)實(shí)驗(yàn)過(guò)程:i.將160mL蒸餾水、鹽酸(4mL)和正丁醇混合于三頸燒瓶中,形成乳濁液,置于冰水浴中。
ii.向三頸燒瓶中緩慢滴加10mLTiCl4,然后組裝好裝置。
ⅲ.不斷攪拌并緩緩?fù)ㄈ隢H3至pH=3時(shí)停止。
①在水中的溶解度:正丁醇(填“大于”“等于”或“小于”)乙醇;
②TiCl4容易發(fā)生水解,生成TiO2?2H2O,由于顆粒太大不符合實(shí)驗(yàn)要求,請(qǐng)寫(xiě)出TiCl4水解反應(yīng)方程式:;實(shí)驗(yàn)中使用的鹽酸濃度為6mol/L,實(shí)驗(yàn)室配制該濃度溶液時(shí)使用的玻璃儀器有:燒杯、玻璃棒、膠頭滴管、一定規(guī)格的容量瓶和;本實(shí)驗(yàn)中鹽酸的作用有、;
③實(shí)驗(yàn)中需不斷攪拌,主要目的是充分混合正丁醇與水,使正丁醇把水切割、包圍在非常小的區(qū)域,這樣做的目的是(填序號(hào));
A.降低水解速率
B.使正丁醇完全溶于水
C.有利于形成TiO2?2H2O納米結(jié)構(gòu)
D.降低鹽酸的溶解性
④實(shí)驗(yàn)中不能使用溫水浴的主要原因是。組卷:4引用:1難度:0.6 -
19.高純AgNO3在感光、電子和信息、電鍍等行業(yè)中有著廣泛的用途。由粗銀制備高純AgNO3的流程圖如圖:
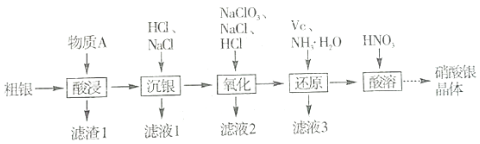
(1)物質(zhì)A的化學(xué)式為。
(2)沉銀的離子方程式為,若沉銀得到的固體顆粒越小,則過(guò)濾速率;若沉銀得到的固體顆粒結(jié)塊,則產(chǎn)品純度。
(3)“氧化”工序中,鹽酸濃度控制在1.5mol/L左右,如果超過(guò)規(guī)定濃度,則NaClO3消耗量會(huì)超過(guò)理論值,原因是;工藝中“氧化”工序的主要目的為。
(4)利用Vc、NH3?H2O把銀還原,操作中Vc、NH3?H2O加入順序?yàn)椋合认蚵然y固體中加入,后加入,其中還原劑是。
(5)“酸溶”工序中選擇用濃硝酸而不用稀硝酸溶解銀,主要目的是(填序號(hào))。
A.防止產(chǎn)生污染性氣體
B.減少硝酸消耗
C.增加反應(yīng)速率
D.減少“AgNO3晶體析出”時(shí)蒸發(fā)的水量
(6)為了進(jìn)一步提高AgNO3純度,需要對(duì)AgNO3晶體進(jìn)行(填操作方法)。組卷:3引用:1難度:0.5


