2021年天津市耀華中學(xué)高考化學(xué)二模試卷
發(fā)布:2024/12/14 1:30:1
一、選擇題(共12小題,每小題3分,滿(mǎn)分36分)
-
1.化學(xué)與生活生產(chǎn)社會(huì)可持續(xù)發(fā)展密切相關(guān),下列說(shuō)法錯(cuò)誤的是( )
A.免洗洗手液能殺菌消毒,主要是因?yàn)槠溆行С煞只钚糟y離子能使蛋白質(zhì)變性 B.牙膏中添加的Na2PO3F、NaF所提供的氟離子濃度相等時(shí),它們防治齲齒的作用是相同的 C.用聚氯乙烯代替木材,生產(chǎn)快餐盒,以減少木材的使用 D.石墨晶體中存在范德華力,常用作潤(rùn)滑劑 組卷:61引用:1難度:0.5 -
2.已知NA是阿伏加德羅常數(shù)的值,下列關(guān)于0.1mol?L-1Na2CO3溶液說(shuō)法正確的是( )
A.陰離子總數(shù)等于陽(yáng)離子總數(shù) B.100mL溶液中離子總數(shù)大于0.03NA C.溶液中離子濃度c(Na+)>c(OH-)>c(CO32-)>c(HCO3-) D.配制100mL需用托盤(pán)天平稱(chēng)取1.06g Na2CO3固體 組卷:107引用:1難度:0.6 -
3.下列化學(xué)用語(yǔ)表示正確的是( )
A.SO2分子的空間構(gòu)型:V型 B.丙烷的比例模型: 
C.中子數(shù)為20的硫原子: S2016D.CO32-水解的離子方程式:CO32-+2H2O?H2CO3+2OH- 組卷:19引用:1難度:0.6 -
4.下列操作能達(dá)到實(shí)驗(yàn)?zāi)康牡氖牵ā 。?/h2>
A. 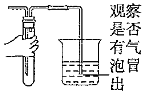
檢驗(yàn)裝置氣密性B. 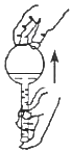
檢查容量瓶是否漏水C. 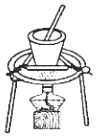
從食鹽溶液中獲得氯化鈉晶體D. 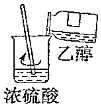
混合濃硫酸和乙醇組卷:49引用:4難度:0.5 -
5.下列敘述Ⅰ、Ⅱ有因果關(guān)系的是( )
敘述Ⅰ 敘述Ⅱ A CH4中碳元素處于最低化合價(jià),具有還原性 可燃冰是一種清潔能源 B Fe3+具有氧化性 NH4Fe(SO4)2?12H2O作凈水劑 C 斷裂NH3分子中H-N鍵要吸收熱量 工業(yè)上用液氨作制冷劑 D 有機(jī)玻璃(PMMA)透光性好、易加工 有機(jī)玻璃常作光學(xué)儀器 A.A B.B C.C D.D 組卷:44引用:3難度:0.7
二、解答題(共4小題,滿(mǎn)分0分)
-
15.二氧化氯(ClO2)是一種高效、廣譜的滅菌消毒劑。已知ClO2為橙黃色氣體,極易溶于水,在混合氣體濃度讀過(guò)高時(shí)易生發(fā)生爆炸。請(qǐng)回答下列問(wèn)題:
(1)“二氧化氯泡騰片”的有效成分為NaClO2、NaHSO4、NaHCO3,該泡騰片能快速溶于水,生成的ClO2溶于水得到ClO2溶液,同時(shí)生成另一種氣體而放出大量氣泡。每產(chǎn)生1molClO2消耗NaClO2的量為mol,產(chǎn)生另一種氣體的離子方程式為。
(2)在處理廢水時(shí),ClO2可與水中的有毒離子(如CN-)反應(yīng)生成兩種無(wú)毒氣體,反應(yīng)的離子方程式。
(3)利用NaClO3還原法可制備ClO2,其實(shí)驗(yàn)裝置如圖。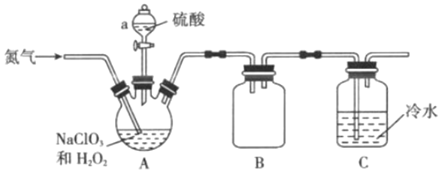
①儀器a的名稱(chēng)為﹔實(shí)驗(yàn)安全至關(guān)重要,從安全角度考慮A裝置左側(cè)通入氮?dú)獾哪康氖?!--BA-->,裝置A中生成ClO2的化學(xué)方程式為。
(4)ClO2穩(wěn)定性較差,需隨用隨制,產(chǎn)物用水吸收得到ClO2溶液,為測(cè)定所得溶液中的含量,進(jìn)行了以下實(shí)驗(yàn):
Ⅰ.準(zhǔn)確量取ClO2溶液10mL,稀釋成100mL試樣
Ⅱ.量取V1mL試樣加入錐形瓶中,調(diào)節(jié)試樣的pH≤2.0,加入足量的KI晶體,搖勻,在暗處?kù)o置30分鐘[已知2ClO2+10I-+8H+═5I2+2Cl-+4H2O]
Ⅲ.以淀粉溶液作為指示劑,用cmoL/LNa2S2O3溶液滴定至終點(diǎn),消耗Na2S2O3溶液V2mL。(已知2S2O32-+I2=2I-+S4O62-)
①準(zhǔn)確量取10.00mL ClO2溶液的玻璃儀器是。
②上述步驟Ⅲ中滴定終點(diǎn)的現(xiàn)象是。
③據(jù)上述步驟可以算出原ClO2溶液的濃度為mol?L-1(用含字母的代數(shù)式表示)
④實(shí)驗(yàn)中使用的標(biāo)準(zhǔn)溶液部分因被氧氣氧化而變質(zhì),則實(shí)驗(yàn)結(jié)果(填“偏高”、“偏低”或者“無(wú)影響”)組卷:66引用:1難度:0.5 -
16.近年來(lái)我國(guó)在環(huán)境治理上成效斐然。回答下列問(wèn)題:
(1)CH4還原氮氧化物使其轉(zhuǎn)化為無(wú)毒氣體,部分反應(yīng)的熱化學(xué)方程式及活化能(E)如下:
i.CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1E=1274kJ?mol-1
ii.CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ?mol-1E=493kJ?mol-1
①反應(yīng)CH4(g)+2NO2(g)═N2(g)+2H2O(g)+CO2(g)△H3=kJ?mol-1
②相同條件下,反應(yīng)i比反應(yīng)ii的速率慢,理由為。
(2)探究催化劑條件下CO和NO的處理,反應(yīng)原理為:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H4,向某密閉容器中充入等物質(zhì)的量的CO和NO,不同條件下NO的平衡轉(zhuǎn)化率如圖1所示: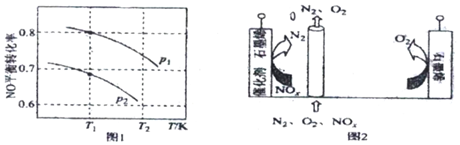
①下列事實(shí)能說(shuō)明該反應(yīng)達(dá)到平衡狀態(tài)的是(填選項(xiàng)字母)。
a.CO和NO的轉(zhuǎn)化率相等
b.NO和N2的總物質(zhì)的量不再發(fā)生變化
c.CO和CO2的總物質(zhì)的量不再發(fā)生變化
②△H40((填“>”、“<”或者“=”,下同),p1p2。
(3)最近我國(guó)科學(xué)家設(shè)計(jì)了一種電解法處理污染氣體中NOx的高效去除裝置,如圖2所示,其中電極分別為催化劑石墨烯(石墨烯包裹催化劑)和石墨烯。
①催化劑石墨烯為極(填“陰”或“陽(yáng)”)
②若電解質(zhì)溶液顯酸性,則催化劑石墨烯電極的電解反應(yīng)式為。
(4)燃煤煙氣脫硫的方法有多種,其中有種方法是用氨水將SO2轉(zhuǎn)化為NH4HSO3,再氧化成NH4HSO4,向NH4HSO3溶液中通入空氣氧化的離子方程式。
已知H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8。常溫下,將SO2通入某氨水中至溶液恰好呈中性,此時(shí)溶液中的=c(NH+4)c(HSO-3)。組卷:75引用:1難度:0.7


