2022-2023學年廣東番禺中學高一(上)期末化學試卷
發布:2024/4/20 14:35:0
一、單選題(1-10題,每題2分,共20分;11-18題,每題3分,共24分)
-
1.2022年諾貝爾物理獎獲得者之一使用鈣做實驗材料。下列說法正確的是( )
A.鈣的金屬活動性比鎂弱 B.鈣與水反應生成H2 C.鈣在自然界以單質形式存在 D.實驗中剩余的鈣丟入下水道 組卷:47引用:1難度:0.6 -
2.據古代文獻記載:“慈石治腎家諸病,而通耳明目”.“慈石,色輕紫,石上皸澀,可吸連針鐵”.文中“慈石”在一定條件下與下列物質反應屬于非氧化還原反應的是( )
A.稀硝酸 B.稀硫酸 C.氫碘酸 D.鋁粉 組卷:28引用:2難度:0.8 -
3.下列除去雜質的方法中,正確的是( )
選項 物質(括號內為雜質) 試劑 方法 A CO2(HCl) 飽和NaCl溶液 洗氣 B FeCl2(FeCl3) 銅粉 過濾 C Fe粉(Al粉) NaOH溶液 過濾 D KNO3(NaCl) AgNO3溶液 過濾 A.A B.B C.C D.D 組卷:25引用:3難度:0.7 -
4.下列物質轉化中有明顯顏色變化且沒有發生氧化還原反應的是( )
A.過氧化鈉粉末吸收水蒸氣 B.向含有KSCN的FeCl2溶液中滴加氯水 C.在硫酸鐵溶液中滴加Ba(OH)2溶液 D.向裝有濕潤紅色布條的集氣瓶中通入足量的氯氣 組卷:13引用:2難度:0.6 -
5.下列實驗能達到目的的是( )
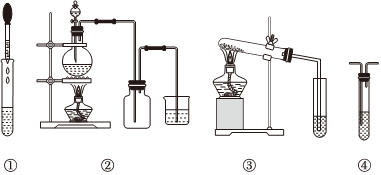
選項 A B C D 試劑 FeSO4溶液,NaOH溶液 濃鹽酸、MnO2 NaHCO3、澄清石灰水 Cl?、HCl、NaOH溶液 目的 制備并長時間觀察Fe(OH)3 制備純凈氯氣 探究NaHCO3的穩定性 除去氯氣中氯化氫 裝置 ① ② ③ ④ A.A B.B C.C D.D 組卷:23引用:3難度:0.7 -
6.下列排列順序不正確的是( )
①熱穩定性:H2O>H2S
②氧化性:Cu2+>Fe3+>H+>Fe2+
③原子半徑:Na>Mg>O
④還原性:F->Cl->S2-
⑤結合H+的能力:OH->CH3COO->Cl-
⑥酸性:H2CO3<HNO3<H3PO4A.②④⑥ B.①②③ C.③⑤ D.②④⑤ 組卷:38引用:1難度:0.7 -
7.O2F2可以發生反應:H2S+4O2F2═SF6+2HF+4O2,下列說法錯誤的是( )
A.氧氣是還原產物 B.O2F2是氧化劑 C.若生成4.48LHF,則轉移0.8mol電子 D.還原劑與氧化劑的物質的量之比為1:4 組卷:70引用:1難度:0.5
四、實驗題(每空2分,共14分)
-
21.ClO2又稱百毒凈,可用于水的消毒和紙張、紡織品的漂白。用如圖所示裝置(夾持裝置和加熱裝置省略)制備ClO2,并探究ClO2的某些性質。
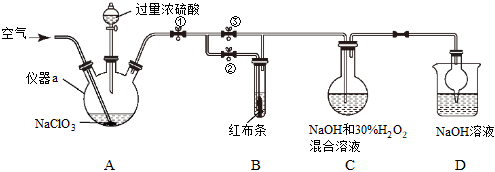
已知:①濃硫酸能與硫酸鈉反應,產物為硫酸氫鈉。
②飽和NaClO2溶液隨溫度變化情況如圖: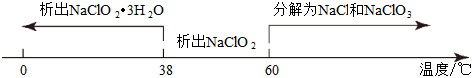
回答下列問題:
(1)寫出裝置A制備ClO2,同時生成高氯酸(HClO4)的化學方程式:。
(2)關閉止水夾②,打開止水夾①③,通入一段時間空氣,裝置C中生成NaClO2,離子方程式為。若關閉止水夾③,打開止水夾②,B中可觀察到的現象為。
(3)從裝置C反應后的溶液中獲得NaClO2晶體,需控溫在范圍內進行減壓蒸發結晶,采用減壓蒸發的原因是。
(4)下列說法不正確的是(填字母)。
A.通入的空氣可將A中產生的ClO2全部驅趕到C中
B.ClO2處理飲用水時殘留的ClO2-可用FeSO4除去,反應的離子方程式為ClO2-+2Fe2++4H+═2Fe3++Cl-+2H2O
C.工業上將ClO2氣體制成NaClO2固體,其主要目的是便于貯存和運輸
D.用Cl2和NaClO2制備ClO2,氧化劑與還原劑物質的量之比為2:1
(5)城市飲用水處理新技術用NaClO2、高鐵酸鈉替代Cl2。如果以單位質量的氧化劑所得到的電子數來表示消毒效率,那么NaClO2、Na2FeO4、Cl2的消毒效率由大到小的順序是。組卷:17引用:1難度:0.5
五、工業流程題(每空2分,共14分)
-
22.鋁土礦(主要成分為Al2O3,還含有SiO2、Fe2O3)是工業上制備氧化鋁的主要原料。工業上提取氧化鋁的工藝流程如圖。
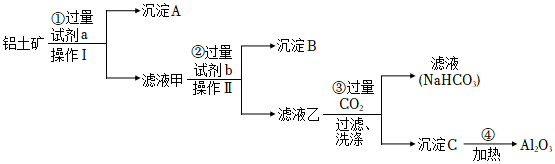
(1)沉淀A的化學式為,試劑b的化學式為。
(2)檢驗濾液甲中Fe3+時使用的試劑為。
(3)步驟②中加入過量b時,生成沉淀B的離子反應方程式為;得到濾液乙的離子反應方程式為。
(4)步驟③中通入過量CO2氣體而不加入過量鹽酸的理由是。
(5)準確稱取8g鋁土礦樣品,加入一定量試劑a的溶液,使其中的Al2O3、Fe2O3,恰好溶解;然后向濾液中加入10mol/L的NaOH溶液,產生沉淀的質量與加入NaOH溶液的體積關系如圖所示,則樣品中Al2O3的質量分數為。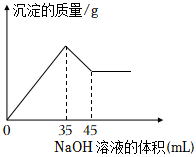 組卷:11引用:3難度:0.5
組卷:11引用:3難度:0.5


