2023年天津市高考化學最后一卷
發布:2024/5/3 8:0:9
一、單項選擇題:在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.在剛剛過去的2022年,我國的科技發展成果舉世矚目。下列說法不正確的是( )
A.2022年冬奧會中,國家速滑館“冰絲帶”采用CO2跨臨界制冰,比氟利昂更環保 B.2022年我國風電、光伏發電量突破一萬億千瓦時,光伏發電符合綠色發展理念 C.2022年我國鋰離子電池產量同比增長超130%,鋰離子電池屬于二次電池 D.2022年中國空間站全面建成,空間站所使用太陽能電池的主要成分為SiO2 組卷:95引用:5難度:0.7 -
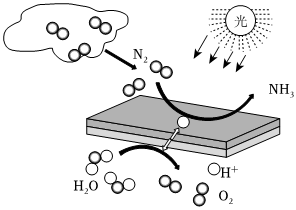 2.近年來,利用半導體光催化實現還原氮氣制備氨氣引起全世界極大關注。如圖是在半導體光催化的作用下,N2被光催化材料捕獲進而被還原實現“N2→NH3”的轉化示意圖。下列說法正確的是( )
2.近年來,利用半導體光催化實現還原氮氣制備氨氣引起全世界極大關注。如圖是在半導體光催化的作用下,N2被光催化材料捕獲進而被還原實現“N2→NH3”的轉化示意圖。下列說法正確的是( )A.此方法不屬于人工固氮技術 B.由轉化示意圖可知,氮氣化學性質很活潑 C.該反應過程中有共價鍵的斷裂和形成 D.該反應的化學方程式N2+H2 2NH3△組卷:179引用:3難度:0.8 -
3.下列說法中不正確的是( )
A.共價化合物中一定不含有離子鍵,離子化合物中可能含有共價鍵 B.充電電池放電時發生的是氧化還原反應,而充電時發生的是非氧化還原反應 C.離子的還原性由強到弱:S2->Cl->F- D.若石墨完全轉化為金剛石需吸收能量,則說明石墨比金剛石穩定 組卷:31引用:2難度:0.7 -
4.既可以用來鑒別甲烷和乙烯,又可以用來除去甲烷中混有的少量乙烯的操作方法是( )
A.混合氣通過盛酸性高錳酸鉀溶液的洗氣瓶 B.混合氣通過盛足量溴水的洗氣瓶 C.混合氣通過盛蒸餾水的洗氣瓶 D.混合氣跟適量氯化氫混合 組卷:192引用:25難度:0.7 -
5.食品保鮮膜按材質分為聚乙烯(PE)、聚氯乙烯(PVC)等種類。PVC被廣泛地用于食品、蔬菜外包裝,它對人體有潛在危害。下列有關敘述錯誤的是( )
A.PVC單體可由PE的單體與氯化氫加成制得 B.PVC保鮮膜屬于鏈狀聚合物,在高溫時易熔化,能溶于有機溶劑 C.用濕潤的藍色石蕊試紙檢驗加熱PE和PVC產生的氣體,可鑒別PE和PVC D.等質量的PE和乙烯完全燃燒消耗的氧氣質量相等 組卷:268引用:6難度:0.7
二、解答題
-
15.過氧化鈣在工農業生產中有廣泛的用途。
Ⅰ.過氧化鈣制備方法很多。
(1)制備方法一:H2O2溶液與過量的Ca(OH)2懸濁液反應可制備CaO2?8H2O,其化學方程式為。
(2)制備方法二:利用反應Ca(s)+O2CaO2(s),在純氧條件下制取CaO2,實驗室模擬裝置示意圖如圖:△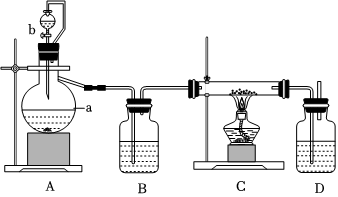
請回答下列問題:
①裝置A中反應的化學方程式為,儀器a的名稱為。
②裝置D中盛有的液體是濃硫酸,其作用一是;二是。
Ⅱ.水產運輸中常向水中加一定量CaO2?8H2O增加溶氧量(DO),水中溶氧量(DO)是用每升水中溶解氧氣的質量來表示,其測定步驟及原理為:
a.固氧:堿性下,O2將Mn2+氧化為MnO(OH)2:2Mn2++O2+4OH═2MnO(OH)2↓;
b.氧化:酸性下,MnO(OH)2將I-氧化為I2:MnO(OH)2+2I-+4H+═Mn2++I2+3H2O;
c.滴定:用Na2S2O3標準溶液滴定生成的I2:2S2+I2═S4O2-3+2I-。O2-6
某同學向水中加一定量CaO2?8H2O,取此水樣100.00mL,按上述方法測定水中溶氧量(DO),消耗0.0100mol?L-1 Na2S2O3標準溶液13.50mL。
(1)滴定過程中使用的指示劑是;
(2)該水樣中的溶解氧量(DO)為mg?L-1。
(3)步驟b中加入硫酸溶液反應后,若溶液pH過低,滴定時會產生明顯的誤差,寫出產生此誤差的原因(用離子方程式表示,至少寫出2個)。組卷:102引用:3難度:0.5 -
16.地球上的氮元素對動植物有重要作用,其中氨的合成與應用是當前的研究熱點。
(1)人工固氮最主要的方法是Haber-Bosch法。通常用以鐵為主的催化劑在400~500℃和10~30MPa的條件下,由氮氣和氫氣直接合成氨。
①已知上述反應中生成1molNH3放出46kJ熱量,該反應的熱化學方程式為。
②該反應放熱,但仍選擇較高溫度。其原因是。
(2)常溫常壓下電解法合成氨的原理如圖1所示: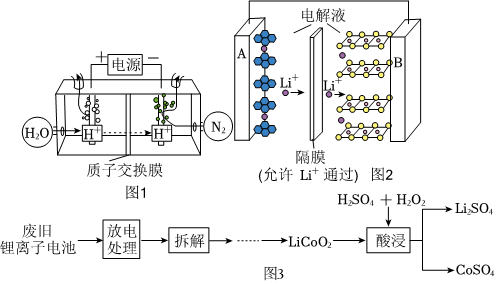
①陰極生成氨的電極反應式為。
②陽極氧化產物只有O2。電解時實際生成的NH3的總量遠遠小于由O2理論計算所得NH3的量,結合電極反應式解釋原因:。
(3)氨是生產氮肥的原料,經如下轉化可以得到NH4NO3。NH3NO①O2NO2②O2HNO3③H2O+NH4NO3④NH3
。已知:氮原子利用率是指目標產物中氮的總質量與生成物中氮的總質量之比上述反應③的氮原子利用率為66.7%。要使原料NH3轉化為NH4NO3的整個轉化過程中氮原子利用率達到100%,可采取的措施是。
(4)現在廣泛使用的鋰離子電池有多種類型。某可充電鈷酸鋰電池的工作原理如圖2所示。
①該電池放電時,其中一極的電極反應式是LixC6-xe-=6C+xLi+,則該極應為圖2中的(填“A”或“B”)。
②碳酸乙烯酯(EC)常用作電解液的溶劑,其結構為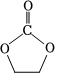 ,熔點35℃,可燃,可由二氧化碳和有機物X在一定條件下合成。X與乙醛互為同分異構體,核磁共振氫譜顯示只有一組峰。寫出合成EC的化學方程式:
,熔點35℃,可燃,可由二氧化碳和有機物X在一定條件下合成。X與乙醛互為同分異構體,核磁共振氫譜顯示只有一組峰。寫出合成EC的化學方程式: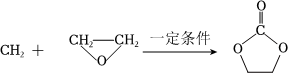 。
。
③從正極材料中回收鈷和鋰的流程如圖3所示,寫出酸浸過程中發生反應的化學方程式。拆解廢舊電池前需進行放電處理,既可保證安全又有利于回收鋰。有利于回收鋰的原因是。組卷:46引用:2難度:0.5


