2022-2023學(xué)年河南省鄭州外國語學(xué)校高一(上)期中化學(xué)試卷
發(fā)布:2024/12/18 0:30:2
一.選擇題(本題包括18小題,每小題3分,共54分,每小題只有一個選項符合題意)
-
1.下列說法正確的是( )
A.復(fù)分解反應(yīng)一定有沉淀、氣體或水生成 B.堿性氧化物一定是金屬氧化物 C.有單質(zhì)參加的反應(yīng)一定是氧化還原反應(yīng) D.丁達爾效應(yīng)是溶液和膠體的本質(zhì)區(qū)別 組卷:15引用:1難度:0.7 -
2.下列邏輯關(guān)系圖示正確的是( )
A. 
B. 
C. 
D.  組卷:7引用:1難度:0.7
組卷:7引用:1難度:0.7 -
3.《中國詩詞大會》不僅弘揚了中國傳統(tǒng)文化,還蘊含著許多化學(xué)知識,下列有關(guān)傳統(tǒng)文化分析不正確的是( )
A.李白詩句“日照香爐生紫煙,遙看瀑布掛前川”,“紫煙”指“香爐”中碘升華的現(xiàn)象 B.《抱樸子》記載“以曾青涂鐵,鐵赤色如銅”,涉及置換反應(yīng) C.于謙詩句“千錘萬鑿出深山,烈火焚燒若等閑”,涉及分解反應(yīng) D.曹植詩句“煮豆燃豆其,豆在釜中泣”,涉及氧化還原反應(yīng) 組卷:41引用:1難度:0.7 -
4.已知NA為阿伏加德羅常數(shù)的值,下列說法正確的是( )
A.標(biāo)況下,5.6LHF所含原子個數(shù)為0.5NA B.5.6g鐵粉與足量稀硫酸反應(yīng),轉(zhuǎn)移電子數(shù)0.2NA C.0.1mol/LAlCl3溶液中含有的Cl-數(shù)目為0.3NA D.將1L2mol/L的FeCl3溶液加入到沸水中,加熱使之完全反應(yīng),所得到的氫氧化鐵膠體粒子數(shù)為2NA 組卷:20引用:1難度:0.5 -
5.分類法是學(xué)習(xí)化學(xué)的重要方法,人們在認識事物時可采用多種分類方法。下表(2)不能與(1)歸為一類的是( )
選項 (1) (2) A FeCl2、Na2S、SO2 KI B H2SO4、CH3COOH、HClO H3PO4 C 過濾、滲析、蒸發(fā) 電離 D (NH4)2SO4、NH4Cl、NH4NO3 NH4HCO3 A.A B.B C.C D.D 組卷:7引用:1難度:0.7 -
6.下列說法不正確的是( )
A.同溫同壓下,體積相等的CH4和SO2,所含原子數(shù)之比為5:3 B.同溫同壓下,質(zhì)量相等的O2和CO2,密度比為8:11 C.同溫同體積的兩容器中,裝有等質(zhì)量的O2和N2,兩容器中壓強之比為8:7 D.同溫同壓下,等質(zhì)量的H2和N2的體積比為14:1 組卷:212引用:4難度:0.5 -
7.下列應(yīng)用或事實與膠體聚沉無關(guān)的是( )
①河流入海口處易形成三角洲;
②一支鋼筆使用不同品牌的墨水易堵塞;
③化工廠利用靜電除塵技術(shù)除廢氣中的固體懸浮物;
④在實驗中手不慎被玻璃劃破,可用FeCl3溶液應(yīng)急止血;
⑤由腎功能衰竭等疾病引起的血液中毒,可利用血液透析法進行治療;
⑥將鹽鹵或石膏加入豆?jié){,制成豆腐;
⑦清晨密林中可以看見一縷縷光束。A.①②④⑥ B.③④⑤ C.③⑤⑦ D.③⑥⑦ 組卷:32引用:1難度:0.6
二.填空題(每空2分,共46分)
-
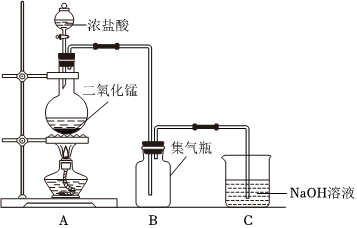 20.瑞典化學(xué)家舍勒是最早發(fā)現(xiàn)氯氣的人,他在研究軟錳礦礦石(主要成分是二氧化錳)時,把濃鹽酸和軟錳礦礦石混合加熱,意外地得到了氯氣。至今,實驗室中還用這種方法制取氯氣,裝置如圖所示,化學(xué)反應(yīng)方程式為:MnO2+4HCl(濃)MnCl2+Cl2↑+2H2O。回答下列問題:△
20.瑞典化學(xué)家舍勒是最早發(fā)現(xiàn)氯氣的人,他在研究軟錳礦礦石(主要成分是二氧化錳)時,把濃鹽酸和軟錳礦礦石混合加熱,意外地得到了氯氣。至今,實驗室中還用這種方法制取氯氣,裝置如圖所示,化學(xué)反應(yīng)方程式為:MnO2+4HCl(濃)MnCl2+Cl2↑+2H2O。回答下列問題:△
(1)實驗室制取Cl2的反應(yīng)中,濃鹽酸表現(xiàn)(填“氧化性”、“還原性”或“酸性”)。
(2)請用單線橋表示該反應(yīng)中電子轉(zhuǎn)移的方向和數(shù)目。
(3)標(biāo)況下,若生成5.6LCl2,則轉(zhuǎn)移電子的數(shù)目為。
(4)裝置C可吸收多余的Cl2,生成NaCl和NaClO,寫出離子方程式。所用NaOH溶液一般為5.0mol/L,用NaOH固體配制100mL該溶液,需要用到的儀器有托盤天平、燒杯、玻璃棒、膠頭滴管、。
(5)ClO-有強氧化性,某實驗小組為探究ClO-、I2、在酸性條件下的氧化性強弱,設(shè)計實驗如下:SO2-4
實驗①:在淀粉碘化鉀溶液中加入少量次氯酸鈉溶液,并加入少量的稀硫酸,溶液立即變藍;
實驗②:向?qū)嶒灑俚娜芤褐屑尤肷倭縼喠蛩徕c溶液,藍色又褪去。
以上實驗說明,在酸性條件下ClO-、I2、的氧化性由弱到強的順序是SO2-4。
(6)裝置C中也可能生成NaClO3,NaClO3和濃鹽酸也可以制備Cl2,試寫出離子方程式。組卷:20引用:1難度:0.6 -
21.氯化鈉是生活必需品,也是重要的化工原料。提純粗鹽一般經(jīng)過如圖操作流程;
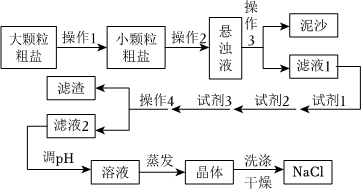
查閱相關(guān)資料得知:粗鹽中除含泥沙等不溶性雜質(zhì)外,還含有少量的MgCl2、CaCl2、Na2SO4等可溶性雜質(zhì)。
回答下列問題:
(1)操作1必須要用到研缽,操作1是,操作2和操作3均能用到玻璃棒,玻璃棒的作用分別是、。
(2)若試劑1是NaOH溶液,則試劑2和試劑3分別是、。
(3)濾液2中除含有Na+和Cl-外,還含有(不考慮水的電離)。
(4)某同學(xué)對調(diào)節(jié)pH后所得溶液中是否存在還存在疑問,請你設(shè)計實驗檢驗SO2-4是否存在:SO2-4。
(5)實驗結(jié)束后稱量獲得的“NaCl”,并計算“NaCl”的制得率,發(fā)現(xiàn)制得率偏高,其可能原因是(填序號)。
A.粗鹽沒有全部溶解即過濾
B.蒸發(fā)時液滴飛濺劇烈
C.調(diào)pH時,pH值偏大
D.蒸發(fā)皿上粘有的“NaCl”沒有全部轉(zhuǎn)移到稱量紙上組卷:6引用:1難度:0.5


