2023年黑龍江省大慶三十六中中考化學模擬試卷
發布:2024/4/20 14:35:0
一、選擇題(每題只有一個選項,每題4分,共40分)
-
1.下列物質的用途中,利用其化學性質的是( )
A.金剛石用于切割玻璃 B.鐵粉用作食品保鮮吸氧劑 C.液氮用作冷凍劑 D.銅用于制作導線 組卷:29引用:3難度:0.9 -
2.下列圖示的實驗操作中正確的是( )
A. 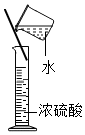
濃硫酸稀釋B. 
聞氣體氣味C. 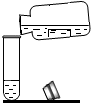
液體的傾倒D. 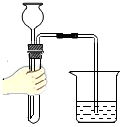
檢查氣密性組卷:216引用:16難度:0.5 -
3.下列實驗不能達到實驗目的的是( )
A. 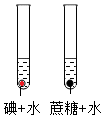
利用甲實驗比較不同物質在同種溶劑中的溶解性B. 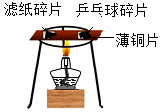
利用乙實驗探究可燃物燃燒所需的溫度應達到著火點C. 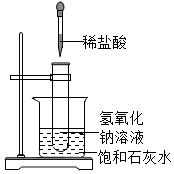
利用丙實驗驗證稀鹽酸和氫氧化鈉溶液反應放熱D. 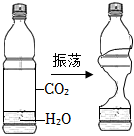
利用丁實驗證明二氧化碳能與水發生反應組卷:30引用:1難度:0.5 -
4.下列化學方程式與事實相符且正確的是( )
A.檢驗硫酸鈉中是否含有氯化鈉:NaCl+AgNO3═NaNO3+AgCl↓ B.用稀硫酸可以除鐵銹:FeO+H2SO4═FeSO4+H2O C.碳酸鈣用做補鈣劑:CaCO3+2HCl═CaCl2+H2O+CO2↑ D.天然氣可以用作燃料:CH4+2O2═CO2+2H2O 組卷:23引用:1難度:0.6 -
5.“何以解憂,唯有杜康”就是對我省杜康酒的贊美。“酒越陳越香醇”是指酒在存放過程中可生成有香味的乙酸乙酯(C4H8O2),下列有關乙酸乙酯的說法正確的是( )
A.乙酸乙酯的相對分子質量為(12×4+1×8+16×2)g B.乙酸乙酯由4個碳原子、8個氫原子和2個氧原子構成 C.生成乙酸乙酯的過程中原子的種類、數目均未發生改變 D.乙酸乙酯中碳元素的質量分數= ×100%1229組卷:81引用:4難度:0.6 -
6.下列除去物質中少量的雜質,所選用的試劑和主要操作方法都正確的是( )
物質(括號內為雜質) 所用試劑和主要操作方法 A ZnCl2溶液(CuCl2) 加入足量的鐵粉后過濾 B 銅粉(木炭) 在空氣中灼燒 C CO2(CO) 通入過量的氧氣后點燃 D KCl(MnO2) 加水充分溶解后過濾,蒸發結晶 A.A B.B C.C D.D 組卷:230引用:7難度:0.5
三、實驗探究
-
18.食鹽、碳酸鈉和碳酸氫鈉是生活中常見的鈉鹽。請回答下列問題。
(1)碳酸氫鈉的水溶液顯性(填“酸”、“堿”或“中”)。碳酸氫鈣受熱易分解,碳酸氫鈉性質與其相似。除去碳酸鈉固體中混有的少量碳酸氫鈉,反應的化學方程式為;
(2)等質量的碳酸鈉和碳酸氫鈉分別與足量鹽酸反應時生成的CO2質量,前者后者(填“>”、“<”或“=”);
(3)粗鹽含有少量雜質(主要為CaCl2、MgCl2、Na2SO4等)。用粗鹽制取“化學純”級的NaCl,步驟為溶解、加過量a、加過量NaOH、加過量b、過濾、加適量鹽酸,蒸發結晶得到“化學純”級的NaCl固體。
①試劑a、b分別是(填序號);
A.Na2CO3、BaCl2
B.BaCl2、Na2CO3
C.BaCl2、Na2SO4
②加過量NaOH的目的是;
③加適量鹽酸的目的是;
④蒸發結晶時,玻璃棒的作用是。
(4)工業上用電解飽和食鹽水的方法生產氯氣和燒堿。
資料一:Cl2+H2O═HCl+HClO
資料二:初中化學中,我們學習了酸和堿發生中和反應的實質是H++OH-═H2O。像這種用實際參加反應的離子符號來表示反應的式子叫離子方程式。離子方程式的書寫一般按以下步驟:(以Na2SO4與BaCl2反應為例)
第一步:寫出Na2SO4與BaCl2反應的化學方程式;
第二步:把易溶于水、易電解的物質寫成離子形式,把難溶的物質、氣體和水等仍用化學式表示。上述化學方程式可改寫成:2Na+++Ba2++2Cl-═BaSO4↓+2Na++2Cl-;SO2-4
第三步:刪去方程式兩邊不參加反應的離子:Ba2++═BaSO4↓;SO2-4
第四步:檢查方程式兩邊各元素的原子個數和電荷總數是否相等。
①寫出Na2CO3與稀鹽酸反應的離子方程式:;
②某化工廠發生氯氣泄漏事件,工作人員噴射NaOH溶液形成液幕,包圍并吸收泄漏的氯氣,其反應原理(用離子方程式表示);
資料三:化學反應類型有不同的分法,其中反應前后,有元素化合價變化的化學反應是氧化還原反應。氧化還原反應中有元素化合價升高的反應物是還原劑,有元素化合價降低的反應物是氧化劑,化合價沒有變化的反應物既不是氧化劑也不是還原劑。
③工業上可用氨檢驗輸送氯氣的管道是否漏氣。反應化學方程式如下:8NH3+3C12═6NH4Cl+N2。該反應(填“是”或“不是”)氧化還原反應,其中氧化劑和還原劑的質量比為(若是氧化還原反應,此空作答,反之,不作答)。組卷:149引用:1難度:0.5
四.計算題(8分)
-
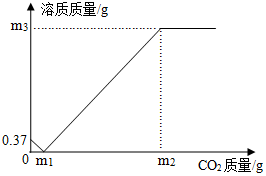 19.某化學興趣小組取9.87g部分變質的熟石灰樣品放入大燒杯中,加入255.51g水,充分攪拌至熟石灰全部溶解后,通入足量的CO2,溶質質量與反應的CO2質量的關系如圖所示,求通入m2g CO2時所得溶液的溶質質量分數。
19.某化學興趣小組取9.87g部分變質的熟石灰樣品放入大燒杯中,加入255.51g水,充分攪拌至熟石灰全部溶解后,通入足量的CO2,溶質質量與反應的CO2質量的關系如圖所示,求通入m2g CO2時所得溶液的溶質質量分數。
[提示:CaCO3+H2O+CO2=Ca(HCO3)2]組卷:155引用:3難度:0.1


