2013-2014學年山東省日照一中高二(上)模塊化學試卷
發布:2024/4/20 14:35:0
一、(本題包括25小題,每小題2分,共50分,每小題只有一個選項符合題意)
-
1.對于反應中的能量變化,表述正確的是( )
A.物質發生化學反應時一定都伴隨著能量變化 B.斷開化學鍵的過程會放出能量 C.加熱才能發生的反應一定是吸熱反應 D.等質量的硫蒸氣和硫固體分別完全燃燒,后者放出的熱量多 組卷:5引用:4難度:0.9 -
2.在2A+B?3C+4D反應中,表示該反應速率最快的是( )
A.υ(A)=0.5 mol/(L?s) B.υ(B)=1 mol/(L?s) C.υ(C)=0.8 mol/(L?s) D.υ(D)=0.3 mol/(L?s) 組卷:60引用:28難度:0.9 -
3.將盛有NH4HCO3粉末的小燒杯放入盛有少量醋酸的大燒杯中.然后向小燒杯中加入鹽酸,反應劇烈,醋酸逐漸凝固.由此可見( )
A.NH4HCO3和鹽酸的反應是放熱反應 B.該反應中,熱能轉化為產物內部的能量 C.反應物的總能量高于生成物的總能量 D.反應的熱化學方程式為:NH4HCO3+HCl=NH4Cl+CO2↑+H2O△H=-Q kJ/mol(Q>0) 組卷:30引用:7難度:0.9 -
4.下列說法正確的是( )
A.原電池的負極、電解池的陽極都發生氧化反應 B.原電池中,溶液中的陰離子移向正極 C.雙液原電池中的鹽橋是為了聯通電路,所以也可以用金屬導線代替 D.電解時電解池的陽極一定是陰離子放電 組卷:4引用:2難度:0.9 -
 5.某反應的反應過程中能量變化如圖所示(圖中E1表示正反應的活化能,E2表示逆反應的活化能)。下列有關敘述正確的是( )
5.某反應的反應過程中能量變化如圖所示(圖中E1表示正反應的活化能,E2表示逆反應的活化能)。下列有關敘述正確的是( )A.該反應為吸熱反應 B.催化劑能改變反應的焓變 C.催化劑能降低反應的活化能 D.逆反應的活化能大于正反應的活化能 組卷:356引用:94難度:0.9 -
6.下列事實不能用化學平衡移動原理解釋的是( )
A.合成氨工業中采用高壓條件 B.由H2、I2蒸氣、HI組成的平衡體系加壓后顏色變深 C.用排飽和食鹽水的方法收集Cl2 D.在含有[Fe(SCN)]2+的紅色溶液中加鐵粉,振蕩靜置,溶液顏色變淺或褪去 組卷:10引用:3難度:0.9 -
7.用鐵片與稀硫酸反應制取氫氣時,下列措施不能使氫氣生成速率加大的是( )
A.加入少量較濃的硫酸 B.加入幾滴CuSO4溶液 C.加入CH3COONa固體 D.不用鐵片,改用鐵粉 組卷:5引用:2難度:0.9 -
8.密閉容器中有如下反應:mA(g)+nB(g)?pC(g)達到平衡后,保持溫度不變,將容器體積縮小到原來的
,當達到新平衡時,C的濃度為原來的1.8倍.下列說法中正確的是( )12A.m+n>p B.A的轉化率降低 C.平衡向正反應方向移動 D.C的質量分數增加 組卷:31引用:9難度:0.7 -
9.下列關于鹽酸與醋酸兩種稀溶液的說法正確的是( )
A.相同濃度的兩溶液中c(H+)相同 B.100 mL 0.1 mol?L-1的兩溶液能中和等物質的量的氫氧化鈉 C.pH=3的兩溶液稀釋100倍,pH都為5 D.兩溶液中分別加入少量對應的鈉鹽固體,c(H+)均明顯減小 組卷:1876引用:21難度:0.9
二、(本題包括4小題,共50分)
-
28.鋁和硫的單質及其化合物在工農業生產和生活中有重要的作用.
(1)真空碳熱還原-氯化法可實現由鋁礦制備金屬鋁,其相關的熱化學方程式如下:
2Al2O3(s)+2AlCl3(g)+6C(s)=6AlCl(g)+6CO(g)△H=a kJ?mol-1
3AlCl(g)=2Al(l)+AlCl3(g)△H=b kJ?mol-1
反應Al2O3(s)+3C(s)=2Al(l)+3CO(g)的△H=kJ?mol-1(用含a、b的代數式表示);
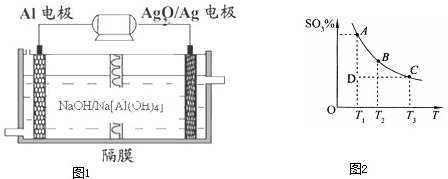
(2)鋁電池性能優越,Al-Ag2O電池可用作水下動力電源,其原理如圖1所示:
請寫出該電池正極反應式;常溫下,用該化學電源和惰性電極電解300mlNaCl溶液(過量),陽極的電極反應式為,電解反應的離子方程式為,消耗27mg Al后溶液的pH=(不考慮溶液體積的變化).
(3)硫酸的年產量可以用來衡量一個國家的無機化工水平.工業生產硫酸的流程中存在反應:2SO2(g)+O2(g)?2SO3(g).反應體系中SO3的百分含量和溫度的關系如圖2所示(曲線上任何一點都表示平衡狀態).下列說法正確的是
a.若在恒溫、恒壓條件下向上述平衡體系中通入氦氣,平衡不移動
b.若在恒溫、恒容條件下向上述平衡體系中通入SO3(g),壓強增大,平衡向右移動
c.B點、C點反應的平衡常數分別為K1、K2,則K1<K2
d.在A點時,消耗1mol SO2必定同時消耗1mol SO3
e.在D點時,v正>v逆.組卷:11引用:1難度:0.5 -
29.(1)25℃時,將pH=5的硫酸溶液稀釋500倍,稀釋后溶液中的[SO42-]:[H+]約為
(2)25℃時,某強酸溶液pH=a,某強堿溶液pH=b,已知a+b=12,酸堿溶液混合后pH=7,則酸溶液體積V(酸)和堿溶液體積V(堿)的正確關系為
(3)25℃時,pH=3的鹽酸中水電離的H+的濃度為mol?L-1
(4)某溫度(t℃)時,測得0.01mol?L-1 的NaOH溶液的pH=11,則該溫度下水的Kw=在此溫度下某溶液的pH=3,在該溶液中[H+]:[OH-]=.
(5)純水中[H+]=5.0×10-7 mol/L,則此時純水中的[OH-]=.組卷:46引用:1難度:0.1


