2013-2014學年江蘇省常州市金壇市建昌中學九年級(上)化學周末作業(2)
發布:2024/4/20 14:35:0
一、選擇題(共20小題,每小題2分,滿分40分)
-
1.下列變化中,屬于物理變化的是( )
A. 
B. 
C. 
D.  組卷:1引用:1難度:0.9
組卷:1引用:1難度:0.9 -
2.下列屬于化學性質的是( )
A.溶解性 B.揮發性 C.金屬活動性 D.導電性 組卷:6引用:1難度:0.9 -
3.下列物質屬于純凈物的是( )
A.醫用酒精 B.干冰 C.清新空氣 D.加碘食鹽 組卷:60引用:44難度:0.9 -
4.下列基本實驗操作中正確的是( )
A. 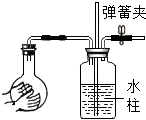
檢查氣密性B. 
滴加試劑C. 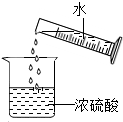
稀釋濃硫酸D. 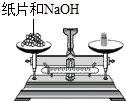
稱量NaOH固體組卷:28引用:8難度:0.9 -
5.下列說法錯誤的是( )
選項 甲 乙 A 常見堿 燒堿、熟石灰、氨水 B 常見合金 生鐵、不銹鋼、黃銅 C 常見有機高分子材料 合金、合成橡膠、合成纖維 D 常見營養物質 蛋白質、維生素、脂肪 A.A B.B C.C D.D 組卷:11引用:4難度:0.9 -
6.在“綠色化學”工藝中,理想狀態是反應物中的原子全部轉化為欲得到的產物,即原子的利用率為100%,從根本上減少乃至杜絕污染.下列做法符合“綠色化學”的是( )
A.農民就地焚燒秸稈 B.深埋含鎘、汞的廢舊電池 C.工業制酒精:C2H4+H2O C2H5OH催化劑D.化工生產中的廢氣向高空排放 組卷:30引用:19難度:0.9 -
7.下圖表示治理汽車尾氣所涉及反應的微觀過程。下列說法不正確的是( )
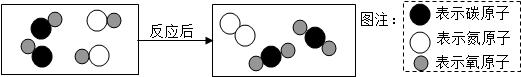
A.該反應的本質是原子的重新組合 B.反應后分子個數發生了改變 C.圖中所示單質是空氣中含量最多的氣體 D.生成單質與化合物的質量比為7:11 組卷:23引用:4難度:0.9 -
8.下列說法錯誤的是( )
A.用碘酒可區別加碘食鹽和無碘食鹽 B.用水能區分NH4NO3和NaOH固體 C.用灼燒的方法能區別棉花和羊毛 D.用飽和硫酸銨溶液能區分淀粉和蛋白質溶液 組卷:6引用:2難度:0.9 -
9.下列實驗數據或現象合理的是( )
①用托盤天平稱取15.6g氧化銅粉末; ②用廣泛pH試紙測得某溶液的pH為3.52;
③鐵絲在空氣中燃燒,火星四射; ④用10mL量筒量取某溶液6.6mL.A.①②③④ B.②③④ C.③④ D.①④ 組卷:84引用:7難度:0.9 -
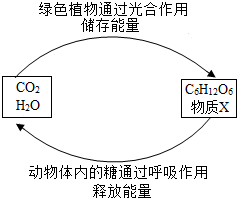 10.如圖是兩組物質之間在一定的條件下相互轉化的過程.下列說法錯誤的是( )
10.如圖是兩組物質之間在一定的條件下相互轉化的過程.下列說法錯誤的是( )A.物質X是O2 B.綠色植物通過光合作用,將太陽能轉化成化學能 C.人體中氧化產生的CO2如不及時排出,則血液的pH將減小 D.C6H12O6與X反應生成CO2和H2O屬于置換反應 組卷:10引用:2難度:0.7
五、推斷題(本題包括2小題,共13分)
-
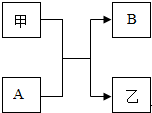 31.已知A與B,甲與乙均為初中化學常見的物質,其轉化關系如圖所示。
31.已知A與B,甲與乙均為初中化學常見的物質,其轉化關系如圖所示。
(1)若甲為氧氣,則A的化學式為;該化學反應的方程式是。
(2)若甲是一種紅色的氧化物,乙的溶液呈黃色,則反應的化學方程式為。
(3)若甲、乙是常見的堿,A,B是常見的鹽,而且當甲轉化為B,乙轉化為A時,都是與同一種氣體X發生反應。
①則氣體X的化學式是;A的化學式為;
②甲轉化為B的化學方程式為。
(4)若甲和A發生中和反應,而且當甲轉化為B,乙轉化為A時,都是與同一物質Y發生反應,則Y的化學式為,此中和反應的化學方程式為。組卷:25引用:4難度:0.1
六、綜合題(本題1小題,共15分)
-
32.用作牙膏摩擦劑的輕質碳酸鈣可以用礦石A來制備,某化學興趣小組設計了2種轉化流程,如圖所示。
【生產流程】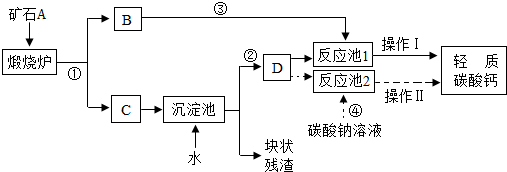
【相關資料】
a.二氧化碳持續通入氫氧化鈣溶液發生如下反應:
CO2+Ca(OH)2=CaCO3↓+H2O,CaCO3+H2O+CO2=Ca(HCO3)2;
b.碳酸氫鈣微溶于水,微熱易分解:Ca(HCO3)2CaCO3↓+H2O+CO2↑;加熱
c.生石灰與水充分反應后可得到顆粒非常細小的熟石灰漿。
【問題討論】
(1)小王主張用流程①、②、④和操作Ⅱ的設計。請寫出反應①和④的化學方程式:①;④;操作Ⅱ包括攪拌和、洗滌、烘干等工序;該流程中,通過反應④可回收副產品。
(2)小李認為流程①、②、③和操作I比小王的主張更好,理由是:;
(3)制輕質碳酸鈣時,D為(選填“懸濁液”或“溶液”),理由是:。
(4)小李認為得到的產品中可能含有雜質Ca(HCO3)2,所以操作Ⅰ包括攪拌、和過濾、烘干等工序,以提高產率。
【產品含量測定】CaCO3含量的測定:取20.0g產品,研成粉狀后,按圖進行實驗。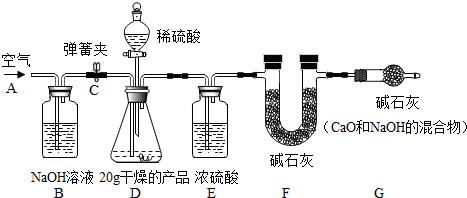
(5)實驗步驟:
①連接好裝置,檢查氣密性; ②打開彈簧夾C,在A處緩緩通入一段時間空氣;
③稱量F的質量; ④關閉彈簧夾C,慢慢滴加稀硫酸至過量,直至D中無氣泡冒出;
⑤打開彈簧夾C,再次緩緩通一段時間空氣;⑥稱量F的質量,得前后兩次質量差為8.7g。
(6)問題探究
①產品研成粉的目的;
②B裝置的作用是;G裝置的作用是,
③若沒有E裝置,則測定的CaCO3的質量分數會(填“偏大”、“偏小”、“不變”)。
稱量F的質量,得前后兩次質量差為8.7g,可求得產品中CaCO3的質量分數為%。
【總結反思】
某同學設計上述實驗方案測定牙膏中鈣元素的質量分數:向一定量牙膏中加入過量稀鹽酸,測定生成CO2的質量,據此計算牙膏中鈣元素的質量分數。小李同學認為即使排除實驗儀器和操作的影響,上述測定的結果仍不一定準確,理由是。組卷:222引用:24難度:0.3


