2018-2019學年湖南省長沙市雅禮實驗中學九年級(下)入學化學試卷
發布:2024/4/20 14:35:0
一、選擇題(本大題包括15個小題,每小題3分,共45分)
-
1.下列變化中,屬于化學變化的是( )
A.干冰升華 B.濃鹽酸揮發 C.木材燃燒 D.活性炭吸附 組卷:9引用:1難度:0.5 -
2.下列實驗操作中,不正確的是( )
A. 
聞醋酸氣味B. 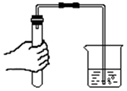
檢查氣密性C. 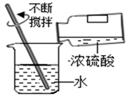
稀釋濃硫酸D. 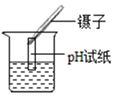
測定溶液pH組卷:5引用:1難度:0.7 -
3.空氣是一種寶貴的資源,下列有關空氣成分的用途與對應性質說法不正確的是( )
A.O2的化學性質比較活潑,可以做火箭發射的助燃劑 B.氮氣化學性質穩定,可用作防腐氣 C.稀有氣體化學性質穩定,可用作電光源 D.二氧化碳能參與光合作用,可用作氣體肥料 組卷:7引用:1難度:0.9 -
4.下列關于化學反應現象的描述正確的是( )
A.紅磷在空氣中燃燒,放熱,產生大量的白色煙霧 B.碳在空氣中不充分燃燒,生成一氧化碳 C.鐵絲在氧氣中燃燒,放熱,發出耀眼的白光 D.銅片在空氣中加熱,固體由紅色變成黑色 組卷:7引用:1難度:0.6 -
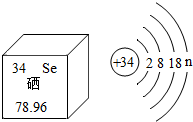 5.亞硒酸鈉(Na2SeO3)可用于提升人體免疫力,硒元素在元素周期表中的部分信息及原子結構示意圖如圖所示,下列說法正確的是( )
5.亞硒酸鈉(Na2SeO3)可用于提升人體免疫力,硒元素在元素周期表中的部分信息及原子結構示意圖如圖所示,下列說法正確的是( )A.Na2SeO3中Se的化合價為+1 B.Se是一種非金屬元素 C.n的值為4 D.Se相對原子質量為78.96g 組卷:5引用:1難度:0.6 -
6.運用“天宮一號”的是“長征二號F-T1”運載火箭,火箭的主要燃料是偏二甲肼(化學式為C2H8N2)。下列有關偏二甲肼組成與結構的敘述,不正確的是( )
A.偏二甲肼由2個碳原子、8個氫氣原子、2氮原子構成 B.偏二甲肼由碳、氫、氮三種元素組成 C.偏二甲肼是化合物 D.偏二甲肼中碳、氫、氮元素的質量比為6:2:7 組卷:6引用:1難度:0.6 -
7.宏觀辨識與微觀探析是化學學科的核心素養。下列說法不正確的是( )
A.花香四溢,是因為分子在不斷運動 B.大多數物體受熱時體積增大,是因為受熱時分子體積增大 C.水電解產生氫氣和氧氣,說明化學變化中分子可分,原子不可分 D.水與酒精混合后體積小于混合前二者體積之和,是因為分子間有間隔 組卷:4引用:1難度:0.5 -
8.下列物質中,前者是單質、后者是混合物的是( )
A.干冰、石油 B.水、啤酒 C.水銀、澄清的石灰水 D.氫氣、氯化鈉 組卷:7引用:1難度:0.9
四、探究題(本大題共2個小題,每空2分,共18分)
-
23.甲、乙兩個化學興趣小組分別利用實驗桌上的氫氧化鈉溶液和稀鹽酸進行實驗。甲組同學將一定量稀鹽酸滴入氫氧化鈉溶液中,未能觀察到明顯現象,于是進行了如下探究:
實驗一:探究氫氧化鈉和稀鹽酸是否能發生反應。
(1)現象A為:序號 實驗操作 實驗現象 實驗結論 1 取滴加稀鹽酸后的溶液樣品于試管中,滴加酚酞溶液 溶液變紅色 氫氧化鈉與稀鹽酸不反應 2 取滴加稀鹽酸后的溶液樣品于試管中,加入鋅粒 現象A 氫氧化鈉與稀鹽酸發生反應 。
(2)對于不同的實驗結果,小組經討論認為實驗(填“1”或“2”)不嚴謹,理由是:。
乙組同學將稀鹽酸滴入另一份未蓋好瓶塞的氫氧化鈉溶液中實驗時,觀察到有氣泡產生這一反常現象,他們得出該氫氧化鈉已變質。
實驗二:測定該氫氧化鈉溶液中碳酸鈉的質量分數。
他們在老師的幫助下設計了如圖裝置進行實驗。實驗中樣品質量為M克,最后測得實驗后C瓶質量增加了N克,根據M、N,可計算得出該樣品中碳酸鈉的質量分數。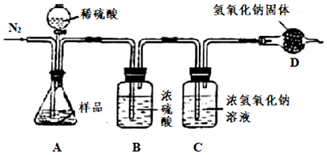
分析:
(3)氫氧化鈉溶液在空氣中變質的原因是。
(4)若沒有B裝置,則測出的碳酸鈉質量分數將(填“偏大”、“偏小”或“不變”)。
(5)實驗中,待A中反應結束后,需通入充足氮氣,該操作的目的是。組卷:35引用:1難度:0.4
五、計算題(本題共1小題,共6分)
-
24.科幻電影《流浪地球》中,人類利用氫氣與氧氣燃燒的反應拯救了地球。模擬該情景,在密閉容器中充入20g氫氣與氧氣的混合氣體,點燃,待充分反應后,測得剩余氣體2g。請回答:
(1)反應生成水的質量為。
(2)求出反應中消耗氧氣的質量。組卷:17引用:1難度:0.5


