《第3章 水溶液中的離子平衡》2012年單元測試卷
發布:2024/4/20 14:35:0
一、選擇題
-
1.下列按純凈物、混合物、電解質和非電解質順序排列的是( )
A.鹽酸、空氣、醋酸、干冰 B.冰醋酸、福爾馬林、硫酸鈉、乙醇 C.蛋白質、油脂、苛性鉀、石灰石 D.膽礬、漂白粉、氯化鉀、硫酸鋇 組卷:218引用:11難度:0.9 -
2.c(H+)相同的等體積的兩份溶液A和B;A為鹽酸,B為醋酸,分別和鋅反應,若最后僅有一份溶液中存在鋅,且放出的氫氣的質量相等,則下列說法正確的是( )
①反應所需要的時間B>A
②開始反應時的速率A>B
③參加反應的鋅的物質的量A=B
④反應過程的平均速率B>A
⑤鹽酸里有鋅剩余
⑥醋酸里有鋅剩余.A.③④⑤ B.③④⑥ C.②③⑤ D.②③⑤⑥ 組卷:111引用:24難度:0.7 -
3.一定量的鋅粉和6mol?L-1的過量鹽酸反應,當向其中加入少量的下列物質時,一定能夠加快反應速率,又不影響產生H2總量的是( )
①石墨 ②CuO ③銅粉 ④鐵粉 ⑤濃鹽酸 ⑥無水乙酸.A.①③④ B.②④⑥ C.②⑤⑥ D.①③⑤⑥ 組卷:36引用:7難度:0.7 -
4.下列物質中屬于強電解質的是(
A.NH3?H2O B.Cu C.飽和食鹽水 D.醋酸銨 組卷:25引用:3難度:0.9 -
5.下列事實不能用勒夏特列原理解釋的是( )
A.棕紅色NO2加壓后顏色先變深后變淺 B.鋼鐵在潮濕的空氣中容易生銹 C.實驗室可用排飽和食鹽水的方法收集氯氣 D.常溫下,將1mLpH=3的醋酸溶液加水稀釋至100mL,測得其pH<5 組卷:30引用:7難度:0.9 -
6.下列說法中正確的是( )
A.在Na3PO4溶液中,c(Na+) 是c( )的3倍PO3-4B.pH=3的鹽酸中,其c(H+)是pH=1的鹽酸的3倍 C.0.1mol/L KOH溶液和0.1mol/L氨水中,其c(OH-)相等 D.在25℃時,無論是酸性、堿性還是中性溶液中,其c(H+)和c(OH-)的乘積都等于10-14 組卷:52引用:1難度:0.9 -
7.25℃時,水的電離達到平衡:H2O?H++OH-ΔH>0,下列敘述正確的是( )
A.向水中加入氨水,平衡逆向移動,c(OH-)降低 B.向水中加入少量固體硫酸氫鈉,c(H+)增大,KW不變 C.向水中加入少量固體CH3COONa,平衡逆向移動,c(H+)降低 D.將水加熱,KW增大,pH不變 組卷:1185引用:173難度:0.9 -
8.常溫下,下列各組離子一定能大量共存的是( )
A.滴加甲基橙試劑顯紅色的溶液中:Na+、Fe2+、Cl-、 NO-3B.c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- C.c(OH-)/c(H+)=1012的溶液中: 、Al3+、NH+4、NO-3CO2-3D.由水電離的c(H+)=1.0×10-13 mol?L-1的溶液中:K+、 、NH+4、AlO-2HCO-3組卷:41引用:14難度:0.7 -
9.對于0.1mol?L-1 Na2SO3溶液,正確的是( )
A.升高溫度,溶液的pH降低 B.c(Na+)=2c( )+c(SO2-3)+c(H2SO3)HSO-3C.c(Na+)+c(H+)=2c( )+c(SO2-3)+c(OH-)HSO-3D.加入少量NaOH固體,c( )與c(Na+)均增大SO2-3組卷:109引用:51難度:0.5 -
10.25℃時,在等體積的①pH=0的H2SO4溶液、②0.05mol?L-1的Ba(OH)2溶液、③pH=10的Na2S溶液、④pH=5的NH4NO3溶液中,發生電離的水的物質的量之比是( )
A.1:10:1010:109 B.1:5:5×109:5×108 C.1:20:1010:109 D.1:10:104:109 組卷:508引用:65難度:0.7 -
11.能促進水的電離,并使溶液中c(H+)>c(OH-)的操作是( )
①將水加熱煮沸
②向水中投入一小塊金屬鈉
③向水中通CO2
④向水中通NH3
⑤向水中加入明礬晶體
⑥向水中加入NaHCO3固體
⑦向水中加NaHSO4固體。A.①③⑥⑦ B.①③⑤⑥ C.⑤⑦ D.⑤ 組卷:49引用:10難度:0.7 -
12.下列敘述正確的是( )
A.某醋酸溶液的pH=a,將此溶液稀釋1倍后,溶液的pH=b,則a>b B.在滴有酚酞溶液的氨水中,加入NH4Cl的溶液恰好無色,則此時溶液pH<7 C.常溫下,1.0×10-3mol/L鹽酸的pH=3.0,1.0×10-8mol/L鹽酸pH=8.0 D.若1mLpH=1鹽酸與100mLNaOH溶液混合后,溶液pH=7,則NaOH溶液的pH=11 組卷:670引用:22難度:0.7 -
13.下列說法正確的是( )
A.25℃時,NH4Cl溶液的KW大于100℃時NH4Cl溶液的KW B.25℃時,向10mL pH=3的醋酸溶液中加入水稀釋后,溶液中 不變c(CH3COO-)c(CH3COOOH)?c(OH-)C.25℃時,pH=12的氨水和pH=2的鹽酸溶液等體積混合,c(Cl-)>c(NH4+)>c(H+)>c(OH-) D.100℃時,將pH=2的鹽酸與pH=12的NaOH溶液等體積混合,溶液顯中性 組卷:41引用:3難度:0.7 -
14.下列事實一定能說明HF是弱酸的是( )
①常溫下NaF溶液的pH大于7;
②用HF溶液做導電性實驗,燈泡很暗;
③HF與NaCl不能發生反應;
④常溫下0.1mol/L的HF溶液的pH為2.3;
⑤HF能與Na2CO3溶液反應,產生CO2氣體;
⑥HF與水能以任意比混溶;
⑦1mol/L的HF水溶液能使紫色石蕊試液變紅.A.①②⑦ B.②③⑤ C.③④⑥ D.①④ 組卷:328引用:38難度:0.9 -
15.下列實驗方法、結論合理的是( )
A.增加反應物的用量,化學反應速率一定加快 B.AgCl在同濃度的CaCl2和NaCl溶液中的溶解度相同 C.pH相同的兩種一元酸HA溶液和HB溶液與足量Zn反應,HA比HB反應速率快,說明HA酸性更強 D.將碳酸鈉溶液和碳酸氫鈉溶液分別蒸干并灼燒,所得固體的成分均為碳酸鈉 組卷:11引用:2難度:0.5 -
16.下列物質中屬于強電解質的是( )
A.NH3?H2O B.H2O C.CH3COOH D.醋酸銨 組卷:52引用:3難度:0.9 -
17.下列電離方程式中書寫正確的是( )
A.NaHSO4?Na++H++SO42- B.NaHCO3?Na++H++CO32- C.HClO=H++ClO- D.H2S?H++HS-;HS-?H++S2- 組卷:152引用:13難度:0.9
二、非選擇題
-
52.現有甲、乙兩種溶液:
甲 pH=2(c(H+)=10-2 mol/L)的醋酸溶液
乙 pH=2(c(H+)=10-2 mol/L)的鹽酸
請根據下列操作回答問題:
(1)取10mL的甲溶液,加入等體積的水,醋酸的電離平衡移動(填“向左”、“向右”或“不”);另取10mL的甲溶液,加入少量無水醋酸鈉固體(假設加入固體前后,溶液體積保持不變),待固體溶解后,溶液中c(H+)/c(CH3COOH)的比值將(填“增大”、“減小”或“無法確定”).
(2)相同條件下,取等體積的甲、乙兩溶液,各稀釋100倍.稀釋后的溶液,其溶液中大小關系為:c(H+)(甲)c(H+)(乙)(填“大于”、“小于”或“等于”).
(3)各取25mL的甲、乙兩溶液,分別用等濃度的NaOH稀溶液中和,則消耗的NaOH溶液的體積大小關系為:V(甲)V(乙)(填“大于”、“小于”或“等于”).
(4)下列事實能證明乙酸(CH3COOH)是弱電解質的是
A.用乙酸(CH3COOH)溶液做導電性試驗燈光較暗 B.乙酸(CH3COOH)是共價化合物
C.常溫下,0.1mol/L乙酸(CH3COOH)溶液的pH為2.2 D.乙酸(CH3COOH)溶液不與NaCl反應.組卷:46引用:1難度:0.5 -
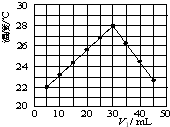 53.某研究小組將V1 mL 1.0mol/L HCl溶液和V2 mL未知濃度的NaOH溶液混合均勻后測量并記錄溶液溫度,實驗結果如圖所示(實驗中始終保持V1+V2=50mL).回答下列問題:
53.某研究小組將V1 mL 1.0mol/L HCl溶液和V2 mL未知濃度的NaOH溶液混合均勻后測量并記錄溶液溫度,實驗結果如圖所示(實驗中始終保持V1+V2=50mL).回答下列問題:
(1)研究小組做該實驗時環境溫度(填“高于”、“低于”或“等于”)22℃,判斷的依據是.
(2)由題干及圖形可知,V1:V2=時,酸堿恰好完全中和,此反應所用NaOH溶液的濃度應為mol/L.
(3)實驗時將酸堿在簡易量熱計中混合,并用攪拌,使溶液混合均勻.經有關計算知此反應共放出Q kJ的熱量,請寫出此反應的熱化學方程式:.組卷:22引用:4難度:0.3


