2022-2023學年重慶市巴蜀中學高三(上)月考化學試卷(四)
發布:2024/11/20 6:30:2
一、選擇題:本題共14小題,每小題3分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.2022年10月31日中國空間站的新成員夢天實驗艙發射成功,航天科技的發展與化學密切相關,下列說法正確的是( )
A.中國天眼FAST用到的高性能碳化硅是一種新型的有機材料 B.“天宮號”空間站使用的太陽能電池帆板的主要成分是二氧化硅 C.“長征五號”運載火箭用液氧液氫推進劑,產物對環境無污染 D.天和核心艙的霍爾發動機燃料 Xe原子核含131個中子13154組卷:11引用:1難度:0.7 -
2.性質決定用途,下列物質的性質與用途正確且具有對應關系的是( )
A.二氧化硫具有漂白性,可用于紅酒殺菌消毒 B.鐵和濃硫酸常溫下不反應,可以用鐵罐盛裝濃硫酸 C.過氧化鈉是淡黃色固體,在呼吸面具中用作供氧劑 D.二氧化硅導光能力強,并且有硬度和柔韌度,可作光導纖維 組卷:4引用:1難度:0.6 -
3.用NA、表示阿伏加德羅常數的值,下列說法正確的是( )
A.反應3H2(g)+N2(g)?2NH3(g)ΔH=-92kJ?mol-1,當放出熱量46kJ時,轉移電子數為3NA B.0.1mol?L-1Na2CO3溶液中,若Na+的數目為NA,則CO32-和HCO3-的總數為0.5NA C.1mol水蒸氣分子間氫鍵的數目為2NA D.78g苯中含有碳碳雙鍵的數目為3NA 組卷:6引用:1難度:0.6 -
4.下列實驗裝置不能達到實驗目的的是( )
A. 
實驗室制取氨氣B. 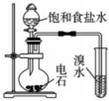
證明乙炔可使溴水褪色C. 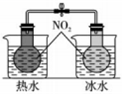
用裝置證明溫度對化學平衡的影響D. 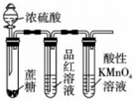
用裝置驗證濃硫酸具有脫水性、強氧化性,SO2具有漂白性、還原性組卷:3引用:1難度:0.5 -
5.下列有關離子方程式不正確的是( )
A.酸性高錳酸鉀滴定過氧化氫:2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O B.海水提溴中用SO2水溶液富集溴:SO2+Br2+2H2O═4H++SO42-+2Br- C.侯氏制堿:Na++NH3+CO2+H2O═NaHCO3↓+NH4+ D.Mg(HCO3)2溶液中滴加少量澄清石灰水:Mg2++2HCO3-+Ca2++2OH-═MgCO3↓+CaCO3↓+2H2O 組卷:11引用:1難度:0.6 -
6.如圖是實驗室中制取KMnO4的流程圖,已知 K2MnO4顯墨綠色,下列說法錯誤的是( )

A.第①步在鐵坩堝中進行,第⑥步中加熱濃縮在蒸發皿中進行 B.第②步中KClO3作還原劑,第③步分批浸取可提高浸取率 C.第④步通CO2發生反應:3MnO42-+2CO2═2MnO4-+MnO2↓+2CO32-,當有43.5g沉淀生成,反應中轉移的電子數為NA個 D.第⑤步加熱趁熱過濾,說明KMnO4的溶解度隨溫度變化較大 組卷:4引用:1難度:0.5
二、非選擇題:本題共4小題,共58分。
-
17.現代煤化工產生大量H2S廢氣,其回收利用有重要意義。
Ⅰ.熱解H2S制H2。
(1)已知下列反應的熱化學方程式:
①2H2S(g)+3O2(g)═2SO2(g)+2H2O(g)ΔH1=-1036kJ?mol-1
②4H2S(g)+2SO2(g)═3S2(g)+4H2O(g)ΔH2=94kJ?mol-1
③2H2(g)+O2(g)═2H2O(g)ΔH3=-484kJ?mol-1
判斷H2S熱分解反應④2H2S(g)?S2(g)+2H2(g)活化能E正E逆(填“>”“<”或“=”)。
(2)在1373K、100kPa反應條件下,對于n(H2S):n(Ar)分別為4:1、1、1:4、1:9、1:19的H2S-Ar混合氣,熱分解反應過程中H2S轉化率隨時間的變化如圖所示: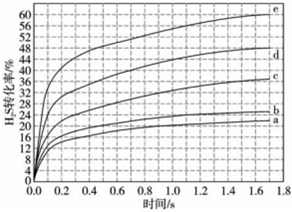
①n(H2S):n(Ar)越大,H2S平衡轉化率,理由是。
②計算n(H2S):n(Ar)=1:4時,在0~0.9s之間,H2S分壓的平均變化率為kPa?s-1。
Ⅱ.H2S可轉化成羰基硫(COS):H2S(g)+CO(g)?COS(g)+H2(g)ΔH。
(1)絕熱恒壓條件下,密閉容器中充入H2S(g)與CO(g)進行上述反應。下列事實不能說明反應達到平衡狀態的是(填序號)。
A.混合氣體的平均相對分子質量不再改變
B.生成amolCOS,同時形成2amolH-S鍵
C.化學平衡常數不再改變
D.混合氣體的密度不再改變
(2)T℃下,將物質的量之比為2:1的H2S(g)與CO(g)充入恒容密閉容器中進行上述反應,測得平衡時容器內氣體的總壓為pPa,COS(g)的體積分數為10%。則此時該反應的平衡常數Kp=(保留2位有效數字)。
Ⅲ.用H2S、空氣和KOH溶液可以組成燃料電池,其總反應式為2H2S+3O2+4KOH═2K2SO3+4H2O。
(1)電池的負極電極反應式為。
(2)若電池開始工作時每100mL電解質溶液含KOH56g。取電池工作一段時間后的電解質溶液20.00mL,加入BaCl2溶液至沉淀完全,過濾洗滌沉淀,將沉淀在空氣中充分加熱至恒重,測得固體質量為11.65g,計算電池工作的這段時間內至少通入了標況下的氧氣約L。組卷:14引用:1難度:0.5 -
18.特布他林(H)是一種治療支氣管哮喘,喘息性支氣管炎,肺氣腫等的藥物,它的一種合成路線如圖所示:
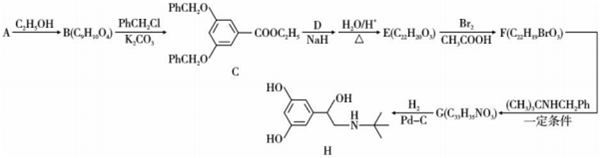
已知:Ⅰ.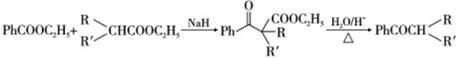 (R,R′為H,烷基,酰基);
(R,R′為H,烷基,酰基);
Ⅱ.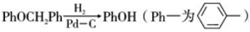 。
。
回答下列問題:
(1)A的系統命名是。
(2)C中所含官能團的名稱是。
(3)E的結構簡式為。
(4)B→C的反應類型為,該反應的目的是。
(5)F→G的反應方程式為。
(6)H的芳香族同分異構體中,僅含-NH2和-CH2CH2OH的結構有種。
(7)根據上述信息,寫出以4-羥基鄰苯二甲酸二乙酯為主要原料制備合成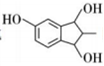 的路線(其他試劑任選) 。組卷:6引用:1難度:0.3
的路線(其他試劑任選) 。組卷:6引用:1難度:0.3


