2021-2022學年湖北省武漢市華中師大一附中高一(下)期中化學試卷
發布:2024/10/28 23:0:2
一.選擇題(每小題3分,共48分,每題只有一個正確選項)
-
1.中國將與各方攜手推動全球環境治理以及可持續發展事業,構建人類命運共同體。下列說法不正確的( )
A.購物時提倡少用塑料袋以減少白色污染 B.排放到空氣中的CO2、NO2、SO2均會形成酸雨 C.為防止電池中的重金屬污染土壤,應積極開發廢電池的綜合利用 D.利用太陽能等清潔能源代替化石燃料,有利于節約資源、保護環境 組卷:50引用:6難度:0.6 -
2.“九秋風露越窯開,奪得千峰翠色來”是贊譽越窯秘色青瓷的詩句,描繪我國古代精美的青瓷工藝品。玻璃、水泥和陶瓷均為硅酸鹽制品,下列有關說法中正確的是( )
A.玻璃是人類最早使用的硅酸鹽制品 B.制水泥的原料為純堿、石灰石和石英砂 C.硅酸鹽制品的性質穩定、熔點較高 D.沙子和黏土的主要成分均為硅酸鹽 組卷:115引用:7難度:0.7 -
3.某化學興趣小組學習原電池知識后,決定用其原理,嘗試利用鐵粉、活性炭、無機鹽等物質開發產品.小組提出的設想或對原理的理解不正確的是( )
A.打算制成小包裝用于糕點的脫氧劑 B.利用反應放出熱量的原理制成暖寶寶 C.調整電池結構,可降低溫度,可用于延長糕點保質期 D.正極的電極反應為:2H2O+O2+4e-=4OH- 組卷:29引用:4難度:0.7 -
4.下列敘述正確的是( )
A.濃硫酸具有吸水性,因而能使蔗糖炭化 B.濃HNO3易揮發,打開裝有濃HNO3容量瓶的瓶塞,瓶口有白煙 C.濃鹽酸是一種干燥劑,能夠干燥氨氣、氫氣等氣體 D.濃硫酸、濃HNO3在常溫下能夠使鐵、鋁金屬鈍化 組卷:37引用:2難度:0.6 -
5.下列關于二氧化硫的說法不正確的是( )
A.SO2能使H2S的水溶液出現黃色沉淀,說明SO2具有氧化性 B.SO2能使品紅溶液褪色,說明SO2具有漂白性 C.SO2通入水中無明顯現象,說明SO2不與水反應 D.SO2能使酸性KMnO4溶液褪色,說明SO2具有還原性 組卷:37引用:1難度:0.7 -
6.在C(s)+CO2(g)═2CO(g)的反應中,現采取下列措施:①縮小體積,增大壓強②增加碳的量 ③通入CO2④恒容下充入N2⑤恒壓下充入N2。能夠使反應速率增大的措施是( )
A.①④ B.②③⑤ C.①③ D.①②④ 組卷:1255引用:37難度:0.9 -
7.反應N2(g)+3H2(g)?2NH3(g)△H<0,若在恒壓容器中發生,下列選項表明反應一定已達平衡狀態的是( )
A.容器內氣體的密度不再變化 B.容器內壓強保持不變 C.相同時間內,生成N-H鍵的數目與斷開H-H鍵的數目相等 D.容器內氣體的濃度之比c(N2):c(H2):c(NH3)=1:3:2 組卷:109引用:5難度:0.9
二、非選擇題(共52分)
-
20.利用甲烷與氯氣發生取代反應制取副產品鹽酸的設想在工業上已成為現實。某化學興趣小組在實驗室中模擬上述過程,其設計的模擬裝置如圖:
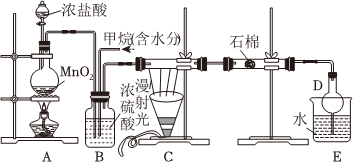
試回答下列問題:
(1)請寫出C裝置中生成CH2Cl2的化學方程式:。
(2)B裝置有三種功能:①混勻混合氣體;②;③。
(3)D裝置的名稱為,其作用是。
(4)E裝置中除鹽酸外,還含有機物,從E中分離出鹽酸的最佳方法為(填字母)。
a.分液法 b.蒸餾法 c.結晶法
(5)將1mol CH4與Cl2發生取代反應,充分反應后生成的CH3Cl、CH2Cl2、CHCl3、CCl4四種有機產物的物質的量依次增大0.1mol,則參加反應的Cl2的物質的量為。
(6)已知丁烷與氯氣的取代反應的產物之一為C4H8Cl2,其有種同分異構體。組卷:113引用:4難度:0.6 -
21.將濃度均為0.01 mol/L 的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定時間后溶液變為藍色。該實驗是一種“碘鐘實驗”。某小組同學在室溫下對該“碘鐘實驗”的原理進行探究。
【資料】
該“碘鐘實驗”的總反應:H2O2 +2S2O32-+2H+═S4O62-+2H2O
反應分兩步進行:
反應A:H2O2 +2I-+2H+═I2+2H2O
反應B:……
(1)反應B的離子方程式是。對于總反應,I-的作用相當于。
(2)為證明反應A、B的存在,進行實驗Ⅰ。
a.向酸化的H2O2溶液中加入試劑X的水溶液,溶液變為藍色。
b.再向得到的藍色溶液中加入Na2S2O3溶液,溶液的藍色褪去。
試劑X是。
試劑
(3)為探究溶液變藍快慢的影響因素,進行實驗Ⅱ、實驗Ⅲ。
(溶液濃度均為0.01 mol/L)
溶液從混合時的無色變為藍色的時間:實驗Ⅱ是30 min、實驗Ⅲ是40 min。用量(ML)
序號H2O2
溶液H2SO4
溶液Na2S2O3
溶液KI溶液
(含淀粉)
H2O實驗Ⅱ 5 4 8 3 0 實驗Ⅲ 5 2 x y z
①實驗Ⅲ中,x、y、z所對應的數值分別是。
②對比實驗Ⅱ、實驗Ⅲ,可得出的實驗結論是。
(4)為探究其他因素對該“碘鐘實驗”的影響,進行實驗Ⅳ.(溶液濃度均為0.01 mol/L)
實驗過程中,溶液始終無明顯顏色變化。用量(mL)
號
試劑H2O2
溶液H2SO4
溶液Na2S2O3
溶液KI溶液(含淀粉)
H2O實驗Ⅳ 4 4 9 3 0
試結合該“碘鐘實驗”總反應方程式及反應A與反應B速率的相對快慢關系,解釋實驗Ⅳ未產生顏色變化的原因:。組卷:135引用:17難度:0.5


