2023年四川省內江市威遠中學高考化學模擬試卷(2月份)
發布:2024/4/20 14:35:0
一、選擇題:本題共7小題,每小題6分,共78分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.2022年4月17日,神舟十三號載人飛船與天和核心艙實現對接后順利返航。下列說法正確的是( )
A.航天器的操縱桿采用的碳纖維屬于有機高分子材料 B.火箭推進劑的燃燒可將化學能完全轉化為機械能 C.空間站使用的太陽能電池板主要材料是二氧化硅 D.核心艙內氧氣來源于水的電解,此過程中氧氣為氧化產物 組卷:50引用:3難度:0.9 -
2.設NA為阿伏加德羅常數的值。下列說法正確的是( )
A.12.0g熔融的NaHSO4中含有的陽離子數為0.1NA B.17.0g-OH和OH-的混合體所含電子數為10NA C.標準狀況下,2.24L甲醇中含有的C-H數為0.3NA D.將足量MnO2與含4molHCl的濃鹽酸混合,轉移電子數為2NA 組卷:36引用:1難度:0.6 -
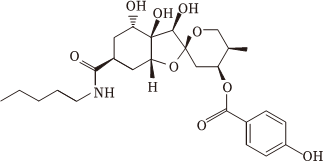 3.據報道,南方醫科大學、香港大學、昆明理工大學聯合科研團隊對傣族藥用植物葉下珠中的抗病毒天然活性分子進行結構優化,合成了葉下珠素HB-43(結構如圖),抗乙肝病毒活性提高了100倍,毒性降低1000倍,且能有效抑制新型冠狀病毒奧密克戎變種的體內感染。下列有關葉下珠素HB-43的說法錯誤的是( )
3.據報道,南方醫科大學、香港大學、昆明理工大學聯合科研團隊對傣族藥用植物葉下珠中的抗病毒天然活性分子進行結構優化,合成了葉下珠素HB-43(結構如圖),抗乙肝病毒活性提高了100倍,毒性降低1000倍,且能有效抑制新型冠狀病毒奧密克戎變種的體內感染。下列有關葉下珠素HB-43的說法錯誤的是( )A.屬于芳香族化合物 B.能與FeCl3溶液發生顯色反應 C.一定條件下能發生取代、加成、消去反應 D.含9個手性碳(連有4個不同原子或原子團的碳) 組卷:37引用:2難度:0.6
三、非選擇題:共174分。第22~32題為必考題,每個試題考生都必須作答。第33~38題為選考題,考生根據要求作答。
-
10.汽車尾氣中含有CO、NO、NO2等有毒氣體,對汽車加裝尾氣凈化裝置,使用催化劑催化,可使有毒氣體相互反應轉化成無毒氣體。
(1)氮氧化物間可以相互轉化
已知2NO(g)+O2(g)=2NO2(g)的反應歷程分兩步:
第一步:2NO(g)=N2O2(g)(快速平衡)
第二步:N2O2(g)+O2(g)=2NO2(g)(慢反應)
①用O2表示的速率方程為v(O2)=k1?c2(NO)?c(O2);NO2表示的速率方程為v(NO2)=k2?c2(NO)?c(O2),k1與k2分別表示速率常數(與溫度有關),則=k1k2。
②下列關于反應2NO(g)+O2(g)=2NO2(g)的說法正確的是(填序號)。
A.增大壓強,反應速率常數一定增大
B.第一步反應的活化能小于第二步反應的活化能
C.反應的總活化能等于第一步和第二步反應的活化能之和
(2)容積均為1L的甲、乙兩個容器,其中甲為絕熱容器,乙為恒溫容器.相同溫度下,分別充入0.2mol的NO2,發生反應:2NO2(g)=N2O4(g)△H<0,甲中NO2的相關量隨時間變化如圖所示。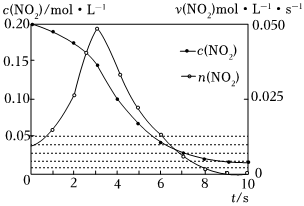
①0~3s內,甲容器中NO2反應速率增大的原因是。
②甲達平衡時,溫度若為T℃,此溫度下的平衡常數K=。
③平衡時,K甲K乙,P甲P乙(填“>”、“<”或“=”)。
(3)CO還原法處理NO:原理為2CO(g)+2NO(g)=N2(g)+2CO2(g)△H=-746kJ/mol。在容積為2L的某密閉容器中充入4molCO和4molNO,發生該反應。平衡體系中NO的體積分數與溫度、體系總壓強的關系如圖所示。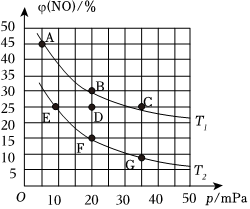
①下列有關說法正確的是(填代號)。
a.溫度:T2>T1
b.NO的平衡轉化率:F>D>B
c.反應速率:C>D>E
②某溫度下,上述反應進行5min時放出的熱量為373kJ,則N2的平均反應速率v(N2)=mol?L?1?min-1。
③圖中E點,N2的體積分數為%。組卷:42引用:1難度:0.5
[化學—選修3:物質結構與性質]
-
11.含鈷化合物在機械制造、磁性材料等領域具有廣泛的應用,請回答下列問題:
(1)基態Co3+的價電子軌道表示式(價電子排布圖)為。
(2)鈷可以形成配合物[Co(NH3)5Cl](NO3)2(硝酸氯五氨合銅)和Co2(CO)8(八羰基二鈷)。
①C、N、O和Na四種元素,第二電離能由大到小順序為。
②1mol[Co(NH3)5Cl]2+中的σ鍵數為;N原子的雜化軌道類型為;的空間構型為NO-3。
③已知Cl的含氧酸酸性由強到弱的順序為HClO4>HClO3>HClO2>HClO,其原因是。
④八羰基二鈷的熔點51~52℃,沸點52℃,該物質的晶體屬于晶體,其不溶于水,可溶于苯、二硫化碳等多種有機溶劑,其原因是。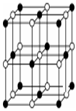
(3)Co的一種氧化物的晶胞如圖,已知鈷原子的半徑為apm,氧原子的半徑為bpm,它們在晶體中是緊密接觸的,鈷原子填在氧原子的(填空間結構)空隙;在該鈷的氧化物晶體中原子的空間利用率為(均用含a、b的計算表達式表示)。組卷:66引用:1難度:0.3


