2021年江蘇省蘇州市高考化學調研試卷(零模)
發布:2024/4/20 14:35:0
一、單項選擇題:共12小題,每題3分,共42分。每題只有一個選項最符合題意。
-
1.加強水資源保護是實現生態文明的核心。下列做法不應該提倡的是( )
A.將有害污染物深度填埋 B.培養節約用水的意識 C.減少農業生產中化肥和農藥的使用 D.合理使用無害化處理后的生活污水 組卷:23引用:1難度:0.6 -
2.反應Cl2+Na2SO3+H2O═Na2SO4+2HCl可用于污水脫氯。下列相關微粒的說法正確的是( )
A.中子數為20的氯原子: Cl2017B.H2O的電子式: 
C.Na+的結構示意圖 
D. 的空間構型為平面三角形SO2-3組卷:104引用:3難度:0.8 -
3.下列用于污水處理的物質,其性質與用途具有對應關系的是( )
A.Ca(ClO)2有強氧化性,可用于消毒殺菌 B.明礬的焰色呈紫色,可用于沉降泥沙 C.木炭具有還原性,可用于吸附苯等有機物 D.CaO具有吸水性,可用于沉淀重金屬離子 組卷:37引用:1難度:0.7 -
4.用石灰乳吸收硝酸工業的尾氣(含NO、NO2)可獲得Ca(NO2)2,其部分工藝流程如圖,下列說法不正確的是( )
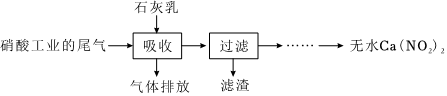
A.吸收時主要反應的化學方程式為NO+NO2+Ca(OH)2═Ca(NO2)2+H2O B.將石灰乳改為澄清石灰水吸收效率將會增大 C.采用氣液逆流接觸有利于尾氣中NO、NO2的充分吸收 D.若尾氣中n(NO2):n(NO)<1:1,吸收后排放的氣體中NO含量升高 組卷:156引用:7難度:0.8 -
5.短周期主族元素X、Y、Z、W原子序數依次增大,X原子核外有7個電子,Y在周期表中位于ⅡA族,Z與X屬于同一主族,基態W原子的核外有2個未成對電子。下列說法正確的是( )
A.原子半徑:r(X)<r(Y)<r(Z)<r(W) B.第一電離能:I1(Y)<I1(W)<I1(Z) C.Z的最高價氧化物對應水化物的酸性比X的強 D.元素Y、W的簡單離子具有相同的電子層結構 組卷:37引用:2難度:0.5
二、非選擇題:共4題,共58分。
-
17.以鹽湖鋰精礦(主要成分為Li2CO3,還含有少量的CaCO3)和鹽湖鹵水(含一定濃度LiCl和MgCl2)為原料均能制備高純Li2CO3。
(1)以鋰精礦為原料制取碳酸鋰的流程如圖1,其中“碳化溶解”的裝置如圖2所示。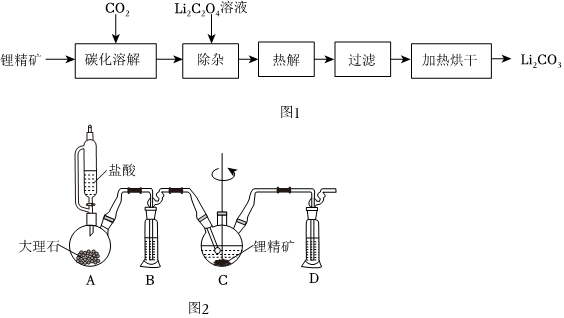
已知:Ⅰ.20℃時LiOH的溶解度為12.8g。
Ⅱ.Li2CO3在不同溫度下的溶解度:0℃1.54g,20℃1.33g,80℃0.85g。
①裝置C中主要反應的化學方程式為。
②裝置C中的反應需在常溫下進行,溫度越高鋰精礦轉化速率越小的原因可能是。保持溫度、反應時間、反應物和溶劑的量不變,實驗中提高鋰精礦轉化率的操作有。
③熱解、過濾獲得Li2CO3的表面有少量Li2C2O4,未經洗滌也不會影響最終Li2CO3產品的純度,其原因是。
(2)設計由鹽湖鹵水制取Li2CO3的實驗方案:向濃縮后的鹽湖鹵水。[已知:pH=10時Mg(OH)2完全沉淀,實驗中必須用的試劑:NaOH溶液、Na2CO3溶液]。組卷:64引用:3難度:0.6 -
18.硫化氫的轉化是資源利用和環境保護的重要研究課題。
(1)通過電化學循環法可將H2S轉化為H2SO4和H2(如圖1所示)。其中氧化過程發生如下兩步反應:H2S+H2SO4═SO2↑+S↓+2H2O、S+O2═SO2。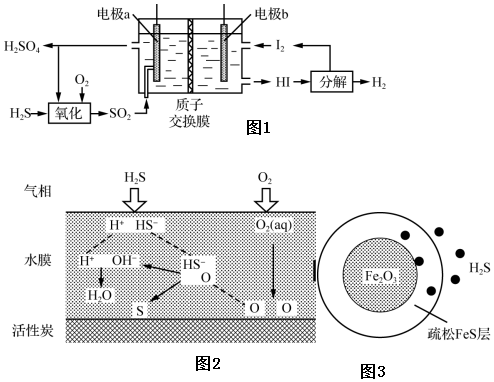
①電極a上發生反應的電極反應式為。
②理論上1mol H2S參加反應可產生H2的物質的量為。
(2)表面噴淋水的活性炭可用于吸附氧化H2S,其原理可用圖2表示。其它條件不變時,水膜的酸堿性與厚度會影響H2S的去除率。
①適當增大活性炭表面的水膜pH,H2S的氧化去除率增大的原因是。
②若水膜過厚,H2S的氧化去除率減小的原因是。
(3)Fe2O3可用作脫除H2S氣體的脫硫劑。H2S首先與表面的Fe2O3產生疏松多孔的產物FeS,隨著反應的進行,Fe2O3不斷減少,產物層不斷加厚,可用圖3所示。失效的脫硫劑可在氧氣中加熱重新轉化為Fe2O3實現“再生”。
①實驗表明用Fe2O3脫除純H2S反應一段時間后,因為產生的S單質將疏松FeS堵塞,反應速率明顯減小。Fe2O3與H2S反應的化學方程式為。
②“再生”時若O2濃度過大、反應溫度過高,“再生”后的脫硫劑脫硫效果明顯變差的原因可能是。組卷:107引用:2難度:0.7


