2016-2017學年廣東省廣州市番禺區高一(下)期末化學試卷(理科)
發布:2025/1/6 5:30:2
一、單項選擇題(共12小題,每小題4分,滿分48分)
-
1.最近日本科學家確認世界還存在著另一種“分子足球”N60,它與C60分子結構相似。N60在高溫或撞擊后會釋放出巨大能量。下列對N60的說法不正確的是( )
A.N60和14N都是氮的同位素 B.N60和N2都是氮的同素異形體 C.N60中氮原子之間由共價鍵結合 D.N60的摩爾質量為840g/mol 組卷:2引用:1難度:0.7 -
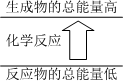 2.下列變化符合圖示的是( )
2.下列變化符合圖示的是( )
①冰雪融化
②KMnO4分解制O2
③鋁與氧化鐵的反應
④鈉與水反應
⑤二氧化碳與灼熱的木炭反應
⑥碘的升華
⑦Ba(OH)2?8H2O和NH4Cl的反應.A.②⑥⑦ B.②⑤⑦ C.①②⑤⑥⑦ D.③④ 組卷:236引用:15難度:0.7 -
3.短周期元素的離子aW2+、bX+、cY2-、dZ-都具有相同的電子層結構,下列推斷正確的是( )
A.原子半徑:W>X>Z>Y B.熱穩定性:H2Y>HZ C.離子半徑:W2+>Y2- D.堿性:XOH>W(OH)2 組卷:244引用:27難度:0.9 -
 4.某有機物的結構如圖所示,該有機物不可能具有的性質是( )
4.某有機物的結構如圖所示,該有機物不可能具有的性質是( )
①能使酸性KMnO4溶液褪色
②可以燃燒
③能發生水解反應
④能發生酯化反應
⑤能發生加聚反應
⑥能跟NaOH溶液反應
⑦能與三氯化鐵發生顯色反應A.①④ B.只有⑦ C.③⑦ D.④⑥ 組卷:3引用:1難度:0.6 -
5.從下列事實所得出的相應結論正確的是( )
實驗事實 結論 A A元素的原子半徑比B元素的原子半徑大 周期表中A位于B的下一周期 B 將CO2通入到Na2SiO3溶液中產生白色渾濁 酸性:H2CO3>H2SiO3 C 常溫下,銅能與濃硝酸反應而鋁被濃硝酸鈍化 還原性:Cu>Al D 常溫下白磷可自燃而氮氣須在放電時才與氧氣反應 非金屬性:P>N A.A B.B C.C D.D 組卷:69引用:5難度:0.5
二、第二部分非選擇題(共4小題,滿分52分)
-
15.以淀粉為主要原料合成一種具有果香味有機物C和高分子化合物E的合成路線如圖1所示。
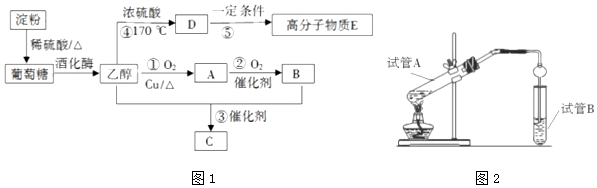
請回答下列問題:
(1)寫出C的結構簡式:,A分子內含有的官能團是(填名稱)。
(2)寫出下列反應的反應類型:①,③。
(3)寫出下列反應的化學方程式:①;⑤。
(4)某同學欲用圖2裝置制備物質C,將試管B中的物質C分離出來,用到的主要玻璃儀器有:燒杯、,插入試管B的導管接有一個球狀物,其作用為。組卷:4引用:2難度:0.6 -
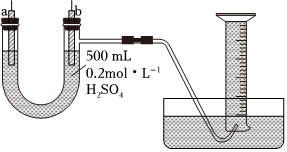 16.Ⅰ.現用如圖裝置來測定某原電池工作時在某段時間內通過導線的電子的物質的量。量筒的規格為1000mL,供選擇的電極材料有純銅片和純鋅片。請回答下列問題:
16.Ⅰ.現用如圖裝置來測定某原電池工作時在某段時間內通過導線的電子的物質的量。量筒的規格為1000mL,供選擇的電極材料有純銅片和純鋅片。請回答下列問題:
(1)b電極材料為,其電極反應式為。
(2)當量筒中收集到672mL(標準狀況下)氣體時,通過導線的電子的物質的量為,此時a電極質量減少g。
Ⅱ.某同學在用稀硫酸與鋅制取氫氣的實驗中,發現加入少量硫酸銅溶液可加快氫氣的生成速率。請回答下列問題:
(1)上述實驗中發生反應的離子方程式有:。
(2)硫酸銅溶液可以加快氫氣生成速率的原因是。
(3)要加快上述實驗中氣體產生的速率,還可采取的措施有、。(答兩種)
(4)為了進一步研究硫酸銅的用量對氫氣生成速率的影響,該同學設計了如下一系列實驗。將表中所給的混合溶液分別加入到6個盛有過量Zn粒的反應瓶中,收集產生的氣體,記錄獲得相同體積的氣體所需時間。(假設混合溶液總體積等于混合前各溶液的體積之和)
①請完成此實驗設計,其中:V3=實驗
混合溶液A B C D E F 4mol/L H2SO4/mL 30 V1 V2 V3 V4 V5 飽和CuSO4溶液/mL 0 0.5 2.5 5 V6 20 H2O /mL V7 V8 V9 V10 10 0 ,V8=。
②該同學最后得出的結論為:當加入少量CuSO4溶液時,生成氫氣的速率會大大提高。但當加入的CuSO4溶液超過一定量時,生成氫氣的速率反而會下降。請分析氫氣生成速率下降的主要原因。
③實驗A測得:收集到產生H2體積為112mL(標準狀況下)時所需的時間為10分鐘,求化學反應速率ν(H2SO4)=。(忽略反應前后溶液體積變化)組卷:28引用:2難度:0.3


