2022年遼寧省遼南協(xié)作體高考化學二模試卷
發(fā)布:2025/1/2 10:30:4
一、選擇題(本題共15小題,每小題3分,共45分。每小題只有一個選項符合要求)
-
1.化學與科技、社會、生活有著密切聯(lián)系。下列有關說法不正確的是( )
A.港珠澳大橋路面使用了瀝青和混凝土,瀝青可以通過石油分餾得到 B.As2O3是治療白血病的一線藥物,我國首次實現(xiàn)其仿生遞送,As2O3是堿性氧化物 C.北京冬奧會采用光伏發(fā)電以減少CO2排放,有利于實現(xiàn)碳達峰 D.神舟十三號飛船成功發(fā)射,航天員的頭盔主要成分是聚碳酸酯,屬于有機高分子 組卷:31引用:3難度:0.6 -
2.下列化學用語使用不正確的是( )
A.中子數(shù)為18的硫原子符號: S3416B.甲醛的分子式為:HCHO C.COCl2的電子式為: 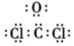
D.CO(NH2)2的球棍模型:  組卷:17引用:1難度:0.6
組卷:17引用:1難度:0.6 -
3.設NA為阿伏加德羅常數(shù)的值,下列說法正確的是( )
A.常溫下,5.6g鐵與足量濃硝酸反應,轉移0.3NA個電子 B.1LpH=1的H2C2O4溶液中含有陽離子總數(shù)為0.2NA C.0.5molCH4和1molCl2在光照下充分反應后的分子數(shù)為1.5NA D.向含有FeI2的溶液中通入適量氯氣,當有l(wèi)molFe2+被氧化時,反應中轉移電子的數(shù)目為3NA 組卷:38引用:1難度:0.5 -
4.水合聯(lián)氨(N2H4?H2O)是具有腐蝕性和強還原性的堿性液體,它是一種重要的化工試劑,其制備的反應原理為:NaClO+2NH3=N2H4?H2O+NaCl下列裝置和操作能達到實驗目的的是( )
A B C D 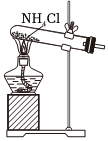
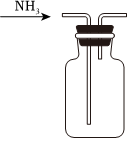
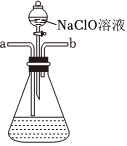
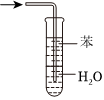
加熱NH4Cl制備NH3 作為反應過程的安全瓶 制備水合聯(lián)氨時從a口通入NH3 吸收反應中過量的NH3 A.A B.B C.C D.D 組卷:28引用:2難度:0.5 -
5.硫酸鹽(含
、SO2-4)氣溶膠是PM2.5的成分之一。近期科研人員提出了霧霾微顆粒中硫酸鹽生成的三個階段的轉化機理,其主要過程如圖所示,下列說法錯誤的是( )HSO-4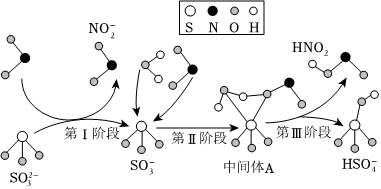
A.第Ⅰ階段的化學方程式為: +NO2=SO2-3+NO-2SO-3B.整個過程中有H2O參加反應 C.1 在第Ⅱ、Ⅲ兩個階段共失去電子數(shù)目為2NAmolSO-3D.NO2是生成硫酸鹽的氧化劑 組卷:15引用:2難度:0.6 -
6.鋁是應用廣泛的金屬。以鋁土礦(主要成分為Al2O3,還含有SiO2和Fe2O3等雜質)為原料制備鋁的一種工藝流程如圖,SiO2在“堿溶”時轉化為鋁硅酸鹽沉淀,下列說法錯誤的是( )
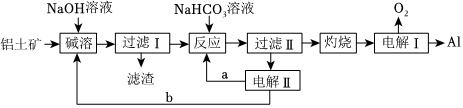
A.“電解Ⅱ”是電解Na2CO3溶液,則b為陰極液,a為陽極液 B.“電解Ⅰ”是電解熔融Al2O3,電解過程中陽極需要定期補充石墨 C.“反應”的離子方程式為: +HCO-3+H2O═Al(OH)3↓+AlO-2CO2-3D.“電解Ⅱ”總反應方程式為:2H2O 2H2↑+O2↑通電組卷:31引用:3難度:0.6
二、非選擇題(本題共55分)
-
18.氨氮廢水中氮元素主要以
、NH3形式存在,氨氮廢水會造成水體富營養(yǎng)化。可用沉淀法處理氨氮廢水并獲得緩釋肥料磷酸鎂銨(MgNH4PO4),過程如圖。NH+4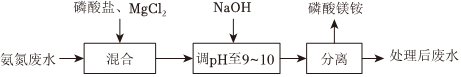
已知:
(1)寫出物質 MgNH4PO4 Mg3(PO4)2 Mg(OH)2 溶度積 2.5×10-13 1.04×1024 1.8×10-11 的電子式NH+4。
(2)經(jīng)處理后,分離磷酸鎂銨所用的方法是。
(3)處理氨氮廢水時氮元素以形式存在,磷酸鹽可選用Na2HPO4,主要生成MgNH4PO4沉淀,反應的離子方程式為NH+4。
(4)向此廢水中加入磷酸鹽和鎂鹽,使銨態(tài)氮的殘留達到一級排放標準(≤1.0mg/L即≤7×10-5mol/L),且c()=1.0×10-5mol/L,則沉淀后的廢水中c(Mg2+)≥PO3-4(保留兩位有效數(shù)字)。
(5)pH過大會降低廢水中氨氮的去除率,可能的原因是。
(6)使用次氯酸鈉等氧化劑可以將污水中的NH3氧化除去,可以產生無色無味氣體,該反應的化學方程式為。某條件下,次氯酸鈉投加量對污水中的氮的去除率的影響如圖所示,當m (NaClO):m(NH3)>7.7時,時,總氮除去率隨m (NaClO):m(NH3)的增大不升反降的原因。 組卷:23引用:2難度:0.5
組卷:23引用:2難度:0.5 -
19.在新型冠狀病毒蔓延的緊要關頭,各科研院所和高校正在緊急攻關治愈新型肺炎的藥物。科學家發(fā)現(xiàn)老藥肉桂硫胺可能對2019-nCoV有效,其合成路線如圖。
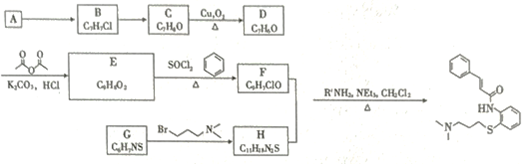
已知: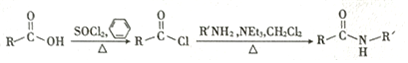
請回答下列問題:
(1)芳香烴A→B的試劑及條件。
(2)G的結構簡式為。
(3)寫出C→D的化學反應方程式。
(4)寫出E的順式結構簡式,E分子中最多有個原子共平面。
(5)K是E的同分異構體,符合下列條件的K的結構有種。其中苯環(huán)上的一氯代物有2種的結構簡式為。
①能發(fā)生銀鏡反應,且能水解
②除苯環(huán)無其他環(huán)狀結構組卷:20引用:1難度:0.3


