2021-2022學(xué)年湖北省鄂西六校高二(下)期中化學(xué)試卷
發(fā)布:2024/12/18 6:0:2
一、選擇題(共15小題,每題3分,共45分。在每小題給出的四個(gè)選項(xiàng)中,只有一項(xiàng)符合題目要求。)
-
1.碳中和是指CO2的排放總量和減少總量相當(dāng)。下列措施中不能有效促進(jìn)碳中和的是( )
A.推動(dòng)氫氧燃料汽車(chē)代替燃油汽車(chē) B.利用可燃冰代替現(xiàn)有化石能源 C.?dāng)U大水力發(fā)電規(guī)模代替火力發(fā)電 D.研發(fā)二氧化碳人工合成淀粉技術(shù) 組卷:5引用:1難度:0.6 -
2.下表列出了某短周期元素R的各級(jí)電離能數(shù)據(jù)(用I表示,單位為kJ/mol),下列關(guān)于元素R的判斷中一定正確的是( )
I1 I2 I3 I4 … 740 1500 7700 10500 … A.短周期元素R的最高正價(jià)為+1價(jià) B.R元素的原子最外層共有4個(gè)電子 C.R元素位于元素周期表中第IIA族 D.R元素基態(tài)原子的價(jià)電子排布式為2s2 組卷:15引用:2難度:0.6 -
 3.元素周期表中鉍元素的數(shù)據(jù)如圖,下列說(shuō)法中正確的是( )
3.元素周期表中鉍元素的數(shù)據(jù)如圖,下列說(shuō)法中正確的是( )A.鉍元素的質(zhì)量數(shù)是209.0 B.鉍原子有83個(gè)能量不相同的電子 C.鉍原子6p能級(jí)有一對(duì)成對(duì)電子 D.鉍原子的價(jià)層電子排布是6s26p3 組卷:8引用:1難度:0.6 -
4.下列關(guān)于共價(jià)鍵的描述錯(cuò)誤的是( )
A.鍵長(zhǎng):O-H<N-H<C-H B.C2H4中碳碳鍵的鍵能:σ鍵>π鍵 C.分子中的鍵角:NH3<CH4 D.氣體單質(zhì)中一定存在σ鍵 組卷:18引用:1難度:0.8 -
 5.已知S2Cl2結(jié)構(gòu)如圖所示,下列關(guān)于S2Cl2的說(shuō)法正確的是( )
5.已知S2Cl2結(jié)構(gòu)如圖所示,下列關(guān)于S2Cl2的說(shuō)法正確的是( )A.S2Cl2是非極性分子 B.沸點(diǎn):S2Cl2<S2Br2 C.S與Cl間的共用電子對(duì)偏離Cl D.S2Cl2分子只含非極性鍵 組卷:10引用:1難度:0.6 -
6.某立方晶系的銻鉀(Sb-K)合金可作為鉀離子電池的電極材料,圖a為該合金的晶胞結(jié)構(gòu)圖,圖b表示晶胞的一部分。下列說(shuō)法正確的是( )
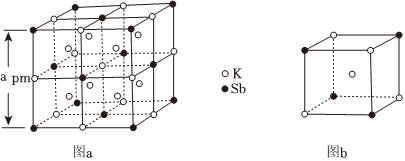
A.該晶胞的體積為a3×10-36cm3 B.晶胞中K和Sb原子數(shù)之比為1:3 C.Sb最鄰近的Sb原子數(shù)為12 D.K和Sb之間的最短距離為0.5apm 組卷:28引用:1難度:0.5
二、非選擇題(共4大題,共55分)
-
18.回答下列問(wèn)題:
(1)已知稀溶液中,1molH2SO4與2molNaOH恰好完全反應(yīng)時(shí),放出114.6kJ熱量,寫(xiě)出該反應(yīng)表示中和熱的熱化學(xué)方程式:。
(2)利用甲烷的還原性,可以對(duì)大氣中的氮氧化合物進(jìn)行處理。已知一定條件下:
①4NO(g)═2NO2(g)+N2(g)ΔH1=-293kJ?mol-l
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)ΔH2=-1160kJ?mol-1
則CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)ΔH=kJ?mol-1,該反應(yīng)能在
下自發(fā)進(jìn)行。(選填“低溫”、“高溫”或“任何溫度”)
(3)①恒溫恒容的密閉容器中,發(fā)生反應(yīng)CO(g)+H2S(g)?COS(g)+H2(g),若反應(yīng)前只充10molCO和xmolH2S,達(dá)到平衡時(shí)CO的物質(zhì)的量為8mol,且化學(xué)平衡常數(shù)為0.1,則x=mol。
②恒溫恒容時(shí),能表明Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)達(dá)平衡狀態(tài)的是(填字母)。
A.單位時(shí)間內(nèi)生成nmolCO同時(shí)消耗nmolCO2
B.c(CO)不隨時(shí)間改變
C.CO2的體積分?jǐn)?shù)不變
D.Fe的濃度不變
(4)某種新工藝裝置是氯堿工業(yè)裝置和另一種電化學(xué)裝置組合而成,相關(guān)物料的傳輸與轉(zhuǎn)化關(guān)系如圖所示,其中電極未標(biāo)出,所用的離子交換膜都只允許陽(yáng)離子通過(guò)。
圖中物質(zhì)Y的電子式,圖中b%a%(填“<”或“>”或“=”),通入除去CO2的空氣一極的電極反應(yīng)式為。組卷:12引用:2難度:0.7 -
19.亞硝酰氯(NOCl)常用于合成洗滌劑、觸媒及用作中間體。某學(xué)習(xí)小組在實(shí)驗(yàn)室用Cl2與NO制備N(xiāo)OCl并測(cè)定其純度,進(jìn)行如圖1所示實(shí)驗(yàn)(夾持裝置略去):

查閱資料:
①亞硝酰氯的熔點(diǎn)為-64.5℃、沸點(diǎn)為-5.5℃,氣態(tài)時(shí)呈黃色,液態(tài)時(shí)呈紅褐色。
②亞硝酰氯遇水易反應(yīng)生成一種氯化物和兩種氮的常見(jiàn)氧化物,其中一種呈紅棕色。
請(qǐng)回答下列問(wèn)題:
Ⅰ.Cl2的制備:舍勒制備氯氣的方法至今還是實(shí)驗(yàn)室制取氯氣的主要方法之一。
(1)該反應(yīng)中被還原與被氧化的物質(zhì)的物質(zhì)的量之比為。
(2)欲收集一瓶純凈干燥的氯氣,選擇上圖中的裝置,其導(dǎo)管連接順序?yàn)閍→→i→h(按氣流方向填小寫(xiě)字母標(biāo)號(hào))。
Ⅱ.亞硝酰氯的制備。實(shí)驗(yàn)室可用如圖2所示裝置制備亞硝酰氯(冰鹽水的溫度一般在-20~-10℃):
(3)組裝好實(shí)驗(yàn)裝置后應(yīng)先檢查裝置氣密性,然后裝入藥品。一段時(shí)間后,兩種氣體在裝置Z中反應(yīng)的現(xiàn)象為。
Ⅲ.亞硝酰氯純度的測(cè)定:將所得亞硝酰氯產(chǎn)品13.10g溶于水,配制成250mL溶液;取出25.00mL,以K2CrO4溶液為指示劑,用0.8mol?L-1AgNO3標(biāo)準(zhǔn)溶液滴定至終點(diǎn),消耗標(biāo)準(zhǔn)溶液的體積為22.50mL。(已知:Ag2CrO4為磚紅色固體)
(4)配制溶液時(shí)除使用燒杯、玻璃棒、膠頭滴管、量筒外,還需用到的玻璃儀器是;當(dāng)?shù)稳胱詈蟀氲蜛gNO3標(biāo)準(zhǔn)溶液后,出現(xiàn)且半分鐘內(nèi)不消失,即達(dá)到滴定終點(diǎn)。
(5)亞硝酰氯(NOCl)與水反應(yīng)的離子方程式為,亞硝酰氯的質(zhì)量分?jǐn)?shù)為。組卷:22引用:1難度:0.5


