2022年山東省德州市高考化學二模試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共10小題,每小題2分,共20分。每小題只有一個選項符合題目要求。
-
1.2021年10月16日,搭載神舟十三號載人飛船的長征二號F遙十三運載火箭,在酒泉衛星發射中心按照預定時間精準點火發射,這是中國空間站關鍵技術驗證階段第六次飛行。下列敘述錯誤的是( )
A.火箭箭體采用的高強度新型鈦合金結構屬于金屬材料 B.航天員航天服上的橡膠屬于有機高分子材料 C.二氧化硅是飛船搭載的太陽能電池板的核心材料 D.航天員手臂“延長器”——操縱棒中的碳纖維材料屬于新型材料 組卷:32引用:2難度:0.6 -
2.下列有關物質性質及其應用敘述正確的是( )
A.利用FeS的還原性,處理廢水中的Hg2+ B.利用MgCl2溶液的導電性,電解MgCl2溶液制Mg C.利用非金屬性C>Si,工業上用C與SiO2反應制備粗Si D.利用H2O2的氧化性處理古畫中變黑的顏料( PbS)恢復白色(PbSO4) 組卷:29引用:1難度:0.7 -
3.關于下列實驗裝置的說法正確的是( )
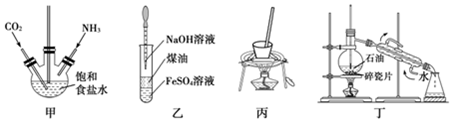
A.圖甲可用來制備小蘇打 B.圖乙能保證較長時間觀察到白色沉淀 C.圖丙可實現蒸發Na2CO3溶液得到Na2CO3固體 D.圖丁可以實現石油分餾 組卷:29引用:3難度:0.5 -
 4.短周期主族元素W、X、Y、Z的原子序數依次增大,且總和為24,四種元素組成的化合物(如圖所示),具有良好的儲氫性能。下列有關敘述正確的是( )
4.短周期主族元素W、X、Y、Z的原子序數依次增大,且總和為24,四種元素組成的化合物(如圖所示),具有良好的儲氫性能。下列有關敘述正確的是( )A.該化合物中X、Y和W原子間均存在配位鍵 B.Y的最高價氧化物的水化物一定為強酸 C.離子半徑:Z>Y>W D.電負性順序:X>Y>W 組卷:27引用:1難度:0.6 -
5.下列由實驗現象所得結論正確的是( )
A.向苯酚鈉溶液中通入二氧化碳,溶液變渾濁,證明碳酸的pH比苯酚小 B.檢驗FeCl3溶液中是否混有Fe2+時,滴入酸性高錳酸鉀溶液,紫紅色褪去,證明含有Fe2+ C.向兩支盛KI3溶液的試管中分別滴加淀粉和硝酸銀溶液,前者變藍,后者生成黃色沉淀,證明存在:I3-?I2+I- D.向0.1mol/LZnSO4溶液中滴加Na2S溶液至不再有白色沉淀生成,再滴加少量0.1mol/LCuSO4溶液,產生黑色沉淀,證明Ksp(ZnS)<Ksp(CuS) 組卷:14引用:1難度:0.7 -
6.下列有關計算正確的是( )
A.Na2O2作供氧劑時,每生成5.6LO2 (標況),轉移電子數為0.25NA B.1.92gCu與足量稀硝酸反應,被還原硝酸的物質的量為0.02mol C.利用鋁熱反應制備金屬時,每得到1molFe,一定消耗0.5mol氧化劑 D.已知NH3的燃燒熱為316.25kJ/mol,則NH3燃燒的熱化學方程式為:4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H=-1265kJ/mol 組卷:62引用:1難度:0.5
三、非選擇題:本題共5小題,共60分。
-
19.有機物G是某藥物的中間體,合成路線如圖所示:

已知:R-CNR-CH2NH2H2催化劑
R1-NH2+R2-COOC2H5催化劑
(1)A的化學名稱,A→B的反應類型,G中官能團名稱。
(2)寫出C→D的化學方程式。
(3)寫出F的結構簡式。
(4)L是D的一種同分異構體,寫出滿足下列條件的L的結構簡式:。
a.能與FeCl3溶液顯紫色
b.核磁共振氫譜有4組峰,且峰面積比為9:3:2:2
(5)設計以 為原料合成
為原料合成 的路線(無機試劑任選)。組卷:11引用:1難度:0.5
的路線(無機試劑任選)。組卷:11引用:1難度:0.5 -
20.3D打印對鈦粉末的要求很高。熔鹽電解精煉是制取鈦粉的有效途徑。精煉時一般采用等摩爾比的KCl-NaCl熔鹽,其中含有一定濃度的低價氯化鈦(TiClx,x=2、3)。(已知:①熔鹽中Ti3+少,Ti2+多熔鹽電解精煉制得的鈦粉顆粒相對粗大;②鈦的熔點為1668℃,TiCl4熔點-24.1℃、沸點136.4℃)。
(1)精煉時,粗品質的海綿鈦、廢鈦材等做電解池的極。
(2)采用海綿鈦與TiCl4制取低價鈦離子的電解質熔鹽時,熔鹽中存下如下4個反應:
ⅰ.3Ti4++Ti0→4Ti3+△H1
ⅱ.Ti4++Ti0→2Ti2+△H2
ⅲ.Ti4++Ti2+→2Ti3+△H3
ⅳ.△H4
①反應ⅳ的化學方程式為。
②上述4個反應的平衡常數與溫度的關系如圖。由此可知△H13△H2(填“>”、“<”或“=”)。
③有助于制取低價鈦離子的電解質熔鹽的措施為。
(3)向如圖裝置中加入海綿鈦,從石英管中緩慢加入amolTiCl4,恒溫條件下進行反應。
①平衡時,測得消耗海綿鈦及TiCl4的物質的量分別為bmol、cmol。熔鹽中低價鈦離子的平均價態為。
②用各離子的物質的量分數表示平衡濃度,則反應ⅲ的平衡常數K3=。
③若向此平衡體系中繼續注入TiCl4,則再次平衡后c平(Ti4+)c平(Ti2+)(填“增大”、“減小”或“不變”)
(4)電解精煉制鈦粉,偶爾會得到一些相對粗大的鈦粉顆粒而影響產品質量,請分析產生的原因(寫出1條原因,合理即可)。組卷:40引用:1難度:0.6


