2021-2022學年福建省泉州實驗中學、惠安一中、安溪一中、養正中學高三(上)期中化學試卷
發布:2024/12/15 6:0:2
一、選擇題(本題共10小題,每小題4分,共40分。每小題只有一個選項符合題目要求。)
-
1.新冠病毒由蛋白質和核酸組成,直徑大約在60~140nm,怕酒精,不耐高溫。下列正確的是( )
A.醫用酒精中乙醇的體積分數越高越好 B.高溫、紫外線、過氧乙酸均可使新冠病毒失去活性 C.新冠病毒擴散到空氣中不可能形成膠體 D.“84”消毒液(主要成分NaClO)中加入濃鹽酸可以增強消毒效果 組卷:19引用:1難度:0.7 -
2.工業上制備下列物質的生產流程合理的是( )
A.由鋁土礦冶煉鋁:鋁土礦 Al2O3提純AlCl3HClAl電解B.由NaCl制漂白粉:飽和食鹽水 Cl2電解漂白粉NaOH溶液C.從海水中提取鎂:海水 Mg(OH)2石灰乳MgO加熱Mg電解D.由黃鐵礦制硫酸:黃鐵礦 SO2煅燒SO3催化氧化H2SO498%濃硫酸組卷:16引用:2難度:0.6 -
3.NA是阿伏加德羅常數的值,下列說法正確的是( )
A.22.4L(標準狀況)HF所含的質子數為10NA B.常溫下,12g石墨中含有C-C鍵的數目為3NA C.疊氮化銨(NH4N3)可發生爆炸反應:NH4N3=2N2↑+2H2↑,則每收集標況下89.6L氣體轉移電子數為4NA D.向100mL1mol/L的Fe(NO3)3溶液中滴加足懸的HI溶液,轉移電子數為0.1NA 組卷:3引用:2難度:0.7 -
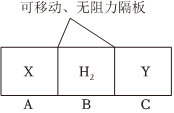 4.如圖所示,在一個容積固定的恒溫容器中,有兩個可左右滑動的密封隔板,在A、B、C分別充入等質量的X、H2、Y三種氣體。當隔板靜止時,A、C內的氣體密度相等,下列說法不正確的是( )
4.如圖所示,在一個容積固定的恒溫容器中,有兩個可左右滑動的密封隔板,在A、B、C分別充入等質量的X、H2、Y三種氣體。當隔板靜止時,A、C內的氣體密度相等,下列說法不正確的是( )A.摩爾質量:M(X)=M(Y) B.分子的數目:N (X)=N(Y) C.氣體的體積:V(X)=V(Y) D.物質的量:n(X)<n(H2)<n(Y) 組卷:25引用:4難度:0.7
二、非選擇題(本題包括5大題,共60分)
-
13.寫出符合下列要求的離子反應方程式。
(1)向NaHSO4溶液中滴加NaHSO3溶液的離子反應方程式為:。
(2)向NaHSO4溶液中滴加過量氫氧化鋇溶液,離子反應方程式為:。
(3)向1L1mol/L的NH4Al(SO4)2溶液中滴加2L等濃度的Ba(OH)2溶液,離子反應方程式為:。
(4)化學在環境保護中起著十分重要的作用,催化反硝化法可用于治理水中硝酸鹽的污染,催化反硝化法中H2能將NO3-還原為N2,一段時間后溶液堿性明顯增強。上述反應的離子方程式為。
(5)利用I2的氧化性可測定鋼鐵中硫的含量。做法是將鋼樣中的硫轉化成H2SO3,然后用一定濃度的I2溶液進行滴定,滴定反應的離子方程式為。
(6)Fe的一種含氧酸根FeO42-具有強氧化性,在其鈉鹽溶液中加入稀硫酸,溶液變為黃色,并有無色氣體產生。該反應的離子方程式是。組卷:6引用:1難度:0.7 -
14.用如下方法回收廢舊CPU中的單質Au(金),Ag和Cu。
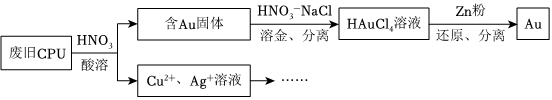
已知:
①濃硝酸不能單獨將Au溶解。
②HAuCl4?H++AuCl-4
(1)酸溶后經操作,將混合物分離。
(2)濃、稀HNO3均可作酸溶試劑。溶解等量的Cu消耗HNO3的物質的量不同,寫出消耗HNO3物質的量少的反應的化學方程式:
(3)HNO3-NaCl與王水[V(濃硝酸):V(濃鹽酸)=1:3]溶金原理相同。
①將溶金反應的化學方程式補充完整:Au+NaCl+HNO3═HAuCl4+++NaNO3
②關于溶金的下列說法正確的是。
A.用到了HNO3的氧化性
B.王水中濃鹽酸的主要作用是增強溶液的酸性
C.用濃鹽酸與NaNO3也可使Au溶解
(4)若用Zn粉將溶液中的1mol HAuCl4完全還原,則參加反應的Zn的物質的量是mol。
(5)用適當濃度的鹽酸、NaCl溶液、氨水與鐵粉,可按照如下方法從酸溶后的溶液中回收Cu和Ag(圖中標注的試劑和物質均不同)。試劑1是;試劑2是。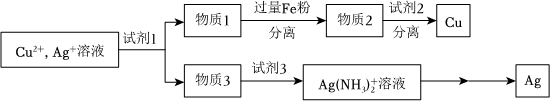 組卷:536引用:9難度:0.4
組卷:536引用:9難度:0.4


