2020-2021學年福建省寧德市高一(上)期末化學試卷
發布:2024/4/20 14:35:0
一、選擇題:每小題只有一個選項符合題意。
-
1.下列不屬于化學對人類貢獻的是( )
A.研制新藥物 B.改良水稻品種 C.合成新材料 D.開發新能源 組卷:23引用:1難度:0.7 -
2.油炸蝦條、薯片等容易擠碎的食品,一般用充氣袋包裝。充氣袋中適宜填充的氣體是( )
A.N2 B.SO2 C.H2 D.NH3 組卷:113引用:2難度:0.8 -
3.打贏藍天保衛戰,提高空氣質量。下列物質不屬于空氣污染物的是( )
A.PM2.5 B.O2 C.SO2 D.NO 組卷:314引用:11難度:0.5 -
4.在實驗室里,保存在棕色試劑瓶中的藥品是( )
A.濃硫酸 B.濃硝酸 C.濃鹽酸 D.碳酸鈉 組卷:6引用:1難度:0.8 -
5.在自然界中只以化合態存在的元素是( )
A.Fe B.N C.S D.Cl 組卷:100引用:1難度:0.9 -
6.用氯化鈉固體配制一定物質的量濃度的溶液,所給圖示對應的操作存在錯誤的是( )
A. 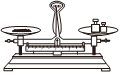
稱量B. 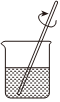
溶解C. 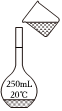
轉移溶液D. 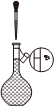
定容組卷:14引用:1難度:0.6 -
7.下列物質均可用于漂白,漂白原理不同于其它物質的是( )
A.漂白粉 B.過氧化鈉 C.氯水 D.活性炭 組卷:14引用:1難度:0.8 -
8.下列物質中,既含有氯分子,又含有氯離子的是( )
A.氯氣 B.氯水 C.氯化鈉 D.氯化氫 組卷:35引用:4難度:0.8
三、非選擇題
-
23.氨和硝酸是重要的工業產品,如圖是工業合成氨及制備硝酸的流程示意圖。
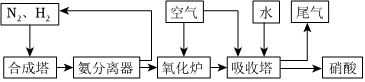
(1)合成塔中發生反應的化學方程式為。
(2)氨分離器中壓強約為15MPa,溫度約為-20℃,分離氨應用了氨的性質。
(3)氧化爐中,NH3轉化為NO的化學方程式為。標準狀況下,5.6LNH3被氧化為NO時轉移電子的物質的量為。
(4)吸收塔中出來的尾氣可用Na2CO3溶液吸收,主要反應為:
a.2NO2+Na2CO3═NaNO3+NaNO2+CO2
b.NO+NO2+Na2CO3═2NaNO2+CO2
①吸收后的溶液經濃縮、結晶、過濾,得到NaNO2晶體。該晶體中的主要雜質是(填化學式);吸收后排放的尾氣中含量較高的氮氧化物是。(填化學式)
②根據反應b,每產生22.4L(標準狀況下)CO2吸收液質量將增加g。
(5)以合成氨為基礎的化肥工業對糧食增長的貢獻率占50%左右,但人類如果過度施用化肥,對環境造成影響是(任答1點);為了維持自然界中氮的平衡,除了合理施用化肥外,人類還可以采取措施是。(任答1點)組卷:31引用:1難度:0.7 -
24.高鐵酸鉀(K2FeO4)是一新型高效無毒的多功能水處理劑,可除水中氨氮、硫化物藻類等。K2FeO4易溶于水,微溶于濃KOH溶液,在0~5℃的強堿性溶液中較穩定,在酸性或中性溶液中快速產生O2。
Ⅰ.制備K2FeO4
實驗室利用如圖1裝置制備K2FeO4,其原理:3Cl2+2Fe(OH)3+10KOH═2K2FeO4+6KCl+8H2O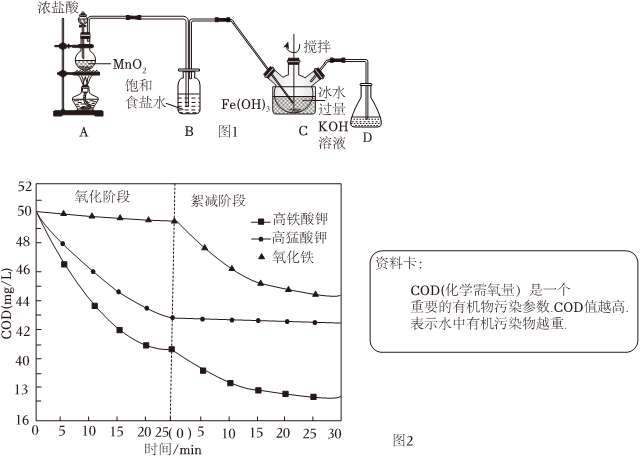
(1)盛放濃鹽酸的儀器名稱是,A中反應的化學方程式為。
(2)B中飽和食鹽水的作用是,實驗時C采用冰水浴的原因是。
(3)D中盛裝的試劑可選用。(填標號)
a.NaCl
b.FeCl2
c.H2SO4
d.NaOH
Ⅱ.探究K2FeO4的性質
某研究性小組通過K2FeO4與Na2S的反應來探究K2FeO4的性質。
已知:
①Fe2+遇鐵氰化鉀(K3[Fe(CN)6])溶液,可產生藍色沉淀。
②BaS是黃色或黑紅粉末,遇水逐漸水解為H2S和Ba(OH)2。
實驗步驟如表:
(4)請完成步驟1中反應的離子方程式:步驟 操作 現象 1 取0.1mol?L-1的Na2S溶液2mL于試管中,滴加幾滴0.1mol?L-1的鹽酸調至酸性,迅速加入少量K2FeO4固體,攪拌 - 2 取步驟1中溶液,滴加K3[Fe(CN)6]溶液 無明顯現象 3 取步驟1中溶液,滴加KSCN溶液 溶液變紅 4 取步驟1中溶液,滴加溶液BaCl2溶液 出現白色沉淀 +FeO2-4S2-+H+═++20H2O
(5)步驟3中溶液變紅的原因可能有兩個:一是K2FeO4與Na2S反應導致,二是(用文字作答)。
Ⅲ.探究K2FeO4對有機污染物的去除效果
(6)對比K2FeO4、KMnO4、FeCl3三種物質對有機污染物去除效果如圖2所示(三種試劑的初始濃度均為2.0×10-4mol?L-1)。氧化階段,去除有機污染物效果最好的試劑是;絮凝階段,幾乎不具備絮凝能力的試劑是。綜上分析,K2FeO4作為優異的有機污染物去除劑的理由是。組卷:13引用:1難度:0.6


