2021-2022學年廣東省清遠市高一(下)期中化學試卷
發布:2024/12/3 16:0:2
一、選擇題:本題共30小題,每小題2分,共60分。在每小題給出的四個選項中,只有一項是符合題目要求的。
-
1.下列物質中不含硅元素的是( )
A.石英 B.石灰石 C.水泥 D.瑪瑙 組卷:4引用:1難度:0.8 -
2.2022年1月7日,PLOS Biology在線發表了關于玉米生物固氮的研究,為減少化肥使用和發展綠色農業提供重要的理論指導。下列反應中,屬于氮的固定的是( )
A.由氨制成碳酸氫銨或硫酸銨 B.NO2與H2O反應生成HNO3 C.NO和O2反應生成NO2 D.N2和H2在一定條件下合成氨 組卷:56引用:2難度:0.9 -
3.下列敘述正確的是( )
A.氨水和液氨不同,氨水是混合物,液氨是純凈物 B.氨水濃度越大,密度也越大 C.氨氣與氯化氫氣體相遇產生白色煙霧 D.在反應NH3+H+= 中,NH3失去電子被氧化NH+4組卷:8引用:1難度:0.7 -
4.下列物質在一定條件下能夠與硫發生反應,且硫作還原劑的是( )
A.O2 B.Fe C.H2 D.Zn 組卷:91引用:4難度:0.9 -
5.下列關于濃硫酸和稀硫酸的敘述中正確的是( )
A.都能作干燥劑 B.加熱時都能與銅發生反應 C.都具有一定的氧化性 D.在常溫下都能用鐵制容器貯存 組卷:66引用:8難度:0.9 -
6.現代社會的發展與進步離不開材料。下列有關說法正確的是( )
A.“遼寧艦”上用于艦載機降落的阻攔索是一種特種鋼纜,屬于新型純金屬材料 B.“中國天眼”FAST用到的碳化硅屬于新型陶瓷材料 C.“港珠澳大橋”使用了大量的鋼鐵,鋼鐵屬于傳統無機非金屬材料 D.某品牌手機使用的麒麟980芯片的主要成分是二氧化硅 組卷:6引用:1難度:0.7 -
7.下列關于能量轉換的認識中不正確的是( )
A.氫氧燃料電池反應時,化學能轉化為電能 B.綠色植物進行光合作用時,太陽能轉化為化學能 C.煤燃燒時,化學能主要轉化為熱能 D.白熾燈工作時,電能全部轉化為光能 組卷:69引用:4難度:0.8 -
8.下列有關物質的性質與用途對應關系錯誤的是( )
A.SO2具有漂白性、防腐性、抗氧化性,可作為食品添加劑 B.濃硫酸具有吸水性,可用于干燥Cl2 C.NH3易溶于水,可用作制冷劑 D.氮氣常溫下化學性質穩定,可用作糧食保護氣 組卷:1引用:2難度:0.7 -
9.在給定條件下,下列選項所示的物質間轉化均能一步實現的是( )
A.Fe FeCl2Cl2點燃Fe(OH)2NaOH(aq)B.S SO3O2點燃H2SO4H2SO4C.N2 NO2O2放電HNO3H2OD.CaCO3 CaO高溫CaSiO3SiO2高溫組卷:31引用:2難度:0.7 -
10.設阿伏加德羅常數的值為NA,則下列說法正確的是( )
A.7.8gNa2O2和Na2S的混合物中含有的陰離子數目為0.1NA B.在標準狀況下,體積為22.4L的SO3含有的質子數為40NA C.常溫下,1molFe分別放入足量的濃HNO3、稀HNO3中,反應后轉移的電子數均為3NA D.將18mol?L-1的濃硫酸50mL與足量銅粉共熱,產生的SO2分子數為0.45NA 組卷:3引用:1難度:0.7 -
11.下列指定反應的離子方程式書寫正確的是( )
A.向NaOH溶液中通入少量SO2:SO2+2OH-=H2O+ SO2-3B.將FeO固體放入稀硝酸中:FeO+2H+=Fe2++H2O C.將銅片放入濃硫酸中加熱:Cu+4H++ SO2-4Cu2++SO2↑+2H2O△D.向NH4HCO3溶液中加足量NaOH溶液: +OH-=HCO-3+H2OCO2-3組卷:4引用:1難度:0.7
二、非選擇題:本題共4小題,共40分。
-
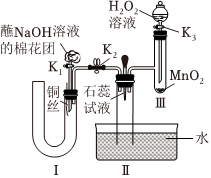 33.硝酸是極其重要的化工原料,工業上將產生的NO2在密閉容器中用水多次反復循環吸收制備硝酸.
33.硝酸是極其重要的化工原料,工業上將產生的NO2在密閉容器中用水多次反復循環吸收制備硝酸.
(1)工業上用水吸收NO2生產HNO3,生成的氣體經多次氧化、吸收的循環操作充分轉化為硝酸(假定上述過程無其他損失).試寫出上述反應的化學方程式:.
(2)為了證明NO也可以與氧氣和水共同反應生成HNO3,某學生設計了如圖所示裝置(有關夾持裝置已略去).
①檢查裝置氣密性良好后,為觀察到NO氣體生成,打開K1,關閉K2,應從U形管的長管口注入稀硝酸至后,迅速關閉K1,觀察到U形管內的現象是.
②裝置Ⅲ中發生反應的化學方程式為.
③蘸NaOH溶液的棉花團的作用是.
④打開K2,至裝置Ⅱ中長玻璃管中的氣體呈無色后,打開K3,反應一段時間后,長玻璃管中并未充滿液體.設計簡單方法檢驗長玻璃管中的氣體是否含NO.組卷:496引用:5難度:0.1 -
34.一定溫度下,在體積為0.5L的恒容密閉容器中,NO2和N2O4之間發生反應:2NO2(g)(紅棕色)?N2O4(g)(無色),反應過程中各物質的物質的量與時間的關系如圖1所示。回答下列問題:
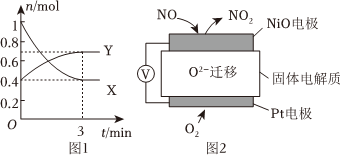
(1)曲線(填“X”或“Y”)表示N2O4的物質的量隨時間的變化曲線。
(2)在0~3min內,用NO2表示的反應速率為。
(3)若在一保溫容器中加入一定量NO2,反應一段時間后,混合氣體溫度升高,說明2molNO2(g)的能量比1molN2O4(g)的能量(填“高”或“低”)。
(4)反應達到平衡后,若降低溫度,混合氣體的顏色變淺,相對于降溫前v(正)(填“增大”“減小”或“不變”,下同),v(逆)。
(5)氮氧化物是重要的大氣污染物,圖2是監測NO含量的傳感器工作原理示意圖。NiO電極發生(填“氧化”或“還原”)反應,Pt電極是電池(填“正極”或“負極”)。組卷:28引用:4難度:0.6


