2020-2021學年江蘇省常州市武進區橫山橋高級中學高一(下)期末化學試卷
發布:2024/4/20 14:35:0
一、單項選擇題:共15題,每題3分,共45分。每題只有一個選項最符合題意。
-
1.化學與生活、生產密切相關,下列說法不正確的是( )
A.低碳生活就是節能減排,使用太陽能等代替化石燃料,可減少溫室氣體的排放 B.高純度的硅單質廣泛用于制作光導纖維 C.“綠色化學”的核心內容之一是使原料盡可能全部轉化為目標產物 D.“奮斗者”號潛水器外殼材料為鈦合金,鈦合金耐腐蝕,耐高壓 組卷:12引用:3難度:0.7 -
2.有關化學用語正確的是( )
A.氯原子的結構示意圖: 
B.乙醇的結構式:C2H6O C.氯化鈉的電子式: 
D.甲烷的球棍模型:  組卷:34引用:2難度:0.6
組卷:34引用:2難度:0.6 -
3.下列反應起了氮的固定作用是( )
A.N2和H2在一定條件下反應生成NH3 B.NH3經催化氧化生成NO C.NO與O2反應生成NO2 D.由NH3制碳銨或硫銨 組卷:55引用:4難度:0.8 -
4.鐵片與稀硫酸反應制氫氣,下列措施不能使氫氣生成速率加快的是( )
A.加熱 B.用鐵粉代替鐵片 C.滴加適量CuSO4溶液 D.用98%的濃硫酸代替稀硫酸 組卷:27引用:5難度:0.7 -
5.下列反應屬于吸熱反應的是( )
A.石灰石在高溫下的分解反應 B.生石灰和水的反應 C.鹽酸與氫氧化鈉溶液的反應 D.木炭在氧氣中燃燒 組卷:357引用:47難度:0.9 -
6.某溶液中存在大量的H+、Cl-、SO42-,該溶液中還可能大量存在的是( )
A.OH- B.Ba2+ C.Fe3+ D.CO32- 組卷:12引用:6難度:0.5
二、非選擇題:共4題,共55分。
-
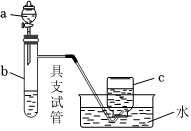 18.如圖是用濃硝酸、銅片、水等試劑探究濃、稀硝酸的強氧化性并觀察還原產物的實驗裝置。
18.如圖是用濃硝酸、銅片、水等試劑探究濃、稀硝酸的強氧化性并觀察還原產物的實驗裝置。
Ⅰ.濃硝酸的強氧化性實驗
將銅片置于具支試管的底部,在分液漏斗中加入約5mL濃硝酸,往具支試管中放入約2mL濃硝酸,用排水法收集產生的氣體。
(1)具支試管中發生反應的化學方程式:。
(2)實驗中觀察到能證明濃硝酸具有強氧化性的現象。
Ⅱ.稀硝酸的強氧化性實驗
(3)上述反應完成后,欲進一步證明稀硝酸也具有強氧化性,緊接的簡便、合理的實驗操作是。
(4)能證明稀硝酸與銅反應產生NO的實驗現象是(填寫序號)。
A.c中收集到無色氣體
B.c中收集到的無色氣體接觸空氣后變為紅棕色
C.b中產生的無色氣體接觸空氣后變為紅棕色
Ⅲ.實驗反思
(5)利用該裝置先進行銅與濃硝酸反應,再進行銅與稀硝酸反應的實驗,其好處是。
Ⅳ.問題討論
用等質量的銅片與等體積的濃硝酸、稀硝酸(硝酸均過量)反應時,發現反應后所得溶液前者呈綠色,后者呈藍色。對此有兩種看法:
①兩者顏色不同的原因是因為Cu2+濃度差異引起的。
②前者溶液呈綠色,是因為生成的紅棕色NO2溶解于溶液中引起的。
(6)你認為上述看法(填“①”或“②”)合理。若是①合理,說明理由,若是②合理,設計一個簡單實驗證明:。組卷:33引用:3難度:0.4 -
19.能源是現代文明的原動力,通過化學方法可以使能量按人們所期望的形式轉化,從而開辟新能源和提高能源的利用率,請回答下列問題。
(1)工業合成氨反應N2+3H2?2NH3是放熱的可逆反應,反應條件是高溫、高壓,并且需要合適的催化劑。已知1mol N2完全反應生成NH3可放出92kJ熱量。如果將10 mol N2和足量H2混合,使其充分反應,放出的熱量(填“大于”“小于”或“等于”)920 kJ。
(2)實驗室模擬工業合成氨時,在容積為2L的密閉容器內,反應經過10 min后,生成10 mol NH3。
①用N2表示的化學反應速率為。
②一定條件下,能說明該反應進行到最大限度的是(填序號)
a.N2的轉化率達到最大值
b.N2、H2和NH3的體積分數之比為1:3:2
c.體系內氣體的密度保持不變
d.體系內各物質的濃度保持不變
(3)用CH4和O2組合形成的質子交換膜燃料電池的結構如圖所示:
①電極d是(填“正極”或“負極”),電極c的電極反應式為。
②若線路中轉移2mol電子,則該燃料電池理論上消耗的O2在標準狀況下的體積為L。組卷:23引用:1難度:0.6


