2023年江蘇省鎮江十中中考化學模擬試卷(三)
發布:2024/6/11 8:0:9
一、單項選擇題(本題包括15小題,每小題2分,共30分。每小題只有一個選項符合題意)
-
1.下列屬于純凈物的是( )
A.食用醋 B.鹽酸 C.潔凈空氣 D.硫酸銅晶體 組卷:44引用:1難度:0.8 -
2.下列現象主要是由化學變化引起的是( )
A.花香四溢 B.空氣液化 C.鹽酸除銹 D.海水曬鹽 組卷:50引用:3難度:0.9 -
3.下列物質的用途主要與其化學性質有關的是( )
A.活性炭用作冰箱除味劑 B.干冰用于制作舞臺云霧 C.2%濃度的雙氧水消毒 D.武德合金制作電路保險絲 組卷:68引用:1難度:0.9 -
4.下列做法正確的是( )
A.回收塑料,再生減污 B.焚燒秸稈,增肥農田 C.深埋電池,消除污染 D.禁用農藥,保護水源 組卷:37引用:6難度:0.8 -
5.下列歸類正確的是( )
選 項 歸 類 內容 A 化石燃料 煤、酒精、可燃冰 B 常見溶液 碘酒、食鹽水、波爾多液 C 營養物質 油脂、糖類、蛋白質 D 復合肥料 KNO3、CO(NH2)2、(NH4)2HPO4 A.A B.B C.C D.D 組卷:17引用:1難度:0.8 -
6.實驗室得到并驗證H2的部分性質。下列實驗裝置和原理不能達到實驗目的的是( )
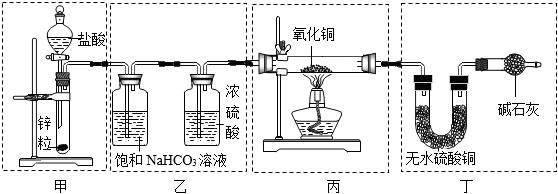
A.裝置甲制取H2 B.裝置乙得到純凈干燥H2 C.裝置丙證明H2的還原性 D.裝置丁證明丙中反應生成H2O 組卷:66引用:4難度:0.5 -
7.下列實驗方法正確的是( )
A.用明礬對自來水進行殺菌消毒 B.用飽和硫酸銨溶液區別蒸餾水和雞蛋清溶液 C.用加碘鹽檢驗淀粉 D.用濕潤的pH試紙測某溶液的pH 組卷:54引用:2難度:0.6 -
8.下列排序正確的是( )
A.利用金屬的年代: Al、Cu、Fe由先到后B.鐵元素質量分數: FeO、Fe2O3、Fe3O4由高到低C.硫元素的化合價: MgS、S、SO2由高到低D.物質在水中的溶解性: CaCl2、CaSO4、CaCO3由大到小組卷:17引用:3難度:0.6 -
9.下列指定反應的化學方程式正確的是( )
A.硫在空氣中燃燒:2S+3O2 2SO3點燃B.碳酸氫鎂受熱分解:Mg(HCO3)2 MgO+2CO2↑+H2O△C.用氫氧化鋁中和過多胃酸:2Al(OH)3+3H2SO4═Al2(SO4)3+6H2O D.用食鹽生產氯氣和燒堿:2NaCl+H2O Cl2↑+2NaOH+H2↑通電組卷:86引用:2難度:0.6 -
10.利用CH4和H2O進行催化重整制氫氣,反應前后數觀示意圖如圖。
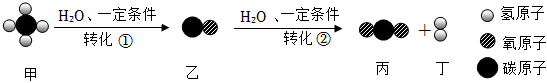
下列說法正確的是( )A.轉化①是化合反應 B.轉化過程中共有四種氧化物 C.轉化②反應前后分子的個數不變 D.甲、乙、丙中碳元素的質量分數依次升高 組卷:52引用:3難度:0.6
第Ⅱ卷(非選擇題  共60分)
-
29.有一包白色固體粉末,可能含有FeCl3、Na2CO3、Ba(NO3)2、(NH4)2SO4、NaCl、NaOH中的一種或幾種。現做如下實驗:
(1)取少量固體加熱,產生的氣體使濕潤的紅色石蕊試紙變藍,則原固體中一定含有。
(2)另取少量固體溶于足量水中,過濾得到白色固體A和無色濾液B,則原固體中一定不含有,向固體A中加入足量稀鹽酸,固體部分溶解,則原固體中還一定含有。
(3)向濾液B中先加入足量的稀硝酸和硝酸鋇,靜置,在上層清液中再加入AgNO3溶液,無現象,則原固體中一定不含有,可能含有。組卷:46引用:1難度:0.5 -
30.鋁及化合物有極其重要的用途。
(一)鋁的廣泛應用
(1)鋁是很活潑的金屬,但用鋁制作的炊具卻耐腐蝕,其原因用方程式表示是。使用鋁制炊具會使人體攝入過量的“鋁”,導致記憶力減退等許多不良癥狀。這里的“鋁”是指。
A.單質
B.元素
C.原子
D.分子
(2)氫能源是最理想的能源,科學家研發出一種以“鋁鎵合金”和水為原料制取氫氣的新工藝。“鋁鎵合金”它屬于(選填序號)。
A.金屬材料
B.無機非金屬材料
C.合成材料
D.復合材料
(3)實驗室可用鋁片與稀鹽酸反應制備氫氣,寫出該反應的化學方程式:。
(二)硫酸鋁銨晶體制取的探究
硫酸鋁銨是一種用途廣泛的含鋁化合物。以某鋁土礦(主要成分Al2O3,含少量SiO2、Fe2O3雜質)為原料制硫酸鋁銨晶體【(NH4)aAlb(SO4)c?xH2O】的流程如下: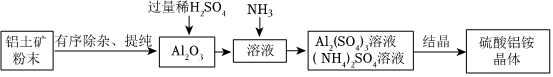
(4)鋁土礦粉碎的目的是。
(5)有關上述流程的說法正確的是。
a.“有序除雜、提純”中有先加過量稀鹽酸再過濾,該做法的目的是除去SiO2
b.稀硫酸過量的目的只是保證純Al2O3溶解完全
(三)硫酸鋁銨晶體分解的定性探究
硫酸鋁銨熱分解可得到納米氧化鋁。興趣小組在科研人員指導下設計實驗探究硫酸鋁銨晶體受熱分解的產物。(6)甲組同學設計了如圖1所示實驗裝置: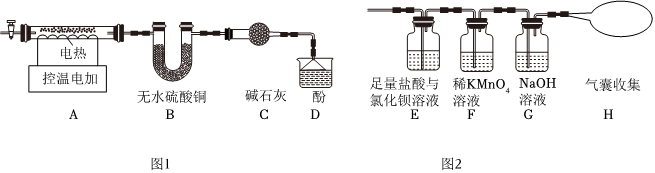
①實驗中,裝置B中觀察到的現象是;
②裝置D中觀察到酚酞溶液變紅色,由此可知分解的產物中有(寫化學式)。
(7)乙組同學認為硫酸鋁銨晶體受熱分解的產物中還有SO2、SO3和N2。為進行驗證,用甲組實驗中的裝置A和圖2所示裝置連接進行實驗。觀察到裝置E中,證明了有SO3生成;而F裝置中、H中最終沒有脹大,表明沒有SO2和N2生成。
(四)硫酸鋁銨晶體成分的定量探究
(8)為確定硫酸鋁銨晶體的組成,進行如下實驗:
【實驗1】稱取45.3g樣品與足量氯化鋇溶液充分反應,生成白色沉淀46.6g。
【實驗2】稱取45.3g樣品在空氣中持續加熱,測定剩余固體質量隨溫度變化的曲線如圖所示。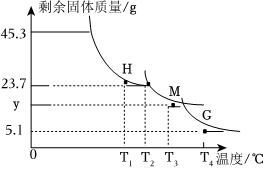
①固體H是T1℃剛好完全失去結晶水的產物,則結晶水的個數x=。
②T3℃時固體M為硫酸鋁,y質量為。
③請寫出T2℃→T4℃段發生反應的總化學方程式:。組卷:176引用:1難度:0.1


