人教版(2019)必修第二冊(cè)《8.1.1 金屬礦物的開(kāi)發(fā)利用》2021年同步練習(xí)卷(1)
發(fā)布:2024/4/20 14:35:0
一、單選題
-
1.金屬冶煉方法選擇的依據(jù)是( )
A.金屬熔點(diǎn)的高低 B.金屬陽(yáng)離子得電子的能力 C.金屬元素在自然界的存在形式 D.金屬元素在地殼中的含量 組卷:14引用:2難度:0.8 -
2.如圖所示為人類(lèi)使用不同金屬的大致年代。這個(gè)先后順序與下列因素有關(guān)的是( )
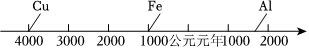
①地殼中金屬元素的含量
②金屬活動(dòng)性順序
③金屬的導(dǎo)電性
④金屬冶煉的難易程度
⑤金屬的延展性A.①③ B.②⑤ C.③⑤ D.②④ 組卷:61引用:4難度:0.8 -
3.下列各組金屬最適合用H2或CO把它從化合物中還原出來(lái)的為( )
A.Ca Mg B.Al Fe C.Fe Cu D.Hg Ag 組卷:67引用:5難度:0.9 -
4.金屬材料在日常生活、生產(chǎn)中有著廣泛的運(yùn)用,下列關(guān)于金屬的說(shuō)法不正確的是( )
A.工業(yè)上金屬M(fèi)g、Al都是用電解熔融的氯化物制得的 B.合金的性質(zhì)與其成分金屬的性質(zhì)不完全相同 C.金屬冶煉的本質(zhì)是金屬陽(yáng)離子得到電子變成金屬原子 D.越活潑的金屬越難冶煉 組卷:35引用:6難度:0.9
三、選做題
-
11.鋁熱反應(yīng)常用于冶煉高熔點(diǎn)的金屬,可簡(jiǎn)單認(rèn)為是鋁與某些金屬氧化物在高溫條件下發(fā)生的反應(yīng).某學(xué)習(xí)小組對(duì)鋁熱反應(yīng)(以Al和Fe2O3反應(yīng)為例)實(shí)驗(yàn)進(jìn)行研究.查閱數(shù)據(jù)得到Al、Al2O3、Fe、Fe2O3的熔點(diǎn)、沸點(diǎn)數(shù)據(jù)如下表所示:
試回答下列問(wèn)題:物質(zhì) Al Al2O3 Fe Fe2O3 熔點(diǎn)/℃ 660 2054 1535 1565 沸點(diǎn)/℃ 2467 2980 2750 …
(1)在鋁熱反應(yīng)中金屬鋁表現(xiàn)出性(填“氧化”或“還原”).請(qǐng)判斷下列金屬中那一個(gè)不能由鋁熱反應(yīng)制取.(填序號(hào))
①Fe ②Cr(鉻) ③V(釩) ④Ca ⑤Mn
(2)某同學(xué)推測(cè),鋁熱反應(yīng)所得到的熔融物中應(yīng)含有鐵、鋁兩種金屬.如設(shè)計(jì)一個(gè)簡(jiǎn)單的實(shí)驗(yàn)方案證明該熔融物中含有金屬鋁,則實(shí)驗(yàn)所需用的試劑為,可觀察到的實(shí)驗(yàn)現(xiàn)象是.
(3)另一同學(xué)推測(cè)鋁熱反應(yīng)得到的熔融物中還含有Fe2O3,他設(shè)計(jì)了如下方案來(lái)驗(yàn)證:
取一塊該熔融物投入到少量稀硫酸中,向反應(yīng)后的混合液中滴加物質(zhì)甲的溶液,觀察溶液顏色未變血紅色,即可證明熔融物中不含有Fe2O3.則
①物質(zhì)甲是(填化學(xué)式).
②該同學(xué)的實(shí)驗(yàn)方案是否合理?(填“合理”或“不合理”).理由:.組卷:61引用:4難度:0.1 -
12.從鋁土礦(主要成分為Al2O3,還有少量雜質(zhì)Fe2O3等)中提取鋁的工藝流程及步驟如圖。
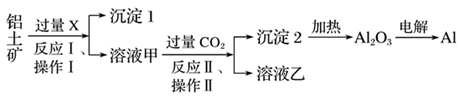
試回答下列問(wèn)題:
(1)試劑X為。反應(yīng)Ⅰ離子方程式:。
(2)寫(xiě)出以上工藝流程中反應(yīng)Ⅱ的離子方程式:。
(3)檢驗(yàn)沉淀2是否洗凈的實(shí)驗(yàn)操作:。
(4)操作Ⅰ、操作Ⅱ均為(填操作名稱(chēng)),在進(jìn)行該操作時(shí)需要的玻璃儀器有。
(5)電解熔融氧化鋁制取金屬鋁,若有12mol電子發(fā)生轉(zhuǎn)移,理論上能得到金屬鋁的質(zhì)量是g。組卷:6引用:1難度:0.5


