2015-2016學年廣東省廣州大學附中黃華路校區高三(上)晚練化學試卷
發布:2024/4/20 14:35:0
一、選擇題:本題共7小題,每小題6分,在每小題給出的四個選項中,只有一項是符合題目要求的
-
1.下列離子方程式表達的反應事實正確的是( )
A.Fe3O4與稀硝酸反應:Fe3O4+8H+═2Fe3++Fe2++4H2O B.向硫酸銨溶液中加入氫氧化鋇溶液:Ba2++SO42-═BaSO4↓ C.向碳酸鎂中加入稀鹽酸:CO32-+2H+═CO2↑+H2O D.20 mL 0.2 mol?L-1FeBr2溶液與0.004 mol的Cl2反應:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2 組卷:15引用:1難度:0.7 -
2.研究人員發明了一種“海水”電池,其電池總反應可表示為:5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl,下列有關說法正確的是( )
A.正極反應式:Ag+Cl--e-═AgCl B.每生成1molNa2Mn5O10轉移2 mol電子 C.Na+不斷向“水”電池的負極移動 D.電子從電源的正極經外電路流向負極 組卷:21引用:2難度:0.7
一、選擇題:本題共7小題,每小題6分,在每小題給出的四個選項中,只有一項是符合題目要求的
-
7.設NA為阿伏加德羅常數的值.下列說法正確的是( )
A.0.56L甲烷中含有的共價鍵數為0.1NA B.標準狀況下,1mol SO3含有的氧原子數為3NA C.含1mol AlCl3的溶液中,Al3+總數為NA D.pH=1的稀硫酸中含有的H+數為0.1NA 組卷:8引用:2難度:0.7
二.非選擇題
-
8.某研究小組為探究弱酸性條件下鐵發生電化學腐蝕類型的影響因素,將混合均勻的新制鐵粉和碳粉置于錐形瓶底部,塞上瓶塞(如圖1)。從膠頭滴管中滴入幾滴醋酸溶液,同時測量容器中的壓強變化。
(1)請完成以下實驗設計表(表中不要留空格):
(2)編號①實驗測得容器中壓強隨時間變化如圖2.t2時,容器中壓強明顯小于起始壓強,其原因是鐵發生了編號 實驗目的 碳粉/g 鐵粉/g 醋酸/% ① 為以下實驗作參照 0.5 2.0 90.0 ② 醋酸濃度的影響 0.5 36.0 ③ 0.2 2.0 90.0 腐蝕,請在圖3中用箭頭標出發生該腐蝕時電子流動方向;此時,碳粉表面發生了(填“氧化”或“還原”)反應,其電極反應式是。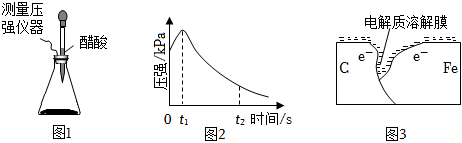
(3)該小組對圖2中0-t1時壓強變大的原因提出了如下假設,請你完成假設二:假設一:發生析氫腐蝕產生了氣體;
假設二:;
…
(4)為驗證假設一,某同學設計了檢驗收集的氣體中是否含有H2的方案,請你再設計一個實驗方案驗證假設一,寫出實驗步驟和結論。組卷:418引用:7難度:0.1


