2021-2022學(xué)年湖北省荊州市八縣市高一(上)期末化學(xué)試卷
發(fā)布:2024/12/9 10:30:2
一、選擇題(本題共15小題,每小題3分,共45分。在每小題給出的四個選項中,只有一項是符合題目要求的)
-
1.“中國”一詞最早見于西周的青銅器(主要成分為銅、錫、鉛等)上。下列有關(guān)青銅的說法中錯誤的是( )
A.冶煉技術(shù)早于煉鐵 B.具有導(dǎo)電性 C.熔點(diǎn)高于純銅 D.硬度大于純鉛 組卷:75引用:4難度:0.8 -
2.日本福島核電站的核原料鈾?235(
U)裂變釋放出具有放射性的碘?131(23592I)和銫?137(13153Cs),關(guān)于它們的說法正確的是( )13755A.127I與131I互為同素異形體 B.137Cs的中子數(shù)為55 C.鈾?235的質(zhì)量數(shù)是235 D.銫與水的反應(yīng)比鈉與水的反應(yīng)緩慢 組卷:26引用:1難度:0.8 -
3.下列關(guān)于電子式的描述正確的是( )
A.Na2O: 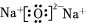
B.CCl4: 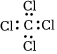
C.MgCl2: 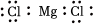
D.O2的電子式: 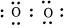 組卷:71引用:2難度:0.8
組卷:71引用:2難度:0.8 -
4.下列反應(yīng)不屬于四種基本反應(yīng)類型,但屬于氧化還原反應(yīng)的是( )
A.Fe+CuSO4=FeSO4+Cu B.AgNO3+NaCl=AgCl↓+NaNO3 C.Fe2O3+3CO 2Fe+3CO2高溫D.MgCl2(熔融) Mg+Cl2↑電解組卷:102引用:8難度:0.9 -
5.磁流體是電子材料的新秀,它既具有固體的磁性,又具有液體的流動性。制備時將含等物質(zhì)的量的硫酸亞鐵和硫酸鐵的溶液混合,再滴入稍過量的氫氧化鈉溶液,隨后加入油酸鈉溶液,即可生成黑色的、分散質(zhì)粒子直徑在36~55nm的磁流體。下列說法中正確的是( )
A.該磁流體是一種純凈物 B.所得的磁流體為懸濁液 C.該磁流體很不穩(wěn)定 D.所得的磁流體能產(chǎn)生丁達(dá)爾效應(yīng) 組卷:407引用:24難度:0.7 -
6.中國傳統(tǒng)文化對人類文明貢獻(xiàn)巨大,很早就把化學(xué)技術(shù)應(yīng)用到生產(chǎn)生活中。下列與化學(xué)有關(guān)的說法不正確的是( )
A.侯氏制堿法的工藝過程中應(yīng)用了物質(zhì)溶解度的差異 B.《神農(nóng)本草經(jīng)》中提到:“白青[Cu2(OH)2CO3]得鐵化為銅”,其中白青屬于堿 C.《本草綱目》中記載“(火藥)乃焰消(KNO3)、硫磺、杉木炭所合,以烽燧銃極”這是利用了“KNO3的氧化性” D.《本草經(jīng)集注》中記載了區(qū)分硝石(KNO3)和樸硝(Na2SO4)的方法:“以火燒之,煙起,乃真硝石也”,二者也可以利用“焰色試驗(yàn)”區(qū)分 組卷:105引用:11難度:0.7
二、非選擇題(本題共5小題,共55分)
-
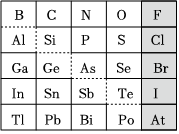 19.1869年俄國化學(xué)家門捷列夫制出第一張元素周期表,到現(xiàn)在形成的周期表經(jīng)過了眾多化學(xué)家的艱辛努力,歷經(jīng)142年。元素周期表體現(xiàn)了元素位構(gòu)性的關(guān)系,揭示了元素間的內(nèi)在聯(lián)系。下圖是元素周期表的一部分,回答下列問題:
19.1869年俄國化學(xué)家門捷列夫制出第一張元素周期表,到現(xiàn)在形成的周期表經(jīng)過了眾多化學(xué)家的艱辛努力,歷經(jīng)142年。元素周期表體現(xiàn)了元素位構(gòu)性的關(guān)系,揭示了元素間的內(nèi)在聯(lián)系。下圖是元素周期表的一部分,回答下列問題:
(1)元素Ga在元素周期表中的位置為:第周期第族。
(2)Sn的最高正價為,Cl的最高價氧化物對應(yīng)水化物的化學(xué)式為,Bi的最高價氧化物為。
(3)根據(jù)元素周期律,推斷:
①陰影部分元素氫化物熱穩(wěn)定性最高的是元素(填化學(xué)式)。
②H3AsO4、H2SeO4的酸性強(qiáng)弱:H3AsO4(填“>”“<”或“=”)H2SeO4。
③氫化物的還原性:H2O(填“>”“<”或“=”)H2S。
④原子半徑比較:N(填“>”“<”或“=”)Si。組卷:61引用:3難度:0.8 -
20.高鐵酸鉀(K2FeO4)是一種高效多功能的新型非氯綠色消毒劑。實(shí)驗(yàn)小組欲制備高鐵酸鉀并探究其性質(zhì)。已知:K2FeO4為紫色固體,具有強(qiáng)氧化性;在堿性溶液中較穩(wěn)定,微溶于KOH溶液;在酸性或中性溶液中快速產(chǎn)生O2,
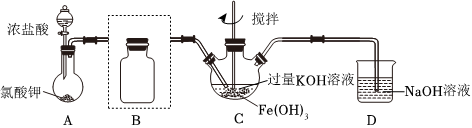
(1)除了用二氧化錳和濃鹽酸反應(yīng)外,實(shí)驗(yàn)室可以用氯酸鉀和濃鹽酸反應(yīng)制取氯氣,反應(yīng)方程式如下:KClO3+6HCl(濃)═KCl+3Cl2↑+3H2O。
①濃鹽酸在反應(yīng)中顯示出來的性質(zhì)是性和性,用雙線橋表示該反應(yīng)中電子轉(zhuǎn)移的情況。
②若產(chǎn)生標(biāo)況下6.72LCl2,則被氧化的HCl的物質(zhì)的量為mol。
③如果要將裝置B補(bǔ)充完整,除需用導(dǎo)管外,試劑瓶中還應(yīng)裝的除雜試劑為。
(2)C中得到紫色固體和溶液。C中Cl2發(fā)生的反應(yīng)有3Cl2+2Fe(OH)3+10KOH═K2FeO4+6KCl+8H2O。另外還有。(用離子方程式表示)
(3)探究K2FeO4的性質(zhì)
取C中紫色溶液,加入稀硫酸,產(chǎn)生黃綠色氣體,得溶液a,經(jīng)檢驗(yàn)氣體中含有Cl2。為證明是否K2FeO4氧化了Cl-而產(chǎn)生Cl2,設(shè)計如下方案:
方案一:取少量a,滴加KSCN溶液至過量,溶液呈血紅色
方案二:用KOH溶液充分洗滌C中所得固體,除去固體表面附著的ClO-,防止其氧化Cl-,再用KOH溶液將K2FeO4溶出,得到紫色溶液b。取少量b,滴加鹽酸,有Cl2產(chǎn)生。
①由方案一中溶液變紅可知a中含有(填離子符號),但該離子的產(chǎn)生不能判斷一定是K2FeO4將Cl-氧化所得,還可能由產(chǎn)生(文字描述)。
②根據(jù)K2FeO4的制備實(shí)驗(yàn)得出:氧化性Cl2(填“>”或“<”),而方案二實(shí)驗(yàn)中Cl2和FeO2-4的氧化性強(qiáng)弱關(guān)系與之相反,原因是FeO2-4。組卷:19引用:3難度:0.7


